Новый курс НМО
Грипп у взрослых
классификации болезней и проблем, связанных со здоровьем:J9, J10, J11
Список сокращений
АД – артериальное давление
АПТВ – активированное парциальное тромбопластиновое время
В/м – внутримышечное введение
ВОЗ – Всемирная организация здравоохранения
ГБ – гипертоническая болезнь
ГПЗ – гриппоподобное заболевание
ДВС-синдром – синдром диссеминированного внутрисосудистого свертывания
Д.м.н. – доктор медицинских наук
ДНК - дезоксирибонуклеиновая кислота
ДЦП – детский церебральный паралич
ИБС – ишемическая болезнь сердца
ИВЛ – искусственная вентиляция легких
ИМП – инструкция по медицинскому применению
ИТШ – инфекционно-токсический шок
ИТЭП – инфекционно-токсическая энцефалопатия
ИФА – иммуноферментный анализ
КДа – килодальтон
К.м.н. – кандидат медицинских наук
КТ – компьютерная томография
ЛС – лекарственное средство
Мг – миллиграмм
МКБ-10 – международная классификация болезней, травм, и состояний, влияющих на здоровье 10-го пересмотра
МНН – международное непатентованное наименование
МКП – миокардиопатия
МЗ РФ – Министерство здравоохранения Российской Федерации
Мин. – минута
Мл – миллилитр
Мм рт. ст. – миллиметров ртутного столба
ОДН – острая дыхательная недостаточность
ОРВИ – острая респираторная вирусная инфекция
ОРИ – острая респираторная инфекция
ОРДС – острый респираторный дистресс-синдром
ОРИТ – отделение реанимации и интенсивной терапии
ОРЗ – острые респираторные заболевания
ОССН – острая сердечная и сосудистая недостаточность
ОСТЛ – острый стенозирующий ларинготрахеит
ОТ-ПЦР – полимеразная цепная реакция с обратной транскрипцией
ПИФ – прямая иммунофлюоресценция
ПЦР – полимеразная цепная реакция
ПЦР-РВ – полимеразная цепная реакция в реальном времени
РИФ – реакция иммунофлюоресценции
РКИ – рандомизированное контролируемое исследование
РНК – рибонуклеиновая кислота
РПИФ – реакция прямой иммунофлуоресценции
РС-инфекция – инфекция, вызванная респираторно-синцитиальным вирусом
РСК - реакция связывания комплементов
РТГА – реакция торможения гемагглютинации
РФ – Российская Федерация
СМЖ – спинномозговая жидкость
СОЭ – скорость оседания эритроцитов
ТВО – тепловлагообменник
ТОРИ – тяжелая острая респираторная инфекция
ТОРС – тяжелый острый респираторный синдром
Уд./мин. – ударов в минуту
ХОБЛ – хроническая обструктивная болезнь легких
ЦНС – центральная нервная система
ЧДД – частота дыхательных движений
ЧСС – частота сердечных сокращений
ЭКГ – электрокардиография
ЭКМО – экстракорпоральная мембранная оксигенация
H – гемагглютинин
N – нейраминидаза
O2СТ– содержание кислорода
РO2– парциальное давление кислорода
РСO2 – парциальное давление углекислого газа
рН – водородный показатель
SaO2 – насыщение кислородом
WHO -World Health Organization
Термины и определения
Доказательная медицина – подход к медицинской практике, при котором решения о применении профилактических, диагностических и лечебных мероприятий принимаются исходя из имеющихся доказательств их эффективности и безопасности, а такие доказательства подвергаются поиску, сравнению, обобщению и широкому распространению для использования в интересах пациентов
Заболевание - возникающее в связи с воздействием патогенных факторов нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма.
Основное заболевание - заболевание, которое само по себе или в связи с осложнениями вызывает первоочередную необходимость оказания медицинской помощи в связи с наибольшей угрозой работоспособности, жизни и здоровью, либо приводит к инвалидности, либо становится причиной смерти;
Сопутствующее заболевание - заболевание, которое не имеет причинно-следственной связи с основным заболеванием, уступает ему в степени необходимости оказания медицинской помощи, влияния на работоспособность, опасности для жизни и здоровья и не является причиной смерти;
Тяжесть заболевания или состояния - критерий, определяющий степень поражения органов и (или) систем организма человека либо нарушения их функций, обусловленные заболеванием или состоянием либо их осложнением;
Исходы заболеваний - медицинские и биологические последствия заболевания;
Последствия (результаты) - исходы заболеваний, социальные, экономические результаты применения медицинских технологий;
Осложнение заболевания - присоединение к заболеванию синдрома нарушения физиологического процесса; - нарушение целостности органа или его стенки; - кровотечение; - развившаяся острая или хроническая недостаточность функции органа или системы органов;
Инструментальная диагностика – диагностика с использованием для обследования больного различных приборов, аппаратов и инструментов.
Качество медицинской помощи – совокупность характеристик, отражающих своевременность оказания медицинской помощи, правильность выбора методов профилактики, диагностики, лечения и реабилитации при оказании медицинской помощи, степень достижения запланированного результата.
Клинические рекомендации – документ, основанный на доказанном клиническом опыте, описывающий действия врача по диагностике, лечению, реабилитации и профилактике заболеваний, помогающий ему принимать правильные клинические решения.
Лабораторная диагностика — совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Модель пациента - совокупность клинических, лабораторных и инструментальных диагностических признаков, позволяющих идентифицировать заболевание (отравление, травму, физиологическое состояние) и отнести его к группе состояний с общей этиологией и патогенезом, клиническими проявлениями, общими подходами к лечению и коррекции состояния;
Медицинский работник - физическое лицо, которое имеет медицинское или иное образование, работает в медицинской организации и в трудовые (должностные) обязанности которого входит осуществление медицинской деятельности, либо физическое лицо, которое является индивидуальным предпринимателем, непосредственно.
Нозологическая форма - совокупность клинических, лабораторных и инструментальных диагностических признаков, позволяющих идентифицировать заболевание (отравление, травму, физиологическое состояние) и отнести его к группе состояний с общей этиологией и патогенезом, клиническими проявлениями, общими.
Синдром - состояние, развивающееся как следствие заболевания и определяющееся совокупностью клинических, лабораторных, инструментальных диагностических признаков, позволяющих идентифицировать его и отнести к группе состояний с различной этиологией, но общим патогенезом, клиническими
Уровень достоверности доказательств – отражает степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным.
Уровень убедительности рекомендаций – отражает не только степень уверенности в достоверности эффекта вмешательства, но и степень уверенности в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации.
Формулярные статьи на лекарственные препараты - фрагмент протоколов лечения больных, содержащий сведения о применяемых при определенном заболевании (синдроме) лекарственных препаратах, схемах, и особенностях их назначения.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Грипп (Grippus, Influenza) — острая инфекционная болезнь с аэрозольным механизмом передачи возбудителя, характеризующаяся массовым распространением, кратковременной лихорадкой, интоксикацией и поражением респираторного тракта [1−5, 62].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Возбудителями гриппа являются РНК-содержащие вирусы, которые входят в семейство ортомиксовирусов (Оrthomyxoviridae). Семейство включает несколько родов, в том числе поражающие человека [1 – 3, 62]:
1. Род Influenzavirus A – вирусы гриппа типа A,
2. Род Influenzavirus B – вирусы гриппа типа B,
3. Род Influenza С – представлен вирусом гриппа типа С.
Основные поверхностные белки представлены:
o Гемагглютинином (НА) – ответственным за прикрепление и проникновение вируса в клетку, а также за "раздевание" вируса, то есть освобождение рибонуклеиновой кислоты. НА состоит из двух субъединиц НА1 и НА2. Изменения в сайте расщепления НА приводят к изменению инфекционной активности вируса. Гемагглютинин является основным иммуногеном и вызывает индукцию вирус-нейтрализующих, антигемагглютинирующих антител.
o Нейраминидазой (NА) – белком, ответственным за инвазию вируса в слизистые оболочки дыхательных путей и отделение почкующихся вирионов от клеточной стенки. Определенные изменения (мутации) в структуре белка приводят к формированию резистентности к селективным ингибиторам нейраминидазы.
В настоящее время на основе свойств гемагглютинина выделяют 18 подтипов вируса гриппа А (обозначаемые как Н1, Н2, …, Н18). Белок нейраминидазы имеет и 11 вариантов (N1, N2, …, N11) [7 – 12, 62]. Вирусы гриппа А широко распространены в природе среди разных видов птиц и млекопитающих. Характерной особенностью вирусов гриппа, особенно типа A, является изменчивость поверхностных гликопротеинов НА и NА.
Для вируса гриппа типа A возможны два вида изменчивости: дрейф – точечные мутации в вирусном геноме с соответствующими изменениями в гемагглютинине или нейраминидазе и шифт- реассортация РНК сегментов, что происходит, благодаря сегментированному строению РНК при одновременном заражении клетки разными субтипами вирусов гриппа [4,12, 23, 62].
Все известные пандемии гриппа были вызваны шифтовыми вариантами вируса гриппа А, имеющими антигенные формулы: A/H1N1, A/H2N2 и A/H3N2.
Заболевания, вызываемые вирусами гриппа типов B и C, встречаются только в популяции людей. Антигенная структура вирусов гриппа типа B изменяется только путем дрейфа [24 – 28]. Вирусы гриппа B не вызывают пандемии, но являются возбудителями крупных вспышек и эпидемий.
Вирус гриппа типа C, имеет только один поверхностный антиген (гликопротеин гемагглютинин-эстераза) [29, 30]. Грипп C не приводит к эпидемическим вспышкам, заболевания носят спорадический характер, но среди маленьких детей вирус гриппа C вызывает локальные вспышки. Наиболее тяжело инфекция протекает у детей младшего возраста.
Даже минимальные изменения в структуре нейраминидазы и/или гемагглютинина, приводят к возникновению заболевания, т.к. анамнестические антитела против новых вирусов не активны. Этой способностью к изменчивости определяется возникновение гриппозных эпидемий и пандемий.
Вирус гриппа избирательно поражает эпителиальные клетки респираторного тракта (преимущественно трахеи). Ведущее значение в патогенезе гриппа имеют эпителиотропные и токсические свойства вирусов гриппа, а также аллергизация макроорганизма антигенами возбудителя.
Соответствие клинических синдромов патогенетическим механизмам и морфологическому субстрату [48] представлено в Приложении А3.
Высокая патогенность вируса гриппа А может быть обусловлена и наличием мутаций, в частности в гене гемагглютинина H D222G, что приводит к увеличению сродства H вируса гриппа к альфа-(2-3)-сиалогалактазидам нижних отделов дыхательных путей и легких, расширению рецепторной специфичности, развитию поражения легких [43, 44, 49].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Источником инфекции является больной человек в остром периоде заболевания (первые 5 – 7 дней болезни), в том числе с легкой или бессимптомной формой, реже – реконвалесцент, выделяющий вирус, в среднем, в течение двух недель от начала заболевания.
Механизмы и пути передачи вируса гриппа:
1. Аэрогенный механизм реализуется воздушно-капельным и воздушно-пылевым путями передачи. Возбудитель вируса гриппа распространяется при разговоре, кашле, чихании. Максимальное его количество содержится в крупнокапельной фазе аэрозоля, выделяемого больным. Радиус рассеивания вируса составляет 2 – 3 м.
2. Контактно-бытовой механизм имеет значительно меньшее эпидемиологическое значение. Реализуется через предметы обихода, соски, игрушки, белье, посуду.
Длительность выживания возбудителей во внешней среде с сохранением вирулентных и патогенных свойств зависит от условий внешней среды: для вирусов гриппа она варьирует от нескольких часов до 7 – 12 дней.
Восприимчивость к вирусу гриппа всеобщая. В течение жизни человек многократно встречается с вирусами гриппа, что не исключает восприимчивость к появляющимся новым штаммам.
По интенсивности проявлений эпидемического процесса принято выделять следующие варианты: спорадическая заболеваемость, вспышки, эпидемии и пандемии.
Продолжительность эпидемий гриппа в крупных городах в среднем составляет 8 недель. При этом переболевает 4 – 8 % населения.
Пандемии вызываются, как правило, новыми шифтовыми вариантами вируса гриппа, к которым восприимчива подавляющая часть населения. Пандемический вирус имеет глобальное распространение и поражает 10 и более процентов населения и вызывает заболевания в очень тяжелой форме.
По данным Всемирной организации здравоохранения (ВОЗ), во всем мире ежегодные эпидемии гриппа приводят примерно к 3 – 5 млн. случаев тяжелых форм заболевания и к 250 – 500 тыс. случаев смерти.
Оценку влияния эпидемий гриппа на смертность населения принято проводить по показателю «дополнительной» смертности.
Показатель «дополнительной» смертности населения изменяется ежегодно в зависимости от особенностей прошедшей эпидемии [57, 58]. Этот показатель рекомендуется ВОЗ использовать в качестве оценочного показателя прошедшего эпидсезона гриппа в каждой стране [59, 60]. Среди всех классов заболеваний основное место в структуре «дополнительной» смертности от гриппа занимает класс болезней органов кровообращения (ишемическая болезнь сердца (ИБС), гипертоническая болезнь (ГБ), гнойный миокардит, перикардит, септический эндокардит), а затем класс болезней органов дыхания (внебольничная пневмония, хронический бронхит, эмфизема, хронические обструктивные болезни легких (ХОБЛ), бронхиальная астма). Среди других классов болезней можно отметить влияние эпидемий гриппа на повышение смертности от злокачественных новообразований (преимущественно в группе лиц старше 50 лет), энцефалитов и менингоэнцефалитов, сахарного диабета, болезни Паркинсона и иммунодефицитных заболеваний. Наиболее высокий показатель "дополнительной" смертности встречается у пациентов с сочетанной патологией: сердечно-сосудистыми заболеваниями и с заболеваниями легких (870 на 100 тыс. населения), сахарным диабетом и заболеваниями сердца (481 на 100 тыс. населения), против 2 на 100 тыс. населения среди здоровых взрослых без соматической патологии [58, 61].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
J09 – Грипп, вызванный выявленным вирусом зоонозного или пандемического гриппа
J10 – Грипп, вызванный идентифицированным вирусом сезонного гриппа
J11 – Грипп, вирус не идентифицирован
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
[1−5, 12, 13, 62]
По течению:
1. Типичное (манифестное);
2. Атипичное (бессимптомное, стертое).
По тяжести (Приложение А3):
1. Легкая степень тяжести;
2. Средняя степень тяжести;
3. Тяжелая степень тяжести;
4. Очень тяжелая степень тяжести (гипертоксическая).
По характеру течения:
1. Неосложненное;
2. Осложненное;
2.1 Специфические осложнения (вирус-ассоциированные)
2.2 Неспецифические осложнения:
2.2.1 Бактериальные осложнения
2.2.2. Обострение/декомпенсация хронических заболеваний.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
[1−5, 12, 13, 62]
Симптомы и признаки гриппа
Инкубационный период гриппа составляет от 1 до 4 дней, в среднем около 48 часов. В легких случаях многие симптомы похожи на симптомы простуды (например, боль в горле, ринорея); Также может возникнуть легкий конъюнктивит.
Типичный грипп у взрослых характеризуется внезапным появлением озноба, лихорадки, прострации, кашля и генерализованных болей (особенно в спине и ногах). Сильная головная боль, часто со светобоязнью и ретробульбарной болью. Вначале респираторные симптомы могут быть легкими, с перхотью в горле, жжением за грудиной, непродуктивным кашлем и иногда насморком. Позже заболевание нижних дыхательных путей становится преобладающим; кашель может быть стойким, хриплым и продуктивным.
Могут возникать желудочно-кишечные симптомы, которые, по-видимому, чаще встречаются у пандемического штамма H1N1 2009 года. У детей может быть выраженная тошнота, рвота или боль в животе, а у младенцев может быть синдром, подобный сепсису.
Через 2–3 дня острые симптомы быстро проходят, хотя лихорадка может длиться до 5 дней. Кашель, слабость, потливость и утомляемость могут сохраняться в течение нескольких дней, а иногда и недель.
При неосложненном гриппе характерны лейкопения с нейтропенией, а также относительный лимфоцитоз и моноцитоз. СОЭ у большинства больных нормальная. При рентгенологическом исследовании легких в остром периоде заболевания выявляют усиление сосудистого рисунка.
Группы высокого риска
Некоторые пациенты подвержены высокому риску осложнений от гриппа:
Дети < 5 лет; дети младше 2 лет подвергаются особенно высокому риску
Взрослые > 65 лет
Люди с хроническими заболеваниями (например, сердечно-легочными заболеваниями, сахарным диабетом, почечной или печеночной недостаточностью, гемоглобинопатиями, иммунодефицитом)
Женщины во 2 или 3 триместре беременности
Пациенты с расстройствами, нарушающими обработку респираторных секретов (например, когнитивная дисфункция, нервно-мышечные расстройства, инсульт, судорожные расстройства)
Пациенты ≤ 18 лет, принимающие аспирин (поскольку синдром Рея представляет собой риск)
Заболеваемость и смертность у этих пациентов могут быть связаны с обострением основного заболевания, острым респираторным дистресс-синдромом, первичной гриппозной пневмонией или вторичной бактериальной пневмонией.
Осложнения
Пневмония — одно из частых осложнений гриппа. Развившиеся на фоне вирусной инфекции пневмонии относят к первичным вирусно-бактериальным (чаще всего стрептококковой и стафилококковой этиологии). Они чаще развиваются у пациентов группы «высокого риска»: с хроническими заболеваниями легких и сердца, лиц пожилого возраста. Постгриппозные пневмонии развиваются в конце 1-й — начале 2-й недели болезни. Антибактериальное лечение дает хорошие результаты. Пневмонии могут иметь как интерстициальный, так и очаговый характер.
Тяжелое осложнение гриппа — ОНГМ. Для него характерны: сильная головная боль, рвота, судороги, оглушенность, потеря сознания, повышение АД, одышка, тахикардия, менингеальный синдром, застойные явления на глазном дне.
Частые осложнения гриппа — синуситы и отиты; реже — пиелонефрит и пиелоцистит. Возможны и другие осложнения: диэнцефальный синдром, менингоэнцефалит и астеновегетативный синдром. На тяжесть течения и исход болезни оказывают влияние сопутствующая хроническая патология и нейроэндокринные нарушения.
В период крупных эпидемий летальность не превышает 1–2%. Причиной смерти при тяжелой форме гриппа могут быть: отек мозга, геморрагический отек легких, острая сосудистая недостаточность.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза
Диагностика гриппа у взрослых производится на основании данных эпидемиологического и клинического анамнеза, клинического осмотра, лабораторных и специальных методов обследования и направлена на определение нозологии и клинической формы, тяжести состояния, выявление осложнений и показаний к терапии.
В период эпидемических подъемов заболеваемости гриппом окончательный диагноз «грипп» может быть установлен как на основании лабораторного подтверждения, так и на основании клинических и эпидемиологических данных[1].
[1] СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней». XXXIV. Профилактика гриппа и других острых респираторных вирусных инфекций (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
2.1 Жалобы и анамнез
Рекомендуется обратить внимание на наличие сроки появления повышенной температуры тела, интоксикации (слабость, снижение аппетита), жалоб на ломоту в мышцах и суставах, боль при движении глазных яблок, катаральные явления (насморк, боли в горле, кашель, царапающие боли за грудиной), боль в грудной клетке для определения тяжести и длительности заболевания [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Рекомендуется обратить внимание на сведения эпидемиологического анамнеза о пребывание в очаге ОРВИ в период, соответствующий инкубационному периоду гриппа, на наличие контакта с пациентом гриппоподобным заболеванием (ГПЗ) или с пациентом (умершим) с лабораторно подтвержденным диагнозом грипп в течение срока менее чем 7 дней до появления первых клинических признаков болезни; оценить степень контакта с учетом состоявшегося механизма и пути передачи инфекции[1] [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Рекомендовано обратить внимание на наличие эпидемического подъема заболеваемости гриппом для клинической диагностики заболевания [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Рекомендуется обратить внимание на наличие вакцинопрофилактики гриппа у пациента для выявления риска тяжелого и осложненного течения заболевания [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Рекомендуется обратить внимание на прием противовирусных препаратов для системного применения до обращения за медицинской помощью для решения вопроса о необходимости коррекции терапии [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Рекомендуется обратить внимание на наличие сопутствующих хронических заболеваний или иных состояний (беременность) для выявления факторов риска развития тяжелого и осложненного течения заболевания [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
[1] Методические рекомендации N 01/7161–9–34 «Организация и проведение лабораторной диагностики заболеваний, вызванных высокопатогенными штаммами вируса гриппа А (H1N1), у людей» (утв. Главным государственным санитарным врачом Российской Федерации 24.05.2009) (Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 25 мая 2009 г. N 01/7170-9-32)
2.2 Физикальное обследование
Рекомендовано начать с общего осмотра с оценкой состояние кожных покровов и видимых слизистых оболочек: цвет (гиперемия, бледность, цианоз), влажность, отечность, инъекция сосудов склер; обращают внимание на наличие и характер одышки, мокроты, дистанционных хрипов, положение и поведение пациента для диагностики степени тяжести и характера течения заболевания [3, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Рекомендовано оценить жизненно-важные показатели – частоту дыхательных движений (ЧДД), артериальное давление (АД), частоту сердечных сокращений (ЧСС), выполнить термометрию для определения степени тяжести заболевания, наличия осложнений и сопутствующих заболеваний [3, 35, 40, 42, 46, 50−52, 62−65].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
2.3 Лабораторные диагностические исследования
2.3.1. Неспецифическая лабораторная диагностика
Рекомендовано выполнение общего (клинического) анализа крови с определением уровня эритроцитов, гематокрита, лейкоцитов, тромбоцитов, лейкоцитарной формулы для диагностики, комплексной оценки степени тяжести болезни, своевременного выявления осложнений и неотложных состояний всем пациентам с подозрением на грипп [50−52, 62, 63, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: при неосложненном течении гриппа характерны нормоцитоз или лейкопения, нейтропения, эозинопения, относительный лимфо- и моноцитоз. При бактериальных осложнениях (пневмония, синусит и т.д.) в крови нарастает лейкоцитоз, палочкоядерный нейтрофилез, увеличивается скорость оседания эритроцитов (СОЭ). При интерстициальном вирусном поражении легких характерны лейкопения, нейтрофилез с палочкоядерным сдвигом, анемия и тромбоцитопения.
Рекомендовано выполнение общего (клинического) анализа мочи для выявления наличия почечной дисфункции, декомпенсации сопутствующих заболеваний всем пациентам с подозрением на грипп [50−52, 62, 63, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: при неосложненном течении гриппа патологических изменений нет; при выраженной лихорадке, интоксикационном синдроме – увеличение плотности мочи, невыраженные лейкоцитурия, протеинурия, цилиндрурия, носящие транзиторный характер, исчезают при нормализации температуры тела и купировании проявлений общей инфекционной интоксикации.
2.3.2. Специфическая лабораторная диагностика
Лабораторное обследование в целях идентификации возбудителя гриппа проводится в обязательном порядке при [1]:
− госпитализации больного по поводу ОРВИ верхних и нижних дыхательных путей (тяжелые и необычные формы заболевания);
− заболевании лиц с высоким риском неблагоприятного исхода гриппа и ОРВИ (в том числе беременных, лиц с хроническими заболеваниями сердца, легких, метаболическим синдромом и других);
− регистрации очагов ОРВИ с множественными случаями заболеваний в организованных коллективах взрослых с числом пострадавших 5 и более человек в один инкубационный период, заболевании лиц из организаций с круглосуточным пребыванием.
Рекомендуется вышеперечисленным группам пациентов с подозрением на грипп произвести забор клинического материала для [2] [50−52, 62, 63, 66–82]:
- Молекулярно-биологического исследования мазков со слизистой оболочки носоглотки и ротоглотки на вирус гриппа (Influenza virus)
- Молекулярно-биологического исследования бронхоальвеолярной лаважной жидкости, мокроты (индуцированной мокроты, фаринго-трахеальных аспиратов) на вирус гриппа (Influenza virus)
- Иммунохроматографического экспресс-исследования носоглоточного мазка, эндотрахеального аспирата, бронхоальвеолярной лаважной жидкости на вирусы гриппа A и B.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: оптимальный срок сбора клинического материала – в течение 3 суток после манифестации болезни1 или в первый день госпитализации (в более поздние сроки не исключена возможность суперинфекции при контакте с другими пациентами в стационаре), предпочтительно до начала противовирусной терапии. От одного больного забирается не менее трех видов клинического материала, обязательно -мазки из полости носа и ротоглотки, и носоглоточное отделяемое1. От одного больного отбирают две пробы: одну пробу для проведения первичного исследования материала методами ПЦР, вторую – для проведения вирусологического исследования. Все виды работ проводят с соблюдением противоэпидемического режима, в строгом соответствии с требованиями действующих нормативно-методических документов.
Правила забора материала для исследований представлены в Приложении А3
Рекомендовано иммунохроматографическое экспресс-исследование носоглоточного мазка на вирус гриппа А и B (обнаружение антигенов вируса гриппа) для ранней диагностики и скрининга гриппа на амбулаторном и стационарном этапах оказания помощи пациентам по клинико-эпидемиологическим показаниям и пациентам из групп риска с целью своевременного назначения этиотропной терапии [81, 83, 84, 199-204].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Комментарии: для обнаружения антигенов вирусов гриппа А и В используется также метод ИФА. Тесты на основе иммунофлуоресценции (РИФ, ПИФ, РПИФ и др.) применяют для обнаружения в мазках из респираторного тракта антигенов вирусов, находящихся внутри клеток слизистой оболочки. Тесты используются только в эпидемиологических целях для массового скрининга, поскольку их аналитические характеристики могут варьировать в широких пределах, давать ложноотрицательные результаты (недостаточная чувствительность по сравнению с культуральными методами и ПЦР), и давать ложноположительные результаты в межэпидемический период (в силу недостаточной специфичности и субъективности интерпретации анализа)[1],[2]
Рекомендовано лицам с симптомами ОРВИ проведение молекулярно-биологического исследования мазков со слизистой оболочки носоглотки и ротоглотки на вирусы гриппа А, В (Influenza virus А, В) с целью своевременного назначения этиотропной терапии [50−52, 62, 63, 74–82].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: ПЦР наиболее эффективный метод, который позволяет обнаружить нуклеиновые кислоты вируса в среднем до 7 дней, и максимум – до 2 недель от начала заболевания (при условии сохранении признаков поражения верхних дыхательных путей). Результаты получают в течение 4–6 часов после представления образца.
Рекомендовано всем лицам с симптомами ОРВИ проведение молекулярно-биологического исследования мазков со слизистой оболочки носоглотки и ротоглотки или иммунохроматографическое экспресс-исследование носоглоточного мазка на коронавирус SARS-CoV-2 для проведения дифференциальной диагностики [250].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендовано пациентам с симптомами ОРВИ молекулярно-биологическое исследование мазков со слизистой оболочки носо – и ротоглотки на вирус парагриппа (Human Parainfluenza virus), риновирусы (Human Rhinovirus), аденовирус (Human Adenovirus), респираторно-синцитиальный вирус (Human Respiratory Syncytial virus), коронавирусы 229E, OC43, NL63, HKUI (Human Coronavirus), бокавирус (Human Bocavirus), метапневмовирус (Human Metapneumo virus) на амбулаторном этапе по клинико-эпидемиологическим показаниям ( тяжелое течение, эпидемический очаг, пожилой возраст, угроза развития ОРДС) , в стационаре - всем заболевшим для проведения дифференциальной диагностики [50−52, 62, 63, 83, 84].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: ПЦР наиболее эффективный метод, который позволяет обнаружить нуклеиновые кислоты вируса в среднем до 7 дней, и максимум – до 2 недель от начала заболевания (при условии сохранении признаков поражения верхних дыхательных путей). Результаты получают в течение 4–6 часов после представления образца.
Рекомендовано произвести исследование на антитела к вирусу гриппа в стандартных серологических тестах парных сывороток крови пациента (при условии соблюдения сроков сбора сывороток крови: первая – в день постановки диагноза, вторая – через 2 – 3 недели) на стационарном этапе оказания помощи при невозможности проведения молекулярно-генетического исследования для ретроспективной диагностики2 [50−52, 62, 63, 83, 84].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: выявление специфических антител в сыворотках крови выполняют с использованием РТГА, ИФА и РСК. Достоверность результата увеличивается в случае выявления 4-кратного и более нарастания титра специфических антител в парных сыворотках с соблюдением сроков исследования. Обнаружение антител к вирусам гриппа методом ИФА уступает по чувствительности и специфичности РТГА.
Рекомендовано пациентам с поражением нижних дыхательных путей обследование и лечение, согласно утвержденным клиническим рекомендациям: Внебольничная пневмония у взрослых [251].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
2.3.3. Специальная лабораторная диагностика
Рекомендовано выполнение анализа крови биохимического общетерапевтического (исследование уровня общего билирубина, альбумин, мочевины, креатинина, глюкозы, определение активности аспартатаминотрансферазы, аланинаминотрансферазы, исследование уровня тропонинов I, T в крови ) у пациентов с тяжелым и осложненным течением гриппа для выявления наличия органной дисфункции, декомпенсации сопутствующих заболеваний и развитие осложнений [50−52, 62, 63, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: биохимический анализ крови не дает какой-либо специфической информации, но обнаруживаемые отклонения имеют определенное прогностическое значение, оказывают влияние на выбор лекарственных средств и/или режим их дозирования.
Рекомендовано исследование кислотно-основного состояния и газов крови: парциальное давление кислорода (PO2), углекислого газа (PCO2), рН, содержание кислорода (O2CT), насыщение кислородом (SaO2), концентрация HCO3 у пациентов с дыхательной недостаточностью для комплексной оценки степени тяжести болезни, диагностики осложнений, неотложных состояний и обострения хронических заболеваний [50−52, 62, 63, 66, 67, 68, 71, 85, 86].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: при неосложненном течении гриппа патологических изменений нет.
Рекомендовано проведение коагулограммы (ориентировочное исследование системы гемостаза): активированное парциальное тромбопластиновое время (АПТВ), протромбиновое время по Квику, тромбиновое время и/или фибриноген пациентам с проявлениями геморрагического синдрома для комплексной оценки степени тяжести болезни и назначения терапии [50−52, 62, 63, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: при неосложненном течении гриппа патологических изменений нет.
Рекомендовано исследование электролитного состава крови (натрий, калий, кальций, магний, неорганический фосфор, хлориды) у пациентов с тяжелым и осложненным течением гриппа для комплексной оценки степени тяжести болезни, диагностики осложнений, неотложных состояний и обострения хронических заболеваний [50, 52, 62, 63, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: при неосложненном течении гриппа патологических изменений нет.
Рекомендовано исследование маркеров воспалительной реакции (фибриногена, протромбина, С–реактивного белка, прокальцитонина) пациентам с тяжелым и осложненным течением гриппа для оценки тяжести течения и прогноза заболевания [50–52, 62, 63, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: при неосложненном течении гриппа патологических изменений нет. Уровень СРБ коррелирует с тяжестью течения, распространенностью воспалительной инфильтрации и прогнозом при пневмонии.
[1] СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней». XXXIV. Профилактика гриппа и других острых респираторных вирусных инфекций (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
[2] Методические рекомендации N 01/7161–9–34 «Организация и проведение лабораторной диагностики заболеваний, вызванных высокопатогенными штаммами вируса гриппа А (H1N1), у людей» (утв. Главным государственным санитарным врачом Российской Федерации 24.05.2009) (Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 25 мая 2009 г. N 01/7170-9-32)
2.4 Инструментальные диагностические исследования
Рекомендуется выполнение пульсоксиметрии с измерением SpO2 всем пациентам с подозрением на ГПЗ на всех этапах оказания медицинской помощи для ранней диагностики респираторных нарушений [50−52, 62, 63, 85, 86, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: пульсоксиметрия является простым и надежным скрининговым методом, позволяющим выявлять пациентов с гипоксемией, нуждающихся в респираторной поддержке и оценивать ее эффективность. Пациентам с признаками острой дыхательной недостаточности (ОДН) (SрO2 менее 90%) рекомендуется исследование газов артериальной крови с определением PaO2, PaCO2, pH, бикарбонатов, лактата.
Рекомендовано регистрация электрокардиограммы (ЭКГ) в стандартных отведениях пациентам при осложненном течении заболевания при наличии аускультативных изменений в сердце для уточнения нарушения функции проведения и трофики ткани сердца [50−52, 62, 63, 85, 86, 66, 67, 68, 71].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: данное исследование не несет в себе какой-либо специфической информации, однако в настоящее время известно, что вирусная инфекция и пневмония помимо декомпенсации хронических сопутствующих заболеваний увеличивают риск развития нарушений ритма и острого коронарного синдрома, своевременное выявление которых значимо влияет на прогноз. Кроме того, определенные изменения на ЭКГ (например, удлинение интервала QT) требуют внимания при оценке кардиотоксичности ряда назначаемых лекарственных препаратов. Для токсикоза характерны изменения: снижение и зазубренность зубца Р, снижение зубца Т в разных отведениях, относительное удлинение интервала Q-Т, удлинение интервала Р –Q. Изменения нестойкие и проходят в течение 1 2 недель.
Рекомендовано выполнение прицельной рентгенографии органов грудной клетки клетки пациентам с явлениями бронхита (для исключения очаговой пневмонии) и наличии физикальных признаков поражения легочной ткани (верификация пневмонии) [50–52, 62, 63, 85–87, 89].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий: может быть выявлено усиление легочного рисунка, уплотнение бронхов. Рентгенологические признаки пневмонии зависят от типа возбудителя пневмонии.
Рекомендовано выполнение рентгенографии придаточных пазух носа пациентам с катаральными проявлениями в острый период гриппа или их появлением на фоне проводимой терапии, при подозрении на синусит, вызванный присоединением бактериальной флоры [50−52, 62, 63, 88, 89].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано выполнение спинномозговой пункции пациентам с наличием менингеальных симптомов с последующим микроскопическим исследованием СМЖ, подсчетом клеток в счетной камере (определение цитоза) для дифференциальной диагностики явлений менингизма и наличия менингита [50−52, 62, 63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: при менингизме патологических изменений ликвора не обнаруживается. Необходимо помнить, что вирусы гриппа не обладают тропизмом к нервной ткани, менингеальная и даже энцефалитическая симптоматика носит дисциркуляторный и гипоксический генез, а все патологические изменения ликвора при гриппе или после него носят вторичный характер, например, при аутоиммунных поражениях нервной ткани (менингит, менингоэнцефалит, полирадикулонейропатия, синдром Гийена-Барре.
2.5 Иные диагностические исследования
Рекомендовано консультация смежных специалистов пациентам в случаях подозрения на осложнения: врача-невролога (при явлениях менингоэнцефалита), врача-пульмонолога (при наличии признаков пневмонии), врача-гематолога (при выраженных гематологических изменениях и геморрагическом синдроме), врача-кардиолога (при присоединении симптомов миокардита, острой сердечно-сосудистой недостаточности), врача-акушера-гинеколога (при развитии гриппа на фоне беременности) для определения дальнейшей тактики ведения [50−52, 62, 63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендуется консультация врача анестезиолога-реаниматолога пациентам с наличием быстропрогрессирующей ОДН (ЧД >25 в 1 мин, SpO2 <92%, а также другой органной недостаточностью (2 и более балла по шкале SOFA) для перевода в отделение реанимации и интенсивной терапии (ОРИТ) [50−52, 62, 63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
2.5.1. Дифференциальная диагностика [1−4, 8–10, 28, 36–39].
Дифференциальную диагностику при гриппе проводят с двумя группами инфекционных заболеваний: протекающими с катарально-респираторным синдромом и характеризующимися ранним развитием лихорадочно-интоксикационного синдрома.
Дифференциальная диагностика гриппа с другими ОРВИ негриппозной этиологии, с острыми респираторными заболеваниями (ОРЗ)представлена в Приложении А3.
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Сроки начала лечения больных с предполагаемым или вероятным случаями гриппа не зависят от отсутствия или задержки получения результата диагностического тестирования на грипп[1].
На выбор тактики лечения оказывают влияние следующие факторы [50–52, 62, 63, 85, 86]: возраст пациента; характер сопутствующих заболеваний; клиническая форма болезни; характер течения болезни (динамики нарастания симптомов); тяжесть заболевания; наличие и характер осложнений.
Информация, касающаяся доз, показаний к применению и способов применения лекарственных средств, содержащаяся в данных рекомендациях, может отличаться от информации, указанной в ИМП. Для получения полной информации о применении того или иного ЛС следует ознакомиться с ИМП. Персональная ответственность за интерпретацию и использование настоящих рекомендаций лежит на лечащем враче.
Диагностическое тестирование на грипп ни в коем случае не должно задерживать начало лечения противовирусными препаратами для системного применения и выполнения процедур по борьбе с инфекцией.
3.1. Консервативное лечение
Рекомендуется начать лечение противовирусными препаратами прямого действия не позднее 48 часов (занамивир – в первые 36 часов) после манифестации болезни всем пациентам с симптомами гриппа для прекращения репликации вируса [87, 88, 90, 91, 92, 95].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: лечение необходимо начинать немедленно, не дожидаясь лабораторного подтверждения диагноза, независимо от сведений о вакцинации против гриппа и степени тяжести болезни. Наилучший лечебный эффект достигается в случаях начала применения противовирусных препаратов прямого действия в первые 12 часов от начала болезни. При отсутствии лечения в ранние сроки прием противовирусных препаратов прямого действия может быть начат на любом этапе разгара болезни, когда предполагается или документально подтверждена возможность текущей репликации вируса гриппа.
Не рекомендуются для лечения гриппа производные адамантана и циклические амины (амантадин**, римантадин) [90, 93, 97, 98, 101].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: вследствие резистентности к данным препаратам большинства штаммов вируса гриппа.
3.1.1. Лечение легких и средне-тяжелых неосложненных форм гриппа в амбулаторных условиях
Рекомендуется использование противовирусных препаратов прямого действия всем пациентам с симптомами гриппа для прекращения репликации вируса:
o Осельтамивир** [[1], 52, 61, 90-115, 117].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарии: является селективным ингибитором нейраминидазы вирусов гриппа А и В. Входит в международные клинические рекомендации по лечению и профилактике гриппа. Пациентам, которые не относятся к группе повышенного риска развития тяжелого и/или осложненного течения гриппа и у которых имеет место лабораторно подтвержденный грипп или с большой вероятностью подозрительный случай гриппа, протекающий без осложнений, не следует назначать препараты из группы селективных ингибиторов нейраминидазы. Осельтамивир** назначают внутрь по 75 мг 2 раза в сутки в течение 5 дней.
o Занамивир [1, 52, 61, 90, 91, 95, 96, 100, 105, 107–109, 111−124].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
Комментарии: является селективным ингибитором нейраминидазы вирусов гриппа А и В. Входит в международные клинические рекомендации по лечению и профилактике гриппа. Пациентам, которые не относятся к группе повышенного риска развития тяжелого и/или осложненного течения гриппа и у которых имеет место лабораторно подтвержденный грипп или с большой вероятностью подозрительный случай гриппа, протекающий без осложнений, не следует назначать препараты из группы селективных ингибиторов нейраминидазы. Занамивир рекомендуется в случаях резистентности вируса A(H1N1) к осельтамивиру**, при отсутствии препарата, беременным и пациентам с тяжелой почечной недостаточностью. Назначают по 2 ингаляции (по 5 мг каждая) 2 раза в сутки в течение 5 дней. Резистентности к занамивиру не зарегистрировано. Занамивир в форме порошка для ингаляций не следует применять распылением с помощью аэрозольного ингалятора из-за присутствия лактозы, которая может поставить под угрозу дыхательную функцию. Развитие бронхоспазма и/или ухудшение функции дыхания возможно у пациентов без предшествующих заболеваний в анамнезе.
o Балоксавир марбоксил [125-129]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: балоксавир марбоксил представляет собой пролекарство, которое в процессе гидролиза преобразуется в активный метаболит балоксавир марбоксил, обладающий действием в отношении вируса гриппа. Балоксавир марбоксил воздействует на кэп-зависимую эндонуклеазу (CEN) – специфичный для вируса гриппа фермент в полимеразной кислой субъединице комплекса вирусной РНК-полимеразы. Тем самым балоксавир марбоксил ингибирует транскрипцию генома вируса гриппа, приводя к подавлению вирусной репликации и прекращению выделения вируса в течение 1 суток после приема у больных без факторов риска, обладает активностью в отношении штаммов, резистентных к ингибитору нейраминидазы, включая следующие мутации: H274Y для вируса подтипа A/H1N1; E119V и R292K для вируса подтипа A/H3N2; R152K и D198E для вируса типа B; H274Y для вируса подтипа A/H5N1 и R292K для вируса подтипа A/H7N9.
Балоксавир марбоксил может быть назначен взрослым и детям старше 12 лет, как не имеющих дополнительных заболеваний, так и подверженных риску развития осложнений гриппа. Препарат применяется внутрь однократно, вне зависимости от приема пищи. При массе тела пациента от 40 кг до 80 кг – 40 мг, ≥80 кг – 80 мг.
o Умифеновир** [52, 131–135, 140-144].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
Комментарии: умифеновир** специфически подавляет in vitro вирусы гриппа А и В (Influenza virus A, B), включая высокопатогенные подтипы A(H1N1)pdm09 и A(H5N1), а также другие вирусы – возбудители острых респираторных вирусных инфекций (ОРВИ) (коронавирус (Сoronavirus), ассоциированный с тяжелым острым респираторным синдромом (ТОРС), риновирус (Rhinovirus), аденовирус (Adenovirus), респираторно-синцитиальный вирус (Pneumovirus) и вирус парагриппа (Paramyxovirus)). В исследованиях in vitro специфически подавляет вирус SARS-CoV-2, вызывающий новую коронавирусную инфекцию (COVID-19). Рекомендован к применению Международным профессиональным сообществом по изучению гриппа и других респираторных вирусных заболеваний. Противопоказан при повышенной чувствительности к любому компоненту препарата, в первом триместре беременности.
Назначают внутрь до приема пищи по 200 мг 4 раза в сутки в течение 5 дней.
o Риамиловир [145-159].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
Комментарии: риамиловир («предложенное МНН»; до решения осенней 65-ой сессии Консультативной группы экспертов ВОЗ по Международной фармакопее и фармацевтическим препаратам 17-20.10.2017 под наименованием действующего вещества – метилтионитрооксодигидротриазолотриазинид натрия) обладает широким спектром противовирусной активности в отношении РНК-содержащих вирусов, в том числе вирусов гриппа А и В, включая высокопатогенные подтипы A(H1N1)pdm09 и A(H5N1), благодаря подавлению синтеза вирусных РНК и репликации геномных фрагментов. Активное вещество является синтетическим аналогом оснований пуриновых нуклеозидов (гуанина). Не входит в перечень ЛС, рекомендуемых международными клиническими рекомендациями по лечению и профилактике гриппа. Показан в составе комплексной терапии гриппа и других острых респираторных вирусных инфекций у взрослых пациентов. Лечение необходимо начать не позднее 2-го дня от появления клинических симптомов болезни: внутрь независимо от приема пищи по 1 капсуле (250 мг) 3 раза в день (суточная доза – 750 мг) в течение 5 дней. Противопоказан при повышенной чувствительности к компонентам препарата; беременности, в период грудного вскармливания. У пациентов в возрасте до 18 лет и при почечной/печеночной недостаточности эффективность и безопасность не определены.
o Энисамия йодид [136−138].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
Комментарий: рекомендованная схема назначения препарата по 500 мг 3 раза в сутки перорально, курс 5–7 дней. Противопоказан при повышенной чувствительности к компонентам препарата, дефиците лактазы, непереносимости лактозы, глюкозно-галактозной мальабсорбции, дефиците сахаразы/изомальтазы, непереносимости фруктозы, беременности и периоде грудного вскармливания, аллергических реакциях в анамнезе, тяжёлых органических поражениях печени и почек [136−138].
Рекомендовано использование препаратов с широким противовирусным действием пациентам с симптомами гриппа при наличии легкой и среднетяжелой формы иммунодефицитов c иммуномодулирующей и противовирусной целью
o Имидазолилэтанамид пентандиовой кислоты** [52, 160–168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: механизм действия имидазолилэтанамид пентандиовой кислоты** реализуется на уровне инфицированных клеток за счет стимуляции факторов врожденного иммунитета, подавляемых вирусными белками. Вызывает повышение уровня интерферона в крови до физиологической нормы, обладает противовоспалительной активностью. Прием препарата начинают с момента появления первых симптомов заболевания, желательно не позднее 2 суток от начала болезни, внутрь независимо от приема пищи по 1 капсуле (90 мг) 1 раз в сутки в течение 5-7 дней. Противопоказан при повышенной чувствительности к любому компоненту препарата, дефиците лактазы, непереносимости лактозы, глюкозо-галактозной мальабсорбции, беременности и в период грудного вскармливания.
o Интерферон альфа-2b или интерферон гамма человеческий рекомбинантный** [52, 169–173, 187-196, 286-289].
Для интерферона гамма человеческого рекомбинантного**: Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Для интерферона альфа-2b: Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: Интерферон альфа 2b и интерферон гамма человеческий рекомбинантный**, вводимые интраназально, обладают опосредованным противовирусным действием на вирусы гриппа. Используются в схемах комплексной терапии гриппа при первых признаках заболевания. Не входят в перечень ЛС, рекомендуемых международными клиническими рекомендациями по лечению и профилактике гриппа. При интраназальном применении концентрация действующего вещества, достигаемая в крови, не имеет клинической значимости. Интерферон альфа 2b назначают интраназально по 3 капли/дозы в каждый носовой ход 5 – 6 раз в день (разовая доза – 3000 ME, суточная доза – 15000 – 18000 ME) в течение 5 дней; интерферон гамма человеческий рекомбинантный** назначают интраназально по 2 капли в каждый носовой ход 5 раз в день (разовая доза – 4000 ME, суточная доза – 20000 ME) до 3 дня от начала болезни или в течение 5 – 7 дней в период реконвалесценции
o Кагоцел** [52, 174–176].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: обладает опосредованным противовирусным действием на вирусы гриппа (индуктор интерферона). Не входит в перечень ЛС, рекомендуемых международными клиническими рекомендациями по лечению и профилактике гриппа. Применяется перорально по 24 мг (2 таблетки) 3 раза в сутки в первые 2 дня, затем по 12 мг (1 таблетка) 3 раза в сутки в течение 2 дней (курсовая доза 216 мг, 18 таблеток). Противопоказан при гиперчувствительности к компонентам препарата, беременности, в периоде лактации, дефиците лактазы, непереносимости лактозы, глюкозо-галактозной мальабсорбции.
o Тилорон** [177-186].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: обладает иммуномодулирующим и противовирусным эффектом. Индуктор интерферонов. Стимулирует образование в организме интерферонов всех типов (альфа, бета, гамма и лямбда), усиливает антителообразование, уменьшает степень иммунодепрессии, восстанавливает соотношения T-супрессоров и T-хелперов. Не входит в перечень ЛС, рекомендуемых международными клиническими рекомендациями по лечению и профилактике гриппа. Применяется перорально по 125 мг 1 раз в сутки в первые 2 дня, затем по 125 мг в сутки через день (курсовая доза 750 мг). Противопоказан при гиперчувствительности к компонентам препарата, беременности, в периоде лактации, детском возрасте до 18 лет
o Меглюмина акридонацетат [234-243].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
Комментарии: низкомолекулярный индуктор интерферона. Обладает прямым противовирусным действием, подавляя репродукцию вируса на ранних сроках (1–5-е сутки) инфекционного процесса, снижая инфекционность вирусного потомства, приводя к образованию дефектных вирусных частиц. Повышает неспецифическую резистентность организма в отношении вирусных и бактериальных инфекций.
Внутрь один раз в сутки за 30 минут до еды, не разжёвывая, запивая ½ стакана воды, взрослым и детям старше 12 лет: по 450–600 мг (3–4 таблетки) на приём, препарат принимают на 1, 2, 4, 6, 8-е сутки (курс лечения – 20 таблеток). Лечение необходимо начинать при первых симптомах заболевания. При тяжёлом течении гриппа в первый день принимают шесть таблеток.
o Азоксимера бромид** [259-264, 266, 267-269].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: обладает выраженной иммуномодулирующей (в том числе интерферонпродуцирующей) активностью, оказывает неспецифическое защитное действие в отношении широкого спектра патогенов, основанное на регуляции иммунитета макроорганизма. Кроме того, препарат имеет антитоксическое и антиоксидантное свойства. В острый период болезни препарат применяется в комплексе с этиотропной терапией, а в период реабилитации или с целью иммунопрофилактики респираторных инфекций — в качестве монотерапии.
Таблетки: по 1 таблетке сублингвально 2 раза в день 7 дней;
Раствор: по 6 мг ежедневно парентерально в течение 3-х дней, далее через день общим курсом 10 инъекций или интраназально или сублингвально 6 мг в сутки, суточная доза препарата (6 мг) вводится за 2-3 приема в сутки.
При отсутствии эффекта от приема интерферонов и иммуностимуляторов в течение 24 часов рекомендовано применение препаратов прямого противовирусного действия для прекращения репликации вируса[1], [52, 61, 90, 91, 95–117, 131-135, 139-143].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Рекомендуется проведение пероральной дезинтоксикационной терапии в объеме 2–3 литров жидкости в сутки (некрепко заваренного чая с молоком, медом, вареньем, а также отвара шиповника, свежеприготовленных фруктовых и ягодных соков, компотов, щелочных минеральных вод) всем пациентам с гриппом для купирования синдрома интоксикации [52, 62].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано назначение нестероидных противовоспалительных и противоревматических препаратов или анилидов пациентам с гипертермией выше 38 С, мышечными и суставными болями с жаропонижающей, болеутоляющей и противовоспалительной целью [52, 62, 193, 252]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: ибупрофен** перорально по 200–400 мг 3–4 раза в сутки в течение 3–10 дней (максимальная суточная доза — 1200 мг), парацетамол** перорально по 1–2 табл. (500–1000 мг) до 4 раз в сутки (максимальная суточная — 4000 мг.)
Рекомендовано назначение парацетамола в комбинации с другими препаратами, кроме психолептиков, пациентам с выраженными лихорадочно-интоксикационным и респираторным синдромами с анальгезирующей, жаропонижающей, противоаллергической, антиконгестивной целью :
Парацетамол+Фенилэфрин+Фенирамин [252-258].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 2)
Комментарии: Внутрь. Содержимое 1 пакетика растворяют в 1 стакане кипяченой горячей воды. Принимают в горячем виде. Можно добавить сахар по вкусу. Повторную дозу можно принимать через каждые 4 ч (не более 3 доз в течение 24 ч).
Не рекомендуется назначение салициловой кислоты и ее производных пациентам с гипертермией с жаропонижающей целью, вследствие возможных побочных явлений в виде нарушения гемостаза и обострения язвенной болезни желудка и 12-ти перстной кишки [52, 62, 92, 193].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано пациентам с острым бронхитом, обусловленным вирусом гриппа сопровождающихся бронхообструкцией и влажным кашлем назначение отхаркивающих препаратов, кроме комбинаций с противокашлевыми средствами для разжижения и улучшения отхождения мокроты [52, 62, 258, 264-266].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Ацетилцистеин** – по 1 таблетке по 200 мг – 2-3 раза в день, перорально, курс до 5 дней; Бромгексин – внутрь по 8 мг 3 (1–2 таблетки) 3–4 раза в сутки; Амброксол** – внутрь 30 мг, 90 мг/сут, курс до 5 дней; [110]. Бромгексин + Гвайфенезин + Сальбутамол – таблетки (2 мг сальбутамола сульфата + 8 мг бромгексина гидрохлорида + 100 мг гвайфенезина в 1 таблетке) внутрь по 1 таблетке 3 р./сут в течение 5.
Рекомендуется назначение симпатомиметиков и прочих противокашлевых препаратов при лечении гриппа у пациентов с сухим непродуктивным надсадным кашлем, значительно ухудшающим качество жизни [52, 62, 256, 258, 260, 270-273].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Препаратами выбора являются противокашлевые препараты в комбинации с отхаркивающими препаратами, в состав которых состав которых входит активное вещество декстрометорфан:
- R05DB Другие противокашлевые препараты Бутамират – внутрь по 15 мл 4 раза в сутки (сироп)
- R05FB Другие противокашлевые средства в комбинации с отхаркивающими средствами Декстрометорфан+Терпингидрат+[Левоментол]– внутрь по 1 чайной ложке (5 мл) 3-4 раза в день.
- R01BA Симпатомиметики Декстрометорфан+Парацетамол+Псевдоэфедрин+[Аскорбиновая кислота] – по одной таблетке 4 раза в день
- R05X Другие препараты для лечения простудных заболеваний
Декстрометорфан+Фенилэфрин+Хлорфенамин 5 – 7,5 мл сиропа 3-4 раза в сутки.
Не рекомендовано одновременное применение отхаркивающих и противокашлевых средств пациентам с кашлем, что может способствовать застою мокроты за счет подавления кашлевого рефлекса [52, 62, 256-258].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендуется местное применение адреномиметиков пациентам с выраженным затруднением носового дыхания в комплексной терапии ринита, риносинусита для облегчения заложенности носа и восстановления проходимости слуховой трубы не более 5 дней [52, 62, 195, 196].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Нафазолин – интраназально (в каждый носовой ход) по 1–3 капли 0,05–0,1% раствора 3–4 раза в сутки;
o Ксилометазолин** – интраназально (в каждый носовой ход), по 2–3 капли 0,1% раствора или одно впрыскивание из распылителя в каждую ноздрю 4 раза в день;
o Оксиметазолин – интраназально (в каждый носовой ход), по 1–2 капли 0,025–0,05% раствора 2–3 раза в сутки или по 2–3 впрыскивания 0,05% спрея.
3.1.2. Лечение осложненных среднетяжелых, тяжелых и крайне тяжелых форм гриппа в стационарных условиях
Рекомендована комплексная оценка клинических проявлений гриппа при госпитализации пациента в процессе его первичного обследования в условиях приёмного отделения стационара [50−52, 62, 85, 86, 90].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: При поступлении пациента в стационар:
o рекомендовано оценить характер поражения органов дыхания;
o рекомендовано определить степень компенсации сопутствующих болезней;
o рекомендовано измерить основные физиологические константы (ЧДД, ЧСС, АД, SаO2, диурез);
o рекомендовано провести рентгенографию (или широкоформатная флюорография) легких;
o рекомендовано проведение ЭКГ;
o рекомендовано взятие материала для специфической диагностики (ПЦР, серологические реакции).
Рекомендована госпитализация или перевод пациента в ОРИТ при наличии показаний [50–52, 62, 85, 86, 90].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: показания для перевода в отделение реанимации при установленном диагнозе гриппа представлены в Приложении А3.
Рекомендовано незамедлительно после поступления в стационар пациентам с симптомами гриппа начать лечение осельтамивиром** или занамивиром, как высокоэффективными селективными ингибиторами нейраминидазы вирусов гриппа типа А и В для прекращения репликации вируса [52, 61, 62, 90-124, 274].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарии: осельтамивир** назначают внутрь по 75 мг 2 раза в сутки в течение 5 дней. Занамивир рекомендуется в случаях резистентности вируса A(H1N1) к осельтамивиру**, при отсутствии препарата, беременным и пациентам с тяжелой почечной недостаточностью. Назначают по 2 ингаляции (по 5 мг каждая) 2 раза в сутки в течение 5 дней. У пациентов с тяжелым или прогрессирующим заболеванием, а также с тяжелой иммуносупрессией, не отвечающих на стандартный режим лечения, целесообразно использование более высоких доз #осельтамивира** (150 мг два раза в сутки) и более длительного лечения (как минимум, 10 дней) [2] [274]. С осторожностью назначать увеличенные дозы осельтамивира** пациентам с почечной недостаточностью. В случаях, когда осельтамивира** нет в наличии или его невозможно использовать или если вирус устойчив к осельтамивиру**, пациенты с тяжелым или прогрессирующим заболеванием должны получать лечение занамивиром. Пациенты, подверженные повышенному риску развития тяжелого заболевания или заболевания, протекающего с осложнениями, но у которых имеет место заболевание в связи с инфекцией вирусом гриппа, протекающее без осложнений, должны получать лечение осельтамивиром** или занамивиром. Комбинация противовирусных препаратов прямого действия (осельтамивира** и занамивира) с другими препаратами опосредованного (непрямого) механизма действия не имеет достаточной доказательной базы и не внесена в ИМП.
Рекомендовано незамедлительно после поступления в стационар начать лечение балоксавиром марбоксилом пациентам с симптомами гриппа, как высокоэффективным селективными ингибитором РНК-полимеразы вирусов гриппа типа А и В для прекращения репликации вируса [125-129].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: балоксавир марбоксил может быть назначен взрослым и детям старше 12 лет, как не имеющих дополнительных заболеваний, так и подверженных риску развития осложнений гриппа. Препарат применяется внутрь однократно, вне зависимости от приема пищи. При массе тела пациента от 40 кг до 80 кг - 40 мг , ≥80 кг - 80 мг. Увеличение дозы препарата, как и комбинация его с другими препаратами прямого (ингибиторы нейраминиздазы, фузии) и непрямого противовирусного действия не имеет достаточной доказательной базы и не внесена в ИМП.
Рекомендовано в назначение Меглюмина натрия сукцината* пациентам со среднетяжелым и тяжелым течением, а также пациентам с наличием пневмонии с антигипоксической и антиоксидантной целью для купирования синдрома интоксикации [244-249].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 1).
Комментарии: вводят внутривенно капельно со скоростью 1-4,5 мл/мин (до 90 капель в минуту). Средняя суточная доза -10 мл/кг. Курс терапии – до 11 дней. Объем и длительность зависит от степени тяжести пациента.
Рекомендовано назначение нестероидных противовоспалительных и противоревматических препаратов или анилидов пациентам с гипертермией выше 38 С, мышечными и суставными болями с жаропонижающей, болеутоляющей и противовоспалительной целью [52, 62, 193]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: ибупрофен** перорально по 200–400 мг 3–4 раза в 0 сутки в течение 3–10 дней (максимальная суточная доза — 1200 мг), парацетамол** перорально по 1–2 табл. (500–1000 мг) до 4 раз в сутки (максимальная суточная — 4000 мг.)
Рекомендовано назначение парацетамола в комбинации с другими препаратами, кроме психолептиков, пациентам с выраженными лихорадочно-интоксикационным и респираторным синдромами с анальгезирующей, жаропонижающей, противоаллергической, антиконгестивной целью :
Парацетамол+Фенилэфрин+Фенирамин [252-258].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 2)
Комментарии: Внутрь. Содержимое 1 пакетика растворяют в 1 стакане кипяченой горячей воды. Принимают в горячем виде. Можно добавить сахар по вкусу. Повторную дозу можно принимать через каждые 4 ч (не более 3 доз в течение 24 ч).
Не рекомендуется назначение салициловой кислоты и ее производных пациентам с гипертермией с жаропонижающей целью, вследствие возможных побочных явлений в виде нарушения гемостаза и обострения язвенной болезни желудка и 12-ти перстной кишки [52, 62, 92, 193].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендовано пациентам с острым бронхитом, обусловленным вирусом гриппа сопровождающихся бронхообструкцией и влажным кашлем, назначение отхаркивающих препаратов, кроме комбинаций с противокашлевыми средствами для разжижения и улучшения отхождения мокроты [52, 62, 258, 264-266].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Ацетилцистеин** – по 1 таблетке по 200 мг – 2-3 раза в день, перорально, курс до 5 дней; Бромгексин – внутрь по 8 мг 3 (1–2 таблетки) 3–4 раза в сутки; Амброксол** – внутрь 30 мг, 90 мг/сут, курс до 5 дней; [110]. Бромгексин + Гвайфенезин + Сальбутамол – таблетки (2 мг сальбутамола сульфата + 8 мг бромгексина гидрохлорида + 100 мг гвайфенезина в 1 таблетке) внутрь по 1 таблетке 3 р./сут в течение 5 дней.
Рекомендуется назначение симпатомиметиков и прочих противокашлевых препаратов при лечении гриппа у пациентов с сухим непродуктивным надсадным кашлем, значительно ухудшающим качество жизни [52, 62, 256, 258, 260, 270-273].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Препаратами выбора являются противокашлевые препараты в комбинации с отхаркивающими препаратами, в состав которых состав которых входит активное вещество декстрометорфан:
- R05DB Другие противокашлевые препараты Бутамират – внутрь по 15 мл 4 раза в сутки (сироп)
- R05FB Другие противокашлевые средства в комбинации с отхаркивающими средствами Декстрометорфан+Терпингидрат+[Левоментол]– внутрь по 1 чайной ложке (5 мл) 3-4 раза в день.
- R01BA Симпатомиметики Декстрометорфан+Парацетамол+Псевдоэфедрин+[Аскорбиновая кислота] – по одной таблетке 4 раза в день
- R05X Другие препараты для лечения простудных заболеваний Декстрометорфан+Фенилэфрин+Хлорфенамин 5 – 7,5 мл сиропа 3-4 раза в сутки.
Не рекомендовано одновременное применение отхаркивающих и противокашлевых средств пациентам с кашлем, что может способствовать застою мокроты за счет подавления кашлевого рефлекса [52, 62, 256-258].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Рекомендуется местное применение адреномиметиков пациентам с выраженным затруднением носового дыхания в комплексной терапии ринита, риносинусита для облегчения заложенности носа и восстановления проходимости слуховой трубы не более 5 дней [52, 62, 195, 196].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Нафазолин – интраназально (в каждый носовой ход) по 1–3 капли 0,05–0,1% раствора 3–4 раза в сутки;
o Ксилометазолин** – интраназально (в каждый носовой ход), по 2–3 капли 0,1% раствора или одно впрыскивание из распылителя в каждую ноздрю 4 раза в день;
o Оксиметазолин – интраназально (в каждый носовой ход), по 1–2 капли 0,025–0,05% раствора 2–3 раза в сутки или по 2–3 впрыскивания 0,05% спрея.
Дополнительно рекомендовано применение стрессовых (малых/средних) доз глюкокортикоидов для системного применения у больных с рефрактерным септическим шоком и с ранней фазой острого респираторного дистресс-синдрома с противовоспалительной целью (ОРДС) [52, 62, 87, 88, 95, 97, 101].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: необходимо избегать применения данной группы препаратов, если только они не показаны по другим причинам. Продолжительный прием высоких доз кортикостероидов для системного применения у пациентов с текущей репликацией вируса гриппа может привести к серьезным отрицательным последствиям, включая оппортунистическую инфекцию и длительную репликацию вируса. При гриппе, вызванном высокопатогенным штаммом A(H1N1)pdm09, назначение от умеренной до высокой дозы глюкокортикоидовв качестве дополнительного средства лечения не рекомендуется (польза не доказана, воздействие может быть потенциально вредным)[1].
Рекомендовано проведение ингаляторное введение кислорода пациентам с наличием гипоксемии для обеспечения обеспечении адекватной оксигенации [50, 51, 52, 62, 87, 88, 95, 97, 101, 211, 212].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Показаниями является РО2 <60 мм рт ст. или SaO2 <90% (при FiО2 = 0.21, т.е. при дыхании воздухом). Считается оптимальным поддержание SaO2 в пределах 88–95% или PO2 – в пределах 55–80 мм рт ст. В некоторых клинических ситуациях, например, во время беременности, целевой уровень SaO2 может быть повышен до 92–95%. При проведении ингаляторного введения кислорода, кроме определения показателей SaO2 и РО2, желательно также исследовать показатели РСО2 и рН. Необходимо помнить, что после изменения режимов ингаляторного введения кислорода стабильные значения газов крови устанавливаются только через 10–20 минут, поэтому более ранние определения газового состава крови не имеют значения.
Рекомендовано проведение интубации трахеи и искусственной вентиляции легких (ИВЛ) при наличии острой дыхательной недостаточности (ОДН) для обеспечения адекватного газообмена [50, 51, 52, 62, 87, 88, 95, 97, 101, 211, 212].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Задачи респираторной поддержки больных с ОДН, вызванной гриппом:
o Коррекция нарушений газообмена (достижение PO2 в пределах 55 – 80 мм рт ст., SaO2 – 88 – 95%);
o Минимизация риска развития баро- и волюмотравмы;
o Оптимизация рекрутирования альвеол;
o Раннее отлучение больного от респиратора;
o Проведение комплекса специальных мероприятий, направленных на ограничение риска распространения вируса от больного к персоналу и другим больным.
Принципы респираторной поддержки при ОРДС, вызванном вирусом гриппа, представлены в Приложении А3.
При крайне тяжелых случаях ОРДС рекомендовано проведение экстракорпоральной мембранной оксигенации (ЭКМО) для обеспечения адекватного газообмена [50, 51, 52, 62, 87, 88, 95, 97, 101, 211, 212].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Быстрота прогрессирования ОРДС у больных с гриппом диктует необходимость осуществить заблаговременный контакт с центром, располагающим возможностями проведения ЭКМО. ЭКМО проводится в отделениях, имеющих опыт использования данной технологии: стационары, в которых есть специалисты, в т.ч. хирурги, перфузиологи, владеющие техникой канюлизации, настройкой ЭКМО.
Потенциальные показания к ЭКМО:
o Рефрактерная гипоксемия: PO2/FiO2 < 50 мм рт. ст., персистирующая* (несмотря на FiO2 > 80% + PEEP (≤ 20 см H2O) при Pplat = 32 см H2O + прональная позиция +/- ингаляционный NO);
o Давление плато ≥ 35 см H2O (несмотря на снижение PEEP до 5 см H2O и снижение VT до минимального значения (4 мл/кг) и pH ≥7,15).
* Характер персистирования зависит от динамики процесса (несколько часов для быстропрогрессирующих состояний и до 48 часов в случае стабилизации).
Противопоказания к ЭКМО:
o Тяжелые сопутствующие заболевания, с предсказанной продолжительностью жизни больного не более 5 лет;
o Полиорганная недостаточность и SAPS II > 90 баллов или SOFA >15 баллов;
o Немедикаментозная кома (вследствие инсульта);
o Решение об ограничении терапии;
o Техническая невозможность венозного или артериального доступа;
o Индекс массы тела >40 кг/м2.
Рекомендовано назначение легочных сурфактантов пациентам с ОРДС с заместительной целью [71, 72, 211, 212, 280-282].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Рекомендовано назначение прочих противовирусных препаратов для профилактики бактериальных осложнений группам риска по развитию неблагоприятных осложнений (лица старше 60 лет; лица, страдающие заболеваниями эндокринной системы (диабет), нарушениями обмена веществ (ожирение), болезнями системы кровообращения (ГБ, ИБС), хроническими заболеваниями дыхательной системы (хронический бронхит, бронхиальная астма), хроническими заболеваниями печени и почек) [187, 190, 191, 192, 194].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: препаратом выбора является оксодигидроакридинилацетат натрия; применяется в/м, по 250 мг (4 – 6 мг/кг), курс лечения 5–7 инъекций с интервалом 48 часов; при необходимости в разовой дозе до 500 мг (курсовая доза зависит от характера заболевания) [197-198].
Рекомендовано проведение терапии антибактериальными препаратами системного действия (ампициллин**, амоксициллин+клавулановая кислота** или ампициллин+сульбактам**, цефалоспорины III поколения (цефотаксим**, цефтриаксон**), альтернативы – фторхинолоны у пациентов при подозрении на развитие вирусно-бактериальной пневмонии в соответствии с утвержденными рекомендациями по ведению больных с внебольничной пневмонией [208-212, 251, 283-285].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
3.2. Хирургическое лечение
Не проводится.
[1] Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека Российской Федерации от 26.11.2009 № 01/17863-9–32 «О направлении документа ВОЗ «Клинические методы ведения больных, инфицированных пандемическим вирусом гриппа (H1N1)2009»
[2] Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 23 декабря 2009 года № 01/19753-9–32"О направлении временного руководства CDC в отношении гриппа А(H1N1)2009 у пациентов с тяжелой иммуносупрессией".
4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
Рекомендуется начинать реабилитационные мероприятия уже в периоде разгара или в периоде ранней реконвалесценции всем пациентам с гриппом [48, 51,52, 62, 75].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Рекомендуется комплексный характер восстановительных мероприятий с участием различных специалистов и с применением разнообразных методов воздействия всем пациентам с гриппом [48, 51,52, 62, 75].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Рекомендуется соблюдать последовательность и преемственность проводимых мероприятий, обеспечивающих непрерывность на различных этапах реабилитации и диспансеризации всем пациентам с гриппом [48, 51,52, 62, 75].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Рекомендуется адекватность реабилитационных и восстановительных мероприятий и воздействий адаптационным и резервным возможностям пациента с гриппом [48, 51, 52, 62, 75].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: важны постепенность возрастания дозированных физических и умственных нагрузок, а также дифференцированное применение различных методов воздействия
Рекомендуется постоянный контроль эффективности проводимых мероприятий всем пациентам с гриппом [48, 51, 52, 62, 75].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: учитываются скорость и степень восстановления функционального состояния и профессионально-значимых функций, переболевших (косвенными и прямыми методами)
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
5.1 Специфическая профилактика
Рекомендовано проведение вакцинации всем лицам, не имеющим противопоказаний в предэпидемический период для специфической профилактики гриппа [1] [213-228, 275-276].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: для специфической профилактики гриппа используются противогриппозные вакцины отечественного и зарубежного производства, зарегистрированные на территории Российской Федерации и приготовленные из эпидемически актуальных штаммов вируса, рекомендуемых ВОЗ. Вакцина для профилактики гриппа [живая]**
Вакцина для профилактики гриппа [инактивированная]**
Вакцина для профилактики гриппа [инактивированная]+Азоксимера бромид**
Сплит-вакцина для профилактики гриппа четырехвалентная инактивированная**
Вакцинации против гриппа в предэпидемический период в первую очередь подлежат лица, относящиеся к категории высокого риска заболевания гриппом и неблагоприятных осложнений при заболевании, к которым относятся:
- лица старше 60 лет, прежде всего проживающие в учреждениях социального обеспечения;
- лица, страдающие заболеваниями эндокринной системы (диабет), нарушениями обмена веществ (ожирение), болезнями системы кровообращения (ГБ, ИБС), хроническими заболеваниями дыхательной системы (хронический бронхит, бронхиальная астма), хроническими заболеваниями печени и почек;
- беременные женщины (только инактивированными вакцинами);
- лица, часто болеющие острыми респираторными вирусными заболеваниями;
- медицинские работники;
- работники сферы обслуживания, транспорта, учебных заведений;
- воинские контингенты.
Профилактические прививки проводятся лицам, не имеющим противопоказаний (наличие аллергических реакций на куриный белок и другие компоненты вакцины, наличие лихорадки или других признаков острых респираторных инфекций) с их согласия, а также с согласия законных представителей граждан, признанных недееспособными в порядке, установленном законодательством Российской Федерации. Вакцина для профилактики гриппа инактивированная** может вводиться одновременно с другими инактивированными вакцинами, применяемыми в рамках национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям.
Противогриппозные вакцины могут быть слабо иммуногенными у пациентов с тяжелой иммуносупрессией [2], поэтому можно рассмотреть [необходимость] химиопрофилактики против вируса гриппа для этой группы пациентов. Лицам с иммуносупрессией в возрасте 6 месяцев и старше рекомендуется ввести как вакцину для профилактики гриппа инактивированную против сезонного гриппа**, так и инактивированную моновалентную вакцину против гриппа А(H1N1)2009**. Кроме того, лицам в возрасте 6 месяцев и старше, контактирующим с членами семьи, имеющими тяжелую иммуносупрессию, рекомендуется ежегодная вакцинация инактивированной вакциной против сезонного гриппа.
Сезонную иммунопрофилактику гриппа рекомендуется закончить не позднее чем за 2 – 3 недели до начала эпидемического сезона.
5.2 Неспецифическая профилактика
5.2.1 Профилактические мероприятия, направленные на источник инфекции
Рекомендована своевременная диагностика и лечение больных гриппом[1] [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: больной человек наиболее заразен для окружающих в первые 3-4 дня болезни, хотя выделение вируса возможно на протяжении всего заболевания и даже периода реконвалесценции. Больные дети как источник инфекции опасны более длительный период (7-10 дней). При риске заражения гриппом (вспышка в коллективе, эпидемия в городе) большое значение имеет контроль граждан за состоянием своего здоровья, в первую очередь, термометрия и самоизоляция при появлении первых симптомов заболевания с последующим вызовом врача.
Рекомендовано в случае появления в семье больного с симптомами гриппа проведение следующих мероприятий1 [51,52, 62, 75, 231-233].
- изолировать больного в отдельном помещении, если это невозможно, обеспечить, чтобы его кровать, отгороженная ширмой, находилась на расстоянии более одного метра от места расположения других людей;
- часто проветривать помещения и проводить влажную уборку с использованием бытовых моющих и дезинфицирующих средств;
- кипятить и обрабатывать посуду, используемую больным, дезинфицирующими средствами в специальной емкости;
- тщательно мыть руки с мылом после каждого контакта с больным;
- носить маски, имеющиеся в продаже или сделанные из подручных материалов (ватно-марлевые) при условии их смены через каждые два часа с последующей утилизацией или надлежащей стиркой и двухсторонним проглаживанием.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
5.2.2 Профилактические мероприятия, направленные на механизмы и пути передачи
Рекомендовано использование антисептиков для текущей дезинфекции предметов личного обихода и всего помещения 1 [51,52, 62, 75, 231-233].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: этанол**, водорода пероксид**, щелочь (мыло), повидон-йод**, в соответствующих концентрациях на протяжении достаточного количества времени. Активным биологическим действием обладают ультрафиолетовые лучи (УФ). Обеззараживание помещений УФ лампами проводится как прямым, так и рассеянным облучением. Неотъемлемой и важной частью противоэпидемических мероприятий в очаге является текущая дезинфекция предметов личного обихода и всего помещения.
Рекомендовано использование одноразовых масок, носовых платков и полотенец персоналу и пациентам с гриппом 1 [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: маски должны быть одноразовыми и меняться через каждый час. В случае недоступности одноразовых, они подлежат частой замене и стирке с кипячением, как и остальное белье больного.
Рекомендовано проведение влажной уборки с применением дезинфицирующих средств в палате (боксе) не менее двух раз в сутки1 [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендовано после удаления больного из палаты (бокса) проведение заключительной дезинфекция: мытье стен, подоконников, мебели, полов с применением дезсредств, кипячение посуды, белья, УФ- облучение помещения1 [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
5.2.3 Профилактические мероприятия, направленные на восприимчивый организм
Рекомендовано проведение вакцинации всем лицам, не имеющим противопоказаний в предэпидемический период для специфической профилактики гриппа1 [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендовано ведение здорового образа жизни всем лицам (полноценный сон, свежий воздух, активный отдых, сбалансированное питание, прием витаминов) для повышения резистентность к инфекции 1 [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендована профилактика и своевременное лечение сопутствующих заболеваний и состояний всем лицам для повышения восприимчивости организма к вирусу гриппа [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендовано проведение химиопрофилактики лицам при наличии в анамнезе контакта с больным гриппом и ОРВИ другой этиологии с целью немедленного противовирусного действия и с целью повышение резистентности организма 1 [51, 52, 62, 75, 231-233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: неспецифическая профилактика подразделяется на два варианта: экстренную, рассчитанную на немедленное противовирусное действие химиопрепаратов, интерферонов, индукторов интерферона (внутриочаговая и внеочаговая (плановая), и сезонная профилактика, проводимая в предэпидемический период с целью повышение резистентности организма человека к респираторным вирусам во время максимальной вероятности заболевания. Внутриочаговую профилактику проводят среди лиц, находившихся в непосредственном контакте с больными, в семьях, квартирах, больничных палатах (эпидемических очагах). Продолжительность внутриочаговой профилактики колеблется от 2 дней при прекращении контакта с источником инфекции до 5-7 дней, если контакт сохраняется. Внеочаговую профилактику проводят среди непривитых, а также среди контингентов с повышенным риском заражения гриппом и с высоким риском неблагоприятных исходов заболевания.
Химиопрофилактика не заменяет вакцинацию против гриппа.
Рекомендовано избирательное использование препаратов прямого противовирусного действия у лиц после контакта с больным гриппом или в эпидемический сезон с целью экстренной и плановой химиопрофилактики [114, 116, 119, 229-231]:
o Осельтамивир** - экстренная профилактика: по 75 мг 1 раз в сутки не менее 10 дней после контакта с инфицированным (в зависимости от ситуации). Прием препарата нужно начинать не позднее чем в первые два дня после контакта. Рекомендуемая ранее плановая профилактика химиопрепаратами, например, осельтамивиром** – по 75 мг 1 раз в сутки в течение 6 недель в настоящее время не рекомендуется из-за развития резистентности вирусов к действию препарата [230, 277].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
o Занамивир – экстренная профилактика: при непосредственном контакте с больным гриппом: 2 ингаляции по 5 мг 1 раз в день, 10 дней. Общая суточная доза 10 мг. Плановая профилактика, так же, как и осельтамивиром**, не рекомендуется [277].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарии: химиопрофилактика противовирусными препаратами прямого действия из группы ингибиторов нейраминидазы не рекомендуется, если с момента первого контакта с больным гриппом прошло более 48 часов.
Избирательно используется:
- у лиц с высоким риском развития осложнений гриппа в течение первых двух недель после вакцинации после контакта с больным гриппом человеком;
- у лиц с высоким риском развития осложнений гриппа в случае документально подтвержденного факта низкой клинической эффективности вакцины в эпидсезоне из-за циркуляции штаммов вируса гриппа, антигенно далеких от вакцинных штаммов;
- у лиц с тяжелыми иммунодефицитами или других лиц, которые могут не реагировать адекватно на вакцинацию (например, получающие иммунодепрессанты, онкологических больных, реципиентов гемопоэтических клеточных трансплантатов и др.), после контакта с больным гриппом человеком;
- у лиц с высоким риском осложнений от гриппа, которым противопоказана вакцинация, после контакта с больным гриппом человеком;
- среди сотрудников и постояльцев заведений с длительным круглосуточным для получения лечения/ухода, во время вспышек гриппа в учреждении.
o Балоксавир марбоксил – экстренная профилактика: препарат следует принять как можно скорее в течение 48 часов после близкого контакта с заболевшим гриппом человеком. Препарат принимают внутрь однократно, вне зависимости от приема пищи, при массе тела пациента от 40 кг до 80 кг - 40 мг, ≥80 кг - 80 мг [130].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
o Умифеновир** – экстренная (постконтактная) профилактика: при контакте с больным по 200 мг в день в течение 10-14 дней. В период эпидемии гриппа (сезонная профилактика): по 200 мг 1 раз в день каждые 3-4 дня в течение 3 недель [141-143].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Рекомендовано использование интерферонов у лиц после контакта с больным гриппом или в эпидемический сезон с целью экстренной и плановой химиопрофилактики [170-173].
Интерферон лейкоцитарный человеческий (лиофилизат для приготовления назального введения) – содержимое растворяют в 5 мл воды для инъекций, интраназально по 5 капель в каждый носовой ход 2 раза в сутки (разовая доза – 3 тыс. МЕ, суточная доза – 15-18 тыс. МЕ), в течение 5 – 7 дней. При однократном контакте достаточно одного закапывания. При необходимости профилактические курсы повторяют. При сезонном повышении заболеваемости в указанной дозе, утром 1 – 2 дня [279].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Рекомендовано использование иммуностимуляторов у лиц после контакта с больным гриппом или в эпидемический сезон с целью экстренной и плановой химиопрофилактики [169,176, 177, 178, 181, 184, 185, 188, 192].
o Кагоцел** – по 24 мг (2 таблетки) 1 раз в день в течение 2 дней, затем перерыв 5 дней, затем цикл повторить; длительность приема от 1 недели до нескольких месяцев [175, 278]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
o Тилорон** – 125 мг 1 раз в неделю в течение 6 недель, курсовая доза составляет 750 мг. [177, 180, 182, 183, 184]
Уровень убедительности рекомендаций С (уровень достоверности доказа тельств – 5)
o Оксодигидроакридинилацетат натрия [197,198]
– разовая профилактическая доза составляет 250 мг (1 ампула) или 4 – 6 мг на кг массы тела. При длительном применении рекомендуемый интервал между введениями 3–7 суток.
Уровень убедительности рекомендаций В (уровень достоверности доказа тельств – 3)
o Меглюмина акридонацетат [233, 239, 240, 243]
Внутрь один раз в сутки за 30 минут до еды, не разжёвывая, запивая ½ стакана воды, взрослым и детям старше 12 лет: по 450–600 мг (3–4 таблетки) на приём на 1, 2, 4, 6, 8-е сутки после контакта. Далее осуществляют перерыв 72 часа (трое суток) и продолжают курс на 11, 14, 17, 20, 23-и сутки. Общий курс составляет от 5 до 10 приёмов.
Уровень убедительности рекомендаций С (уровень достоверности доказа тельств – 2)
o Азоксимера бромид [261, 263-266, 267, 268].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: для профилактики в предэпидемический период – по 1 таблетке в день в течение 10 дней.
Примечание: для проведения неспецифической профилактики гриппа можно применять любые препараты (в соответствии с инструкцией к применению препарата), разрешенные к применению в установленном порядке на территории Российской Федерации
[1] СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней». XXXIV. Профилактика гриппа и других острых респираторных вирусных инфекций (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
[2] Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 23 декабря 2009 года № 01/19753-9-32"О направлении временного руководства CDC в отношении гриппа А(H1N1)2009 у пациентов с тяжелой иммуносупрессией".
6. Организация оказания медицинской помощи
На выбор тактики лечения оказывают влияние следующие факторы [50–52, 62, 63, 85, 86]: возраст пациента; характер сопутствующих заболеваний; клиническая форма болезни; характер течения болезни (динамики нарастания симптомов); тяжесть заболевания; наличие и характер осложнений.
До принятия решения о тактике ведения больного гриппом рекомендуется установить дефиницию случая гриппа у больного: неосложненный грипп или осложненный/тяжелый грипп1[51, 52, 62, 63, 75].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: алгоритм клинической сортировки пациентов с ГПЗ представлен в Приложении А3.
Рекомендуется госпитализировать больных [1] [52, 62, 63,75]:
− с тяжелым и средне-тяжелым течением гриппа;
− проживающих в общежитиях и в условиях неблагоприятных факторов жилой среды
− из группы риска развития неблагоприятного течения болезни.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: группы риска развития неблагоприятного течения болезни описаны в п.7
Рекомендуется срочно пересмотреть схемы ведения больного гриппом при появлении признаков (симптомов) прогрессирующего течения болезни[1],1[52, 62, 63,75]:
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: 1) при симптомах, свидетельствующих об ухудшении снабжения организма кислородом или сердечно-легочной недостаточности (одышка (при движении или в состоянии покоя), затрудненное дыхание, синюшность, кровянистая или окрашенная мокрота, боль в груди, гипотония; гипоксия, определяемая по показаниям пульсоксиметра);
2) при симптомах, свидетельствующих об осложнениях со стороны ЦНС (измененное психическое состояние, бессознательное состояние, сонливость или трудности с пробуждением и периодические или постоянные конвульсии (судороги), спутанность сознания, сильная слабость или паралич);
3) при подтверждении текущей устойчивой репликации вируса гриппа или вторичной бактериальной инфекции, основанное на результатах лабораторных исследований или клинических признаках (например, сохранение постоянной высокой температуры тела и других симптомов более 3 дней);
4) при появлении тяжелого обезвоживания, проявляющегося в пониженной активности, головокружении, сниженном диурезе и вялости.
Рекомендована выписка из медицинской организации при стойком улучшение клинической картины: нормализации температуры тела, купировании респираторно-катарального синдрома, нормальных показателях общего анализа крови[2] [52, 62, 63,75]:
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Медицинская помощь оказывается в форме:
o экстренной медицинской помощи;
o неотложной медицинской помощи;
Условия оказания медицинских услуг
Медицинская помощь оказывается в виде:
o первичной медико-санитарной помощи;
o скорой, в том числе скорой специализированной, медицинской помощи;
o специализированной, в том числе высокотехнологичной, медицинской помощи.
Медицинская помощь взрослым больным гриппом может оказываться в следующих условиях:
o амбулаторно (в условиях, не предусматривающих круглосуточное медицинское наблюдение и лечение);
o стационарно (в условиях, обеспечивающих круглосуточное медицинское наблюдение и лечение).
Первичная медико-санитарная помощь пациентам оказывается в амбулаторных условиях и в условиях дневного стационара.
Первичная доврачебная медико-санитарная помощь в амбулаторных условиях осуществляется в фельдшерско-акушерских пунктах.
Первичная врачебная медико-санитарная помощь осуществляется врачом-терапевтом участковым, врачом общей практики (семейным врачом) в амбулаторных условиях.
Первичная специализированная медико-санитарная помощь осуществляется врачом-инфекционистом медицинской организации, оказывающим медицинскую помощь пациентам в амбулаторных условиях.
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается в условиях стационара врачами-инфекционистами и другими врачами-специалистами и включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских технологий, а также медицинскую реабилитацию.
Лечение пациентов осуществляется в условиях стационара по направлению врача-терапевта участкового, врача общей практики (семейного врача), врача-инфекциониста, медицинских работников, выявивших грипп.
[1]СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней». XXXIV. Профилактика гриппа и других острых респираторных вирусных инфекций (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
[2] Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека Российской Федерации от 26.11.2009 № 01/17863-9–32 «О направлении документа ВОЗ «Клинические методы ведения больных, инфицированных пандемическим вирусом гриппа (H1N1)2009»
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
К группам риска тяжелого течения гриппа относятся следующие лица[1]:
беременные на любом сроке беременности и в послеродовый период;
лица с хроническими заболеваниями легких (бронхиальная астма, ХОБЛ и др.);
лица с хроническими заболеваниями сердечно-сосудистой системы (пороки сердца, ГБ, ИБС с признаками сердечной недостаточности и др.);
лица с нарушениями обмена веществ (сахарный диабет, ожирение 2–3 степени и др.);
лица с хронической болезнью почек;
лица с хроническими заболеваниями печени;
лица, с определенными неврологическими состояниями (включая нейромускульные, нейрокогнитивные нарушения, эпилепсию);
лица с гемоглобинопатиями;
лица с первичными и вторичными иммунодефицитами (ВИЧ-инфекция, прием иммунодепрессантов и т.п.);
лица со злокачественными новообразованиями;
лица в возрасте 65 лет и старше.
[1] СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней». XXXIV. Профилактика гриппа и других острых респираторных вирусных инфекций (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
Критерии оценки качества медицинской помощи
Критерии качества оказания помощи больным гриппом
№ п/п | Критерии качества | Уровень достоверности доказательств | Уровень убедительности рекомендаций |
|---|---|---|---|
1 | Выполнен общий осмотр | 5 | С |
| Выполнена оценка жизненно-важных показателей –ЧДД, АД, ЧСС, термометрия | 5 | С |
2 | Выполнен общий (клинический) анализ крови развернутый | 5 | С |
3 | Выполнено молекулярно-биологическое исследование мазков со слизистой оболочки носоглотки и ротоглотки или иммунохроматографическое экспресс-исследование носоглоточного мазка на вирусы гриппа A и B. | 5 | С |
4 | Выполнено молекулярно-биологическое исследования мазков со слизистой оболочки носоглотки и ротоглотки или иммунохроматографическое экспресс-исследование носоглоточного мазка на коронавирус SARS-CoV-2 для проведения дифференциальной диагностики | 5 | С |
5 | Выполнено молекулярно-биологическое исследование мазков со слизистой оболочки носо – и ротоглотки на вирус парагриппа (Human Parainfluenza virus), риновирусы (Human Rhinovirus), аденовирус (Human Adenovirus), респираторно-синцитиальный вирус (Human Respiratory Syncytial virus), коронавирусы 229E, OC43, NL63, HKUI (Human Coronavirus), бокавирус (Human Bocavirus), метапневмовирус (Human Metapneumo virus) на амбулаторном этапе по клинико-эпидемиологическим показаниям:тяжелое течение, эпидемический очаг, пожилой возраст, угроза развития ОРДС, в стационаре - всем заболевшим для проведения дифференциальной диагностики | 5 | С |
6 | Выполнена пульсоксиметрия с измерением SpO2 | 5 | С |
7 | Выполнена прицельная рентгенография органов грудной клетки пациентам с явлениями бронхита и наличии физикальных признаков поражения легочной ткани | 5 | С |
8 | Выполнена рентгенограмма придаточных пазух при подозрении на синусит, вызванный присоединением бактериальной флоры | 5 |
С
9
Выполнена консультация смежных специалистов пациентам в случаях подозрения на осложнения: врача-невролога (при явлениях менингоэнцефалита), врача-пульмонолога (при наличии признаков пневмонии), врача-гематолога (при выраженных гематологических изменениях и геморрагическом синдроме), врача-кардиолога (при присоединении симптомов миокардита, острой сердечно-сосудистой недостаточности), врача-акушера-гинеколога (при развитии гриппа на фоне беременности)
5
С
10
Выполнена консультация врача анестезиолога-реаниматолога пациентам с наличием быстропрогрессирующей ОДН или другой органной недостаточностью и произведен перевод в ОРИТ при наличии показаний
5
С
11
Проведено ингаляторное введение кислорода при наличии гипоксемии
5
С
12
Проведена терапия противовирусными препаратами прямого действия не позднее 48 часов (занамивир – в первые 36 часов) после манифестации болезни
5
С
13
Проведена патогенетическая и симптоматическая терапия
5
С
14
Проведена терапия антибактериальными препаратами системного действия (ампициллин**, амоксициллин+клавулановая кислота** или ампициллин+сульбактам**, цефалоспорины III поколения (цефотаксим**, цефтриаксон**), альтернативы – фторхинолоны) у пациентов при подозрении на развитие вирусно-бактериальной пневмонии
5
С
15
Проведена выписка из медицинской организации при стойком улучшение клинической картины: нормализации температуры тела, купировании респираторно-катарального синдрома, нормальных показателях общего анализа крови
5
С
Список литературы
Каверин Н.В., Львов Д.К., Щелканов М.Ю. Ортомиксовирусы (Orthomyxovlridae). Руководство по вирусологии. Вирусы и вирусные инфекции человека и животных: монография; под ред. Д.К. Львова. — М.: МИА, 2013. – С. 307–314.
Щелканов М.Ю. Таксономическая структура Orthomyxoviridae: современное состояние и ближайшие перспективы. Вестник Российской академии медицинских наук. 2011; 5: С. 12–19.
Щелканов М.Ю., Колобухина Л.В., Львов Д.К. Грипп: история, клиника, патогенез. Лечащий врач. 2011;10: С. 33–38.
Field S., Winter G., Wraunlee G.C. Structure of the neuraminidase gene in human influenza virus A/PR/8/34. Nature. 1981; 290: Р.213-217.
Wiley D.C., Skehel J.J. The structure and function of the hemagglutinin membrane glycoprotein of influenza virus. Annual Revier of Biochemistry. 1987;56: Р.365-394.
Noda T., Kawaoka Y. Structure of influenza virus ribonucleoprotein complexes and their packaging into virions. Reviews in Medical Virology. 2010; 20(6): P. 380-391.
Ge S., Wang Z. An overview of influenza A virus receptors. Critical Reviews in Microbiology. 2011; 37(2): P. 157-165.
Gaur P., Munjhal A., Lal S. K. Influenza virus and cell signaling pathways. Medical Science Monitor. 2011; 17(6): P. RA148-154.
Rohm C., Zhou N., Suss J., Mackenzie J., Webster R. Characterization of novel influenza hemagglutinin HI5, criteria for determination of influenza A subtypes. Virology.1996; 217: Р.508- 516.
Castrucci M.R., Kawaoka Y. Biologic importance of neuramidase stalk length in influenza A virus. J. Virol. 1993; 61(2): Р.759-764.
Gamblin S. J., Skehel J. J. Influenza hemagglutinin and neuraminidase membrane glycoproteins. Journal of Biological Chemistry. 2010; 285(37): P. 28403-28409.
Xu R., McBride R., Nycholat C. M., Paulson J. C., Wilson I. A. Structural characterization of the hemagglutinin receptor specificity from the 2009 H1N1 influenza pandemic. Journal of Virology. 2012; 86(2): P. 982-990.
Gorman O.T., Bean W.J., Webster R.G. Evolutionary process in Influenza viruses: Divergence, Rapid Evolution and Stasis. Current topics in Microbiology and Immunology. 1992; 176: Р.75-97.
Xu X., Guo Y., Rota P., Hemphill M., Kendal A., Cox N. Genetic reassortment of human influenza virus in nature. Options for the Control of Influenza. 1993; 2: Р.203-207.
Castrucci M.R, Donatelli I., Sidoli L., Kawaoka Y., Webster R.G. Genetic reassortment between avian and human influenza A viruses in Italian pigs. Virology. 1993; 193: Р.503-506.
Иванова В.Т., Бурцева Е.И., Оскерко Т.А. Изменчивость и особенности распространения вируса гриппа A(H1N1) в период 1990 – 1998гг. Вопр. вирусол. 2000; 5: С. 18–22.
Lin Y.P., Shaw M., Gregory V. et al. Avian-to-human transmission of H9N2 subtype influenza A viruses. Relationship between H9N2 and H5N1 human isolated. PNAS. 2000; 97 (17): Р.9654- 9658.
Koopmans M., Wilbrink B., Conyn M. et al. Transmission of H7N7 avian influenza A virus to human beings during a large outbreak in commercial poultry farms in the Netherlands. Lancet. 2004; 363: Р.587-593.
Wong S.S., Yuen K.Y. Avian Influenza virus infection in humans. Chest.2006; 129: Р. 156- 168.
Garten R.J., Davis C.T., Russell C.A. et al. Antigenic and henetic characteristics of swine origin 2009 A(H1N1) influenza viruses circulating in humans. Science. 2009; 325 (5937): Р.197-201.
Львов Д.К., Бурцева Е.И., Прилипов А.Г. и др. Изоляция 24.05.2009 года и депонирование в Государственную коллекцию вирусов первого штамма A/Moscow/01/2009(H1N1)sw l, подобного свиному вирусу A(H1N1) от первого выявленного 21.05.2009 года пациента в г. Москве. Вопросы вирусологии. 2009; 5: С. 10–22.
Howard W. A., Essen S. C., Strugnell B. W. et al. Reassortant pandemic (H1N1) 2009 virus in pigs, United Kingdom. Emerging Infectious Diseases. 2011;17(6): P. 1049-1052.
Yewdell J. W. Viva la Revolución: Rethinking Influenza A Virus Antigenic Drift. Current Opinion in Virology. 2011; 1(3): P. 177-183.
Rota P.A., Wallis T.R., Harmon M.W., Rota J.S., Kendal A.P., Nerome K. Cocirculation of two distinct evolutionary lineages of influenza type B virus since 1983. Virology. 1990; 175: Р.59–68.
Rota P.A., Hemphill M.L., Whistler I.L., Regnery H.L., Kendal A.P. Antigenic and genetic characterization of two hemagglutinins recent cocirculating strains of influenza type B virus. J. Gen. Virol.1992;73: Р.2737–2742.
Гринбаум Е.Б., Литвинова О.М., Банников А.И. Полиморфизм популяции современных вирусов гриппа А и B человека. Вестник РАМН. 1994; 9: С.36-41.
McCullers J.A., Saito T., Iverson A.R. Multiple genotypes of influenza B virus circulated between 1979 and 2003. J Virol 2004;78: Р.12817-12828.
Иванова В.Т., Бурцева Е.И., Слепушкин А.Н. Особенности вирусов гриппа, обусловивших эпидемический подъем заболеваемости в России в 2002–2003 гг. Возврат в циркуляцию вирусов гриппа, подобных В/Виктория/2/87. Вопросы вирусологии. 2004; 3: С.12.
Guo Y.J. Isolation of influenza С virus from pigs and experimental infection of pigs with influenza С virus. Journal of General Virology. 1983; 64: P. 177-182.
Yuanji G., Desselberger U. Genome analysis of influenza С viruses isolated in 1981/82 from pigs in China. Journal of General Virology. 1984; 65: P. 1857-1872.
Киселёв О.И., Исаков В.А., Шаронов Б.П., Сухинин В.П. Патогенез тяжёлых форм гриппа. Вестник Российской академии медицинских наук. 1994; 9: С. 32–36.
Fukuyama S., Kawaoka Y. The pathogenesis of influenza virus infections: the contributions of virus and host factors. Current Opinion in Immunology. 2011; 23(4): P. 481-486.
Цинзерлинг В.А., Воробьев С.Л., Зарубаев В.В. и др. Патогенетические аспекты гриппа в период эпидемии, вызванной вирусом A/H1N1v в 2009–2010 гг. по аутопсии. Архив патологии. 2011; 73(6): С. 21–25.
Щелканов М.Ю. Патогенез гриппа: механизмы модуляции белками возбудителя. Журнал инфектологии. 2015; 7(2): С. 31–45.
Марков Х.М. Молекулярные механизмы дисфункции сосудистого эндотелия. Кардиология. 2005;12: С.62-72.
Endemann D.H., Schiffrin E.L. Endothelial dysfunction. J. Am. Soc. Nephrol. 2004; 15: P. 1983-1992.
Verma S., Anderson T.J. Fundamentals of endothelial dysfunction for the clinical cardiologist. Circulation. 2002; 105: P. 546–549.
Кузник Б.И. Клеточные и молекулярные механизмы регуляции системы гемостаза в норме и патологии. – Чита: Экспресс-изд-во, 2010. – 832 с.
Азаренок А.А. Роль вируса гриппа и его поверхностных белков в развитии дисфункции эндотелия: автореф. дис. ... канд. биол. наук: 03.02.02. – СПб., 2014. – 29 с.
Горбунов В.В. Повреждение эндотелия у пациентов пневмонией во время пандемии гриппа A H1N1 и возможность его коррекции. Забайкальский медицинский вестник. 2011; 2: С. 104–111.
Ратникова Л.И., Картополова Е.В. Гемодинамические нарушения у пациентов гриппом и роль оксида азота в их развитии. Инфекционные болезни. 2012; 10 (4): С. 27–30.
Эсауленко Е.В., Стуколкин К.О., Дунаева Н.В. и др. Редкие симптомы (диарея, менингизм, геморрагический синдром) у пациентов гриппом различных субтипов. ВестникНовгородского государственного университета им. Ярослава Мудрого. 2013; 71(1): С. 93–97.
Лаврищева, В.В. Этиология летальных пневмоний в период развития пандемии, вызванной вирусом гриппа A (H1N1) pdm09 в России. Вопросы вирусологии. 2013; 58 (3): С. 17–21.
Львов Д.К., Бурцева Е.И., Прилипов А.Г. и др. Возможная связь летальной пневмонии с мутациями пандемического вируса гриппа A(H1N1)swl в рецепторсвязывающем сайте субъединицы НА1 гемагглютинина. Вопросы вирусологии. 2010; 4: С. 4–9.
Чучалин А.Г. Патологическая анатомия лёгких при гриппе A (H1N1), по данным аутопсий. Пульмонология. 2010; 1: С. 5–11.
Цинзерлинг В.А., Васильева М.В., Эсауленко Е.В. и др. Анализ летальных исходов при гриппе A/H1N1/PDM09 в эпидемический сезон 2015-2016гг. Инфекционные болезни. 2016; 14(4): С. 80-83.
Mauad T. Lung pathology in fatal novel human influenza A(H INI) infection. American Journal of Respiratory and Critical Care Medicine. 2010; 181(1): P. 72-79.
Эсауленко Е.В., Го А.А., Сухорук А.А., Понятишина М.В., Позднякова М.В. Грипп: современные диагностические возможности и терапевтические подходы. Учебное пособие для студентов медицинских вузов. Сер. Библиотека педиатрического университета. Санкт-Петербург, 2015: 48с.
Львов, Д.К. Обнаружение аминокислотных замен аспарагиновой кислоты на глицин и глутаминовую кислоту в рецептор-связывающем сайте гемагглютинина в штамме пандемического вируса гриппа H1N1 от пациентов с летальным исходом и со среднетяжелой формой заболевания. Вопросы вирусологии. 2010; 55 (3): С. 15–18.
Киселёв О.И., Маринец И.Г., Соминина А.А. Грипп и другие респираторные инфекции: эпидемиология, профилактика, диагностика и терапия. СПб.: Боргес, 2003. – 244 с.
Киселев О.И., Цыбалова Л.М., Покровский В. И. Грипп: эпидемиология, диагностика, лечение, профилактика. – М., 2012. – 496 с.
Малышев Н.А., Эсауленко Е.В., Яковлев А.А. и др. Рекомендации по диагностике и лечению гриппа у взрослых пациентов (с моделями пациентов). Современная медицина; 2015: С. 2–56.
О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2016 году: Государственный доклад. – М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2017.–220 с.
Отчет о 5-м совместном совещании Европейского регионального бюро ВОЗ/ECDC по эпиднадзору за гриппом. WHO, Будапешт, Венгрия, 14–16 июня 2016 г.
Голохвастова H.O. Особенности современного течения гриппа A (H1N1 swl). Клиническая медицина. 2012; 6: С. 18–25.
Колобухина Л.В. Эпидемический сезон 2013–2014 гг. Госпитальный мониторинг и противовирусная терапия. Терапевтический архив. 2014; 86 (10): С. 52–59.
Карпова Л. С., Поповцева Н. М., Столярова Т. П. и др. Эпидемия гриппа в России в сезон 2014–15 гг. Microbiology Independent Research Journal. 2015; 2 (1): С.19–26.
Карпова Л.С., Волик К.М., Столяров К.А. и др. Влияние эпидемий гриппа на показатели смертности и «дополнительную» смертность от соматических и инфекционных заболеваний среди населения Санкт-Петербурга с 2009 по 2015 годы. Информационный бюллетень «Здоровье населения и среда обитания». 2016, №5:39-44.
Summary of WHO Technical Consultation: H1N1pdm Mortality Estimates, 25-26 October 2011.
Estimating Seasonal Influenza-Associated Deaths in the United States. URL: https://www.cdc.gov/%20flu/about/disease/us_flu-related_deaths.htm
Карпова Л.С., Волик К.М, Столяров., К.А. и др. «Дополнительная» смертность от отдельных нозологических форм соматических и инфекционных заболеваний среди детей и взрослых Санкт-Петербурга с 2009 по 2015 годы. Информационный бюллетень «Здоровье населения и среда обитания». 2016, №10: 8–11.
Инфекционные болезни. Национальное руководство. Под ред. акад. РАМ Н.Д. Ющука, акад. РАЕН Ю.Я. Венгерова. – 2-е изд., перераб. и доп. М.: Издательство ГЭОТАР-Медиа, 2019. –1004 с.
Lee N., Ison M. G. Diagnosis, management and outcomes of adults hospitalized with influenza. Antivir. Ther. 2012; 17: Р.143-157.
Monto A.S., Gravenstein S., Elliott M., Colopy M., Schweinle J. Clinical signs and symptoms predicting influenza infection. Arch Intern Med. 2000; 160: Р.3243-3247.
Сухорук А.А., Перадзе Х.Д., Хомченко И.В. Анализ эпидемиологических особенностей и клинической картины гриппа А/H1N1/California в Санкт-Петербурге у взрослых. Педиатр. 2011; 2(2): С. 41–46.
Яцышина С.Б., Шипулин Г.А. Совершенствование лабораторной диагностики гриппа и ОРЗ. Грипп и гриппоподобные инфекции (включая особо опасные формы гриппозной инфекции). Фундаментальные и прикладные аспекты изучения. 2008; 2: С. 43–48.
Яцышина С.Б., Миненко А.Н., Прадед М.Н. и др. Диагностика гриппа: новый вариант H1N1 в России. Эпидемиология и инфекционные болезни. 2009; 6: С.56-62.
Irving SA, Vandermause MF, Shay DK, Belongia EA. Comparison of nasal and nasopharyngeal swabs for influenza detection in adults. Clin Med Res. 2012;10(4):215-218.
Heikkinen T., Marttila J., Salmi A.A., Ruuskanen O. Nasal swab versus nasopharyngeal aspirate for isolation of respiratory viruses. J Clin Microbiol. 2002; 40: Р.4337-4339.
Hernes S.S., Quarsten H., Hamre R., et al. A comparison of nasopharyngeal and oropharyngeal swabbing for the detection of influenza virus by real-time PCR. Eur J Clin Microbiol Infect Dis. 2013;32(3):381-385.
Sung R.Y., Chan P.K., Choi K.C. et al. Comparative study of nasopharyngeal aspirate and nasal swab specimens for diagnosis of acute viral respiratory infection. J Clin Microbiol. 2008; 46: Р.3073-3076.
Sonal G., Kriengkrai P., Prabda P. et al. The acceptability and validity of self‐collected nasal swabs for detection of influenza virus infection among older adults in Thailand. Influenza Other Respir Viruses. 2017; 11(5): 412–417.
Akmatov MK, Gatzemeier A, Schughart K, Pessler F. Equivalence of self- and staff-collected nasal swabs for the detection of viral respiratory pathogens. PLoS One. 2012;7(11): e48508.
Лабораторная диагностика гриппа и других ОРВИ методом полимеразной цепной реакции. Клинические рекомендации, Москва, 2016:62 с.
Яцышина С.Б., Миненко А.Н., Кушакова Т.Е. и др. Пандемичный грипп А/ Н1N1(SW2009) в России: эпидемиология, диагностика, клиническая картина и лечение. Терапевтический архив. 2010; 11: Р.10-14.
Сухорук А.А. Использование молекулярно-биологического метода (ПЦР) в идентификации вируса гриппа А/H1N1/California у пациентов ОРВИ в период эпидемического подъёма заболеваемости в Санкт-Петербурге в 2009 году. Вестник гематологии. 2010; 6 (1): С. 66–67.
Лободанов С.А., Никонова А.А., Файзулоев Е.Б. и др. Оценка эффективности дифференциальной диагностики гриппа методом мультиплексной ПЦР с детекцией в режиме реального времени. Вопросы вирусологии. 2012; 57(1): С. 42–45.
Dare R., Zhu Y, Williams JV., et al. Detection of Influenza by Real Time RT-PCR is Not Affected by Delays in Specimen Processing of Respiratory Samples. J Med Virol. 2016; 88(11): 1891–1895.
Гребенникова Т.В., Забережный А.Д., Алипер Т.И. Молекулярная диагностика гриппа. Вестник Российской академии медицинских наук. 2011;5: С. 28–34.
Никонова А. А., Успенская Е. С., Лободанов С. А. и др. Применение метода мультиплексной ПЦР с детекцией в режиме реального времени для дифференциальной диагностики респираторных вирусных инфекций. Журн. микробиол. 2009; 1: С. 67–70.
Beck E.T., Jurgens L.A., Kehl S.C. et al. Development of a rapid automated influenza A, influenza B, and respiratory syncytial virus A/B multiplex real-time RT-PCR assay and its use during the 2009 H1N1 swine-origin influenza virus epidemic in Milwaukee, Wisconsin. J. Mol. Diagn. 2010;12 (1): P. 74-81.
Bellau-Pujol S., Vabret A., Legrand L. et al. Development of three multiplex RT-PCR assays for the detection of 12 respiratory RNA viruses. J. Virol. Meth. 2005; 26 (1-2): P. 53-63.
Choi WS, Noh JY, Huh JY et al. The clinical usefulness of the SD Bioline Influenza Antigen Test(R) for detecting the 2009 influenza A (H1N1) virus. Yonsei Med J. 2011; 52(4):683–685.
Tai CF, Lu CY, Shao PL et al. Rapid-test sensitivity for novel swine-origin pandemic influenza A. J Formos Med Assoc. 2012; 111(8):427-430.
Riley S., Kwok K. O., Wu K. M. et al. Epidemiological characteristics of 2009 (H1N1) pandemic influenza baised on paired sera from a longitudinal community cohort study. PLoS Medicine. 2011; 8: Р.e1000442.
Rahman M., Kieke B.A., Vandermause M.F., Mitchell P.D., Greenlee R.T., Belongia E.A. Performance of Directigen flu A+B enzyme immunoassay and direct fluorescent assay for detection of influenza infection during the 2004–2005 season. Diagn Microbiol Infect Dis. 2007; 58: Р.413- 418.
Чучалин А.Г., Авдеев С.Н., Черняев А.Л., Осипова Г.Л., Самсонова М.В. Федеральные клинические рекомендации Российского респираторного общества по диагностике и лечению тяжелых форм гриппа. Пульмонология. 2014;5: С. 11–19.
Рахманова А.Г., Полушин Ю.С., Яковлев А.А. и др. Методические рекомендации по лечению пациентов тяжелой формой грипп А H1N1 (опыт работы СПб ГУЗ Клинической инфекционной больницы им. С.П. Боткина). СПб, 2009.
Серебрякова О.М., Романова Е.Н., Говорин А.В. и др. Особенности клинико-рентгенологических проявлений пневмонии у пациентов гриппом А(Н1N1). Клиническая медицина. 2012; 6: С.70-72.
WHO Guidelines for Pharmacological Management of Pandemic Influenza A(H1N1) 2009 and other Influenza Viruses. WHO, 2010.
EAACI Position Paper on Rhinosinusitis and Nasal Polyps Executive Summary Allergy 2005, 60;5:583-601.
Клинические рекомендации «Грипп у беременных» http://www.influenza.spb.ru/files/publications/rii-influenza-pregnancy-clinical-guidelines-2015.pdf
URL:http://www.who.int/csr/disease/swineflu/guidance/surveillance/WHO_case_definition_swine_flu_2009_04_29 (Annex 3).
ВОЗ. Информационный бюллетень. Грипп. Ноябрь 2016 г. URL: http://www.who.int /mediacentre/factsheets/fs211/ru/
Диагностика и интенсивная терапия гриппа A(H1N1) pdm 2009 осложнённого течения. Клинические рекомендации, подготовленные общероссийской общественной организацией (Федерация анестезиологов и реаниматологов) 2017 г.
Protocol for the Use of Oseltamivir (and Zanamivir) for the Post-Exposure Prophylaxis and Treatment of Seasonal Influenza (A or B) for ‘At-Risk’ Inpatients (Version 5 – October 2014), NICE.
Клинические методы ведения пациентов, инфицированных пандемическим вирусом гриппа А(H1N1)2009: переработанное руководство, ВОЗ 2009:8 с.
Li TC, Chan MC, Lee N. Clinical Implications of Antiviral Resistance in Influenza Viruses. 2015; 7 (9): 4929–4944.
Recommended composition of influenza virus vaccines for use in the 2016-2017 northern hemisphere influenza season WHO February 2016:7 p.
Sominina A., Burtseva E., Eropkin M., et al. Influenza surveillance in Russia based on epidemiological and laboratory data for the period from 2005 to 2012. American Journal of Infectious Diseases 2013; 9 (3): 77-93.
Львов Д.К., Чучалин А.Г., Шестакова И.В. и др. Методические рекомендации «Диагностика и лечение гриппа у взрослых пациентов в эпидемический сезон 2016-2017гг.» http://iia-rf.ru/upload/iblock/1f2/1f2bd1205d716438f32c1ab9f11e9e1c.PDF
Stiver G. The treatment of influenza with antiviral drugs. Canadian Medical Association Journal. 2003; 1689(1): P. 49-57.
De Clercq E. Antiviral agents active against influenza A viruses. Nat. Rev. Drug. Disc. 2006; 5: Р.1015-1021.
Kawai N. A comparison of the effectiveness of oseltamivir for the treatment of influenza A and influenza B: a Japanese multicenter study of the 2003–2004 and 2004–2005 influenza seasons. Clin. Infect. Dis.2006; 43 (4): P. 445-446.
Kaiser L. Impact of oseltamivir treatment on influenza-related lower respiratory tract complications and hospitalizations. Arch. Intern. Med. 2003; 163: P. 1167-1172.
Dixit R., Khandaker G., Ilgoutz S. et al. Emergence of oseltamivir resistance: control and management of influenza before, during and after the pandemic. Infect Disord Drug Targets. 2013; 13 (1): Р.34-45.
Савенкова М.С. Новый отечественный препарат Номидес (осельтамивир) для лечения гриппа у детей и взрослых. Эффективная фармакотерапия. 2016; 40: 4–8.
Oxford J.S. Targeting influenza virus neuraminidase a new strategy for antiviral therapy. Drug Discovery Today. 1998; 3: Р.44856.
Nicholson K.G., Aoki F.Y., Osterhaus A.D.M.E. et al. Efficacy and safety of oseltamivir in treatment of acute influenza: a randomised controlled trial. Lancet. 2000;355: Р.1845-1850.
Treanor J.J., Hayden F.G., Vrooman P.S. et al. Efficacy and safety of the oral neuraminidase inhibitor oseltamivir in treating acute influenza. JAMA 2000; 283: Р.1016-1024.
Bardsley-Elliot A., Noble S. Oseltamivir. Drugs. 1999; 58: Р.851-860.
Winquist A.G., Fukuda K., Bringes C.B. et al. Neuraminidase inhibitors for treatment of influenza A and B infections. MMWR Recomm Rep. 1999; 48(RR14): Р.1-9.
Leneva I.A., Roberts N., Govorkova E.A. et al. The neuraminidase inhibitor GS4104 (oseltamivir phosphate) is efficacious against A/Hong Kong/156/97 (H5N1) and A/Hong Kong/1074/99 (H9N2) influenza viruses. Antiviral. Research 2000; 48: Р.101-115.
Деева Э.Г., Мельникова Т.И. Антивирусные препараты для профилактики и лечения гриппа. Эпидемиология и вакцинопрофилактика. 2009; 4 (47): С. 38–43.
Leneva I.A., Burtseva E.I., Yatsyshina S.B. et al. Virus susceptibility and clinical effectiveness of anti-influenza drugs during the 2010-2011 influenza season in Russia. Int J Infect Dis. 2016;43: P.77-84.
Heneghan CJ, Onakpoya I, Thompson M, Spencer EA, Jones M, Jefferson T. Zanamivir for influenza in adults and children: systematic review of clinical study reports and summary of regulatory comments. BMJ. 2014; 9; 348: g2547.
Осидак Л.В., Зарубаев В.В., Афанасьева О.И. и др. Осельтамивир – средство противовирусной терапии гриппа A(H1N1 )PDM09 у детей и взрослых. Детские инфекции. 2016; 15(3): С. 19–24.
Баранова И.П., Свистунова Н.В. Сравнительное исследование эффективности антивирусных препаратов в комплексном лечении гриппа. Инфекционные болезни. 2014; 12(2): С. 46–53.
Васильев Ю. Ингибиторы нейраминидазы для специфической профилактики и терапии гриппозной инфекции. Врач. 2014; 2: С.17-19.
Cass L.M.R., Brown J., Pickford M. et al. Pharmacoscintigraphic evaluation of lung deposition of inhaled zanamivir in healthy volunteers. Clin Pharmacokinet 1999; 36(suppl 1): Р.21- 31.
The MIST (Management of Influenza in the Southern Hemisphere Trialists) Study Group. Randomised trial of efficacy and safety of inhaled zanamivir in treatment of influenza A and B virus infections. Lancet 1998; 352: Р.1877-1881.
Matsumoto K., Ogawa N., Nerome K. et al. Safety and efficacy of the neu-raminidase inhibitor zanamivir in treating influenza virus infection in adults: results from Japan. Antiviral Ther. 1999;4: Р.61-68.
Murphy K.R., Pauksens K., Stein W.J. et al. Efficacy and safety of inhaled zanamivir for the treatment of influenza in patients with asthma or chronic obstructive pulmonary disease: A double-blind, randomised, placebo-controlled, multicentre study. Clin. Drug. Invest. 2000; 20(5): Р.337-349.
Daniel M.J., Barnett J.M., Pearson B.A. The low potential for drug interactions with zanamivir. Clin Pharmacokinet. 1999; 36(Suppl 1): Р.41-50.
Hayden FG, Sugaya N, Hirotsu N, et al. Baloxavir marboxil for uncomplicated influenza in adults and adolescents. N Engl J Med 2018; 379:913-23.
Ison MG, Portsmouth S, Yoshida Y, et al. LB16. Phase 3 Trial of Baloxavir Marboxil in High-Risk Influenza Patients (CAPSTONE-2 Study). Open Forum Infect Dis. 2018;5(Suppl 1): S764-S765.
Тайеб В., Икеока Х., Ма Ф.-Ф. и др. Сетевой метаанализ эффективности и безопасности балоксавира марбоксила в сравнении с ингибиторами нейраминидазы при лечении гриппа у пациентов без факторов риска. Терапевтический архив. 2020; 92 (11): 51–60.
Taieb V, Ikeoka H, Wojciechowski P, Jablonska K, Aballea S, Hill M, Hirotsu N. Efficacy and safety of baloxavir marboxil versus neuraminidase inhibitors in the treatment of influenza virus infection in high-risk and uncomplicated patients - a Bayesian network meta-analysis. Curr Med Res Opin. 2020 Nov 9:1-20.
Komeda T, Takazono T, Hosogaya N, Miyazaki T, Ogura E, Iwata S, Miyauchi H, Honda K, Fujiwara M, Ajisawa Y, Watanabe H, Kitanishi Y, Hara K, Mukae H. Comparison of Hospitalization Incidence in Influenza Outpatients Treated With Baloxavir Marboxil or Neuraminidase Inhibitors: A Health Insurance Claims Database Study. Clin Infect Dis. 2020 Dec 23: ciaa1870.
Ikematsu H, Hayden FG, Kawaguchi K, et al. Baloxavir marboxil for prophylaxis against influenza in household contacts. N Engl J Med 2020; 383:309-20.9.
Kadam R.U., Wilson I.A. Structural basis of influenza virus fusion inhibition by the antiviral drug Arbidol. Proc Natl Acad Sci U S A. 2017;114(2): P.206-214.
Bulgakova V.A., Poromov A.A., Grekova A.I. et al. Pharmacoepidemiological study of the course of influenza and other acute respiratory viral infections in risk groups. Ter Arkh. 2017;89(1): P62-72.
Leneva IA, Burtseva EI, Yatsyshina SB, et al. Virus susceptibility and clinical effectiveness of anti-influenza drugs during the 2010-2011 influenza season in Russia. Int J Infect Dis. 2016; 43:77-84.
Shi L., Xiong H., He J. et al. Antiviral activity of arbidol against influenza A virus, respiratory syncytial virus, rhinovirus, coxsackie virus and adenovirus in vitro and in vivo. Arch. Virol. 2007; 152: Р.1447-1455.
Kiselev O.I., Maleev V.V., Deeva É.G. et al. Clinical efficacy of arbidol (umifenovir) in the therapy of influenza in adults: preliminary results of the multicenter double-blind randomized placebo-controlled study ARBITR. Ter Arkh. 2015;87(1): P.88-96.
Зырянов С.К., Бутранова О.И., Гайдай Д.С., Крышень К.Л. Фармакотерапия острых респираторных инфекций, вызванных вирусами гриппа: современные возможности. Терапевтический архив, №1–2021.
Зарубаев В.В., А.В. Слита, Е.О. Синегубова, А.А. Мурылёва, И.Н. Лаврентьева. Противовирусная активность энисамия йодида в отношении вирусов гриппа и ОРВИ In Vitro на разных клеточных линиях. Терапевтический архив, №11 2020г., стр. 45–50.
Лиознов Д.А., Карнаухова Е.Ю., Зубкова Т.Г., Шахланская Е.В. Оценка эффективности схемы лечения ОРВИ, включающей этиотропную (энисамия йодид) и симптоматическую терапию. Терапевтический архив, том 92 (№3 2020 г.), стр. 50–55.
Kramarev S.A., Moshchich A.P. The treatment of influenza and acute respiratory viral infections. Lik Sprava. 2013;2: P.99-106.
Liu Q., Xiong H.R., Lu L., Liu Y.Y., Luo F., Hou W., Yang Z.Q. Antiviral and anti-inflammatory activity of arbidol hydrochloride in influenza A (H1N1) virus infection. Acta Pharmacol Sin. 2013; 34(8): Р.1075-1083.
Kadam R.U., Wilson I.A. Structural basis of influenza virus fusion inhibition by the antiviral drug Arbidol. Proc Natl Acad Sci U S A. 2017;114(2):206-214.
Ленева И.А., Гуськова Т.А. Арбидол – эффективный препарат для лечения и профилактики гриппа и ОРВИ: обзор результатов клинических исследований. РМЖ. 2008; 16 (29): С.1972–1976.
Якимова С.С. Стратегия противовирусной терапии при гриппе как лечение и профилактика тяжелых осложнений: обзор результатов клинических исследований препарата Арбидол. Consilium Medicum. 2010;12 (4): С.21-24.
Ситников И. Г., Еганян Г. А., Гроппа Л. Г., и др. Лечение ОРВИ и гриппа в рутинной клинической практике: результаты промежуточного анализа неинтервенционного, открытого, проспективного, наблюдательного исследования. Лечащий врач, 2015, № 9. С. 95–99.
Миронов И.Л., Ратникова Л.И. Триазавирин: изучение клинической эффективности при гриппозной инфекции. Поликлиника. 2015. № 5–3. С. 54–55.
Сабитов А.У., Ковтун О. П., Бацкалевич Н. А., Львов Н. И., Жданов К. В., Эсауленко Е. В., Тихонова Е. П., Калинина Ю. С., Сорокин П. В., Чепур С. В., Степанов А. В. Метаанализ рандомизированных клинических исследований эффективности препарата Риамиловир в этиотропной терапии гриппа. Антибиотики и химиотерапия. 2021; 66: 5–6: 58–71. doi: 10.24411/0235-2990-2021-66-6-6-58-71.
Логинова С.Я., Борисевич С.В., Максимов В.А. и др. Изучение противовирусной активности триазавирина в отношении возбудителя гриппа А (H5N1). Антибиотики и химиотерапия. 2007. Т. 52. № 11–12. С. 18–20.
Логинова С.Я., Борисевич С.В., Максимов В.А. и др. Лечебная эффективность нового отечественного химиопрепарата Триазавирин в отношении возбудителя гриппа А (H5N1). Антибиотики и химиотерапия. 2011. Т. 56. № 1–2. С. 10–13.
Сологуб Т.В., Токин И.И., Мидикари А.С., Цветков В.В. Сравнительная эффективность и безопасность применения противовирусных препаратов в терапии больных гриппом. Инфекционные болезни. 2017. Т. 15. № 3. С. 25–32.
Деева Э.Г., Киселев О.И., Мельникова Т.И. и др. Новый противовирусный препарат «Триазавирин». Результаты I фазы клинического исследования. Эпидемиология и инфекционные болезни, №5, 2013.С. 20–26.
Киселев О.И., Деева Э.Г., Мельникова Т.И. и др. Новый противовирусный препарат Триазавирин. Результаты II фазы клинического исследования. Вопросы вирусологии. – 2012. – № 6. – С. 9–12.
Токин И.И., Цветков В.В., Голобоков Г.С. Сравнительная клинико-экономическая оценка двух альтернативных схем противовирусной терапии больных гриппом // Журнал инфектологии, 2018, Том 10, № 2, с.110-116.
Э.Г. Деева, В.Л. Русинов, В.Н. Чарушин, О.Н. Чупахин, О.И. Киселев. Противовирусный препарат Триазавирин: от скрининга до клинической апробации // Разработка и регистрация лекарственных средств, 2014, №2(7)
И. Н. Фалынскова, И. А. Ленева, О. В. Макарова, Н. Р. Махмудова, Е. А. Глубокова, Н. П. Каратшова, В. А. Мхитаров, Д. Ш. Джалилова. Оценка эффективности комбинации риамиловира и осельтамивира на модели экспериментальной гриппозной инфекции мышей // Антибиотики и химиотерапия, 2017, 62; 11-12;
I.Leneva, I. Falynskova, N. Makhmudova, E. Glubokova, N. Kartasheva, E. Leonova, N. Mikhailova, I. Shestakova. Effect of Triazavirine on the outcome of a lethal influenza infection and secondary bacterial pneumonia following influenza in mice. Microbiology Independent Journal, V. 4, N. 1, 2017.
К.В. Касьяненко, Н.И. Львов, О.В. Мальцев, К.В. Жданов. Нуклеозидные аналоги в терапии гриппа: история и опыт // Журнал инфектологии, Том 11, № 3, 2019, с.20-26;
Ратникова Л. И. Применение нового отечественного противовирусного препарата в этиотропной терапии гриппа // Экспериментальная и клиническая фармакология, 2018, Том 81 №3, с. 24-28;
Веревщиков В.К., Шемякина Е.К., Сабитов А.У., Бацкалевич Н.А. Современная этиотропная терапия гриппа и ОРВИ у взрослых больных с отягощенной преморбидной патологией // Антибиотики и химиотерапия, 2018, Т. 63, № 7-8;
Веревщиков В.К., Шемякина Е.К., Сабитов А.У., Хаманова Ю.Б. Возможности этиотропной терапии при гриппе и ОРВИ с учетом срока госпитализации больных в стационар и риска развития вторичных осложнений // Антибиотики и химиотерапия, 2019, Т. 64, № 3-4.
Колобухина Л.В., Малышев Н.А., Меркулова Л.Н. и др. Изучение эффективности и безопасности нового противовирусного препарата Ингавирин при лечении пациентов гриппом. Русский Медицинский Журнал. 2008; 22: С. 23–29.
Шишкина Л.Н., Небольсин В.Е., Кабанов А.С. и др. Эффективность Ингавирина in vitro и in vivo в отношении штаммов пандемического вируса гриппа A(H1N1/09)v. Журнал микробиологии, эпидемиологии и иммунобиологии. 2011; 2: С.93-96.
Логинова С.Я., Борисевич С.В., Максимов В.А. и др. Изучение лечебной эффективности нового отечественного препарата Ингавирин в отношении возбудителя гриппа A (H3N2). Антибиотики и химиотерапия. 2008; 53: С.7-8.
Шишкина Л.Н., Небольсин В.Е., Скарнович М.О. и др. Изучение эффективности Ингавирина in vivo в отношении штаммов пандемического вируса гриппа A(H1N1/09)v. Антибиотики и химиотерапия. 2010; 55: С. 45–47.
Lvov DK, Kolobukhina LV, Burtseva EI, et al. The 2015-2016 epidemic season in Russia and the world: Circulation of influenza viruses, trends in incidence, clinical aspects, and treatment algorithm. Ter Arkh. 2016; 88(11): 112-120.
Kolobukhina LV, Merkulova LN, Shchelkanov Miu, et al. Pandemic influenza in Russia: specific features of clinical course and the absence of early etiotropic therapy as a risk factor of severe forms of the disease. Ter Arkh. 2011;83(9):48-53.
Kolobukhina LV, Shchelkanov MIu, Merkulova LN et al. Etiotropic therapy of influenza: lessons from the last pandemic. Vestn Ross Akad Med Nauk. 2011;(5):35-40.
Zarubaev V.V., Garshinina A.V., Kalinina N.A. et al. Activity of Ingavirin (6-[2-(1H-Imidazol-4-yl) ethylamino]-5-oxo-hexanoic Acid) Against Human Respiratory Viruses in in vivo Experiments. Pharmaceuticals. 2011; 4(12): Р.1518-1534.
Зарубаев В.В., Беляевская С.В., Сироткин А.К. и др. Влияние Ингавирина на ультраструктуру и инфекционность вируса гриппа in vitro и in vivo. Вопросы вирусологии. 2011;5: С.21-25.
Ершов Ф. И., Киселев О. И. Интерфероны и их индукторы (от молекул до лекарств). — М.: Гэотар—Медиа, 2005. — 356 с.
Малеев В. В., Киселев О. И., Сологуб Т. В., и др. Использование препаратов «Ингарон» и «Альфарона» в лечении и профилактике гриппа, в том числе птичьего происхождения. Врач. Новое в медицине. - 2006.-С.49-53.
Сологуб Т.В., Голобоков Г.С., Цветков В.В., Токин И.И. Интерферон гамма в терапии гриппа и других респираторные вирусных инфекций. Медицинский совет. 2015. № 7. С. 54–58.
Колобухина Л.В., Меркулова Л.Н., Малышев Н.А. и др. Применение местной интерферонотерапии в комплексном лечении гриппа, осложнённого ангиной. В сб.: Ершов Ф.И., Наровлянский А.Н., ред. Интерферон-2011. М., 2012. С. 174–178.
Сологуб Т.В., Эсауленко Е.В., Деева Э.Г., Йолла И. Гамма-инферферон: обоснование и перспективы применения в инфекционной практике. Медлайн-экспресс. 2006. № 2–3. С. 21–23.
Sologub TV, Tsvetkov VV. Kagocel in the therapy of influenza and acute respiratory viral infections: Data analysis and systematization from the results of preclinical and clinical trials. Ter Arkh. 2017; 89(8): 113-119.
Ershov F.I., Boev B.V., Ershov I.F. Mathematic prognosis of cagocel effectiveness for prophylaxis and therapy of influenza. Zh Mikrobiol Epidemiol Immunobiol. 2014;(5):50-53.
Кареткина Г. Н. Применение индукторов интерферонов для лечения и профилактики гриппа и других острых респираторных вирусных инфекций // Лечащий врач. — 2009.-№9.
Selkova EP, Iakovlev VN, Semenenko TA, Filatov NN, Gotvianskaia TP, Danilina GA, Pantiukhova TN, Nikitina GIu, Tur"ianov MKh (2001). «Evaluation of amyxin effect in prophylaxis of acute respiratory viral infections» (Russian). Zh. Mikrobiol. Epidemiol. Immunobiol. (3): 42–6.
Semenenko T.A., Selkova E.P., Nikitina G.Y., et al. Immunomodulators in the prevention of acute respiratory viral infections. Russ J Immunol. 2002 Jul;7(2):105-114.
Selkova EP, Semenenko TA, Nosik NN, Iudina TI, Amarian MP, Lavrukhina LA, Pantiukhova TN, Tarasova GIu (2001). «[Effect of amyxin--a domestic analog of tilorone--on characteristics of interferon and immune status of man]» (Russian). Zh. Mikrobiol. Epidemiol. Immunobiol. (4): 31– 5.
Калюжин О.В. Тилорон как средство выбора для профилактики и лечения острых респираторных вирусных инфекций. Лечащий врач. - 2013. - №10. - С. 43.
Селькова Е., Волчецкий А., Лапицкая А. Индукторы интерферонов в профилактике и лечении ОРВИ и гриппа. Врач. 2013. № 4. С. 48–54.
Будневский А.В. и др. Анализ комплаенса и эффективности профилактики острых респираторных инфекций у пациентов хронической обструктивной болезнью легких с применением тилорона. Пульмонология. 2016; 26(2): 201–207.
Волчек И.В. Профилактическая и лечебная эффективность амиксина при гриппе и других острых респираторных вирусных инфекциях. TERRA MEDICA. 2003; 1 (29): 17–20.
Ершов Ф.И., Григорян С.С. Рекомендации по применению препарата Амиксин в клинической практике. Пособие для врачей. М., 2007.
Tazulakhova EB1, Parshina OV, Guseva TS, Ershov FI. Russian experience in screening, analysis, and clinical application of novel interferon inducers. J Interferon Cytokine Res. 2001; 21(2): 65-73.5).
Григорян С., Исаева Е., Бакалов В. и др. Амиксин: индукция интерферонов-α, -β, -γ и -λ в сыворотке крови и легочной ткани. Фармакология. 2015; 3:28-34; 207–213.
Охотников С. В., Васильев М. Ю., Поваженко А. А. Иммунологическая реактивность у вахтовых работников в условиях Крайнего Севера и ее коррекция. Медицинская иммунология. 2000; 2 (1): С. 93–96.
Ершов Ф.И., Наровлянский А.Н. Использование индукторов интерферона при вирусных инфекциях. Вопросы вирусологии. 2015; 60 (2): С.5-10.
Савенкова М.С., Савенков М.П. Обоснованный выбор иммуномодулирующих препаратов с противовирусным действием. Фарматека. 2015;11(304): С. 17–22.
Кареткина Г.Н. Применение индукторов интерферонов для лечения и профилактики гриппа и других острых респираторных вирусных инфекций. Лечащий врач. 2009;10: С. 36–40.
Кареткина Г.Н. Грипп и ОРВИ: лечение и профилактика в наступившем эпидемическом сезоне 2015-2016гг. Лечащий врач. 2015;11: С. 46–54.
Бабанов С.А. Индукторы интерферона в лечении и профилактике гриппа и острых респираторных вирусных инфекций. Справочник поликлинического врача. 2012; 11: С. 31–36.
Moore N., Le Parc J.M., van Ganse E. et al. Tolerability of ibuprofen, aspirin and paracetamol for the treatment of cold and flu symptoms and sore throat pain. Int J Clin Pract 2002;56(10):732- 4.
Spivak N.I., Grabchenko N.I., Lazarenko L.N. et al. The antibacterial efficacy of preparations of interferon and its inducers. Mikrobiol Z. 1999; 61(1): P. 32–45.
Лопатин А.С., Свистушкин В.М. Острый риносинусит: этиология, патогенез, диагностика и принципы лечения. Клинические рекомендации. М.: Российское общество ринологов. -2009-26 с.
Oстрый риносинусит. Клинические рекомендации. М-Ростов-на-Дону: Общероссийская общественная организация "Ассоциация врачей общей практики (семейных врачей) Российской Федерации. - 2014-27с.
Захаров К.А., Сурков К.Г., Василюк В.Б., Синенченко А.Г., Волков Г.А., Сухорук А.А., Эсауленко Е.В. Эффективность применения препарата неовир для профилактики заболеваемости острыми респираторными заболеваниями и гриппом в производственном коллективе. Фарматека. 2015. № 11 (304). С. 72-77.
Volkov G.A., Zakharov K.А., Surkov K.G., Vasilyuk V.B., Sinenchenko A.G., Sukhoruk A.A., Esaulenko E.V. The use of low-molecular interferon inducer neovir for prevention of acute respiratory diseases in a production collective. В сборнике: . Материалы II съезда инфекционистов Узбекистана. 2015. С. 201-202.
Antoniol S., Fidouh N., Ghazali A., et al. Diagnostic performances of the Xpert® Flu PCR test and the OSOM® immunochromatographic rapid test for influenza A and B virus among adult patients in the Emergency Department. J Clin Virol. 2018;99-100:5-9.
Дробченко С.Н., Ривец Б., Сэмюэльс Ф. Новые экспресс-тесты для диагностики гриппа. Поликлиника. 2010; 4: С. 18.
Петрова Е.Р., Суховецкая В.Ф., Писарева М.М., Майорова В.Г., Сверлова М.В., Даниленко Д.М., Петрова П.A., Кривицкая В.З., Соминина А.А. Сравнительный анализ эффективности быстрых тестов в диагностике гриппа А и респираторно-синцитиальной вирусной инфекции у детей. Клиническая лабораторная диагностика. 2015; 60(11): 44–49.
Яцышина С.Б., Куличенко Т.В., Артемова И.В., Рыбалка О.Б., Елькина М.Н. Использование иммунохроматографических тестов в алгоритме лабораторной диагностики гриппа. Эпидемиология и инфекционные болезни. Актуальные вопросы №1 / 2018 с. 42–48.
Мальчиков И.А., Аминев Р.М., Рубова С.Р. и др. Сравнительная эффективность методов, применяемых для диагностики гриппа на современном этапе. Дальневосточный журнал инфекционной патологии. 2010;17: С. 8–10.
Hurt A.C. Performance of six influenza rapid tests in detecting human influenza in clinical specimens. J Clin Virol. 2007; 39: P. 132-135.
Громов М.И. Иммуномодуляторы и активаторы репарации в хирургии. Поликлиника. 2009; 3: С. 81–84.
Земсков М.А., Деева Ю.А., Токмаков А.И. и др. Фармакологическая иммунокоррекция в комплексном лечении гнойно-воспалительных заболеваний. Научно-медицинский вестник Центрального Черноземья. 2008; 31: С.23-27.
Путинцева О.В., Артюхов В.Г., Сиделева Н.Н. Влияние препарата Неовир на уровень экспрессии CD3-комплексов Т-лимфоцитами крови доноров при различных сроках инкубации. Современная биология: вопросы и ответы. Материалы I Международной научной конференции. 2012; С. 100–103.
Азнабаева Л.М., Киргизова С.Б. Лекарственная регуляция антилизоцимной активности стафилококков. Современные проблемы науки и образования. 2013;2: С. 46–47.
Фомина М.В., Киргизова С.Б., Азнабаева Л. М., Михайлова Е.А. Новые возможности лекарственных препаратов, используемых в терапии бактериальных инфекций для профилактики бактерионосительства. Вестник Оренбургского государственного университета. 2015;10(185): С.279-281.
Михайлова Е.В., Киргизова С.Б., Миронов А.Ю. Санация стафилококкового бактерионосительства – новые возможности и перспективы. Клиническая лабораторная диагностика. 2015; 60(7): С. 56–57.
Лещенко И.В. Внебольничная пневмония у взрослых: диагностика и лечение в амбулаторных условиях. Фтизиатрия и пульмонология. 2017;3(16):50-63.
Чучалин А.Г., Синопальников А.И., Козлов Р.С. и др. Внебольничная пневмония у взрослых: практические рекомендации по диагностике, лечению и профилактике. Пособие для врачей. М., 2010.
Hayden F. WHO Guidelines on the Use of Vaccines and Antivirals during Influenza. Annex 5- Considerations for the Use of Antivirals during an Influenza pandemic. – Geneva, 2002.
Wilde J.A., McMillan J.A., Serwint J. et al. Effectiveness of influenza vaccine in health care professionals: a randomized trial. JAMA. 1999;281: Р908-913.
Campbell D.S., Rumley M.H. Cost-effectiveness of the influenza vaccine in a healthy, working-age population. J Occup Environ Med. 1997;39: Р.408-414.
Nichol K.L., Lind A., Margolis K.L. et al. The effectiveness of vaccination against influenza in healthy, working adults. N Engl J Med. 1995;333: Р.889-893.
Potter J., Stott D.J., Roberts M.A. et al. Influenza vaccination of health care workers in long-term-care hospitals reduces the mortality of elderly patients. J Infect Dis 1997;175: Р.1-6.
Carman W.F., Elder A.G., Wallace L.A. et al. Effects of influenza vaccination of health-care workers on mortality of elderly people in long-term care: a randomised controlled trial. Lancet 2000;355: Р.93-97.
Kunzel W., Glathe H., Engelmann H. et al. Kinetics of humoral antibody response to trivalent inactivated split influenza vaccine in subjects previously vaccinated or vaccinated for the first time. Vaccine 1996;14: Р.1108-1110.
Nichol K.L., Margolis K.L., Lind A. et al. Side effects associated with influenza vaccination in healthy working adults: a randomized, placebo-controlled trial. Arch Intern Med 1996;156: Р.1546- 1550.
Scheifele D.W., Bjornson G., Johnson J. Evaluation of adverse events after influenza vaccination in hospital personnel. Can Med Assoc J. 1990;142: Р.127-130.
Ельшина Г.А., Тиньков А.Н., Борщук Е.А. и др. Эпидемиологическая и экономическая эффективность вакцинации против гриппа взрослого работоспособного населения вакциной Инфлювак. Эпидемиология и вакцинопрофилактика. 2007; 2(33): С.47-53.
Костинов М.П., Ерофеева М.К., Харит С.М. Эффективность и безопасность вакцинопрофилактики гриппа у разных контингентов. TERRA MEDICA. 2011; 3(2): С. 7–11.
Duque J., Gaga S., Clark D. et al. Knowledge, attitudes and practices of South African healthcare workers regarding the prevention and treatment of influenza among HIV-infected individuals. PLoS One. 2017;12(3): P. e0173983.
Hodgson D., Baguelin M., van Leeuwen E. et al. Effect of mass paediatric influenza vaccination on existing influenza vaccination programmes in England and Wales: a modelling and cost-effectiveness analysis. Lancet Public Health. 2017; 2(2): P.e74-e81.
Coghlan B., Carlson S., Leder K., Dalton C., Cheng A.C.Timing of influenza vaccination in an Australian community-based surveillance system, 2010-2014. Commun Dis Intell Q Rep. 2016; 40(3): P.E347-E350.
Chao A.S., Chang Y.L., Chao A. et al. Seropositivity of influenza A H1NI in mothers and infants following maternal vaccination with trivalent seasonal influenza vaccine after the 2009 pandemic. Taiwan J Obstet Gynecol. 2017; 56(1): P.37-40.
Simpson C.R., Lone N.I., Kavanagh K. et al. Evaluating the effectiveness, impact and safety of live attenuated and seasonal inactivated influenza vaccination: protocol for the Seasonal Influenza Vaccination Effectiveness II (SIVE II) study. BMJ Open. 2017;7(2): P. e014200.
Hayden F.G. Atmar R.L., Schilling M. et al. Use of the selective oral neuraminidase inhibitor oseltamivir to prevent influenza N Engl J Med. 1999;341: Р.1337-1338.
Welliver R. Monto A.S., Carewicz O. et al. Effectiveness of oseltamivir in preventing influenza in household contacts: a randomized conterolled trial. JAMA. 2001;285(6): Р.748-754.
Лыткина И.Н., Малышев Н.А. Профилактика и лечение гриппа и острых респираторных вирусных инфекций среди эпидемиологически значимых групп населения. Леч. Врач. 2010; 10: 65–69.
Позднякова М.Г., Ерофеева М.К., Максакова В.Л. Неспецифическая профилактика гриппа и других острых респираторных вирусных заболеваний. РМЖ. 2011;19 (2): С. 84–88.
Романцов М.Г., Зарубаев В.В., Коваленко А.Л. Грипп A/H1N1 – типичная эмерджентная инфекция. Вопросы терапии и экстренной профилактики. Вестник гос. мед. академии им. И.И. Мечникова. 2009; 2: 168–172.
Н.К. Мазина, И.В. Шешунов и соавт. Клиническая эффективность иммуномодулятора циклоферона (таблетки) при вирусных инфекциях органов дыхания: результаты систематического обзора и метаанализа, Терапевтический архив, 11, 2017, С. 83-91.
С.С. Григорян, Е.И. Исаева, Е.Н. Ветрова Противовирусное действие циклоферона в зараженных вирусом гриппа А (H3N2) культурах клеток, Экспериментальная и клиническая фармакология, 2019, Том 82, №5, С. 36-39.
В.П. Сухинин, В.В. Зарубаев, В.Г. Платонов и соавт. Защитное действие циклоферона при экспериментальной гриппозной инфекции, Вопросы вирусологии, 2000, №5, С. 26-30.
В.В. Зарубаев, М.Г. Романцов Защита от вируса гриппа А/H1N1 (материалы экспериментального исследования, проведенного в НИИ гриппа РАМН), Медико-фармацевтический журнал Парацельс, №7, 2009, С. 10-13.
Исаков В.А., Ерофеева М.К., Коваленко А.Л. и др. Применение таблеток циклоферона в терапии гриппа и ОРЗ, Поликлиника. 2004. № 3. С. 12–14.
Романцов М.Г., Сологуб Т.В., Коваленко А.Л. Циклоферон в лечении и экстренной профилактике респираторных вирусных инфекций и гриппа, Клиническая медицина, 2011, № 1, С. 51–54.
Сологуб Т.В. Циклоферон как средство лечения и экстренной профилактики гриппа и ОРВИ (многоцентровое рандомизированное контрольно-сравнительное исследование), Клиническая медицина, 2009, Том 54, 7-8, С. 30-36.
Ющук Н.Д. и соавт., Применение таблеток циклоферона в терапии гриппа и ОРЗ, Лечащий врач, 2012, №10, С. 64.
Романцов М.Г., Голофеевский С.В. Эффективность циклоферона при лечении ОРВИ и гриппа в период эпидемического подъёма респираторной заболеваемости (2009-2010 гг.). Антибиотики и Химиотерапия, 2010, 55 (1-2), С. 30-35.
Исаков В.А. Эффективность Циклоферона в терапии и профилактике гриппа и ОРЗ, РМЖ: Болезни дыхательных путей. 2011. № 23. С. 1420–1425.
Мазина Н.К., Шешунов И.В., Мазин П.В. Адъювантная энергопротекция реамберином в практике интенсивной терапии и реанимации: эффективность по данным метаанализа (систематический обзор). Анестезиология и реаниматология. 2016; 61(4), С. 314–319.
Картополова Е.В. Оптимизация комплексной терапии гриппа. Вестник ДГМА № 1 (18), 2016, С. 31–34.
Исаков В.А., Водейко Л. П., Каболова И. В., Туркин В. В. Клиническая эффективность реамберина в терапии гриппа. Терапевтический архив, 2010, № 11, С.19−22.
Ратникова Л.И., Картополова Е.В. Влияние патогенетической терапии гриппа на продукцию оксида азота и купирование интоксикационного синдрома. Инфекционные болезни: новости, мнения, обучение, №4 2016, С. 100–103.
Каболова И.В., Днепровская Г.Л., Туркин В.В. Использование реамберина в терапии тяжелого гриппа. Вестник новгородского государственного университета 2005, №32, С.43−45.
Исаков В.А., Архипов Г.С., Коваленко А.Л., Туркин В.В. Терапия вирусных инфекций. Лечащий врач, 2000 №3 С. 57–59
"Временные методические рекомендации "Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 16 (18.08.2022)" (утв. Минздравом России)
Клинические рекомендации «Внебольничная пневмония у взрослых» Москва : Министерство здравоохранения Российской Федерации, 2021. https://cr.minzdrav.gov.ru/schema/654_1
Eccles, R., Turner, R. B. & Dicpinigaitis, P. V. Treatment of Acute Cough Due to the Common Cold: Multi-component, Multi-symptom Therapy is Preferable to Single-Component, Single-Symptom Therapy—A Pro/Con Debate. Lung 194, 15–20 (2016).
Picon PD, Costa MB, da Veiga Picon R, et al. Symptomatic treatment of the common cold with a fixed-dose combination of paracetamol, chlorphenamine and phenylephrine: a randomized, placebo-controlled trial. BMC Infect Dis. 2013;13:556.
Kiran, Mayuresh D., Monali P. Vakharia, Lalit J. Pawaskar, and Shaheen N. Sheikh. 2018. “Efficacy and Safety of a Fixed Dose Combination of Paracetamol, Chlorpheniramine Maleate and Phenylephrine in Treatment of Common Cold: A Phase IV, Open-Labelled, Multi-Centric Study.” International Journal of Basic & Clinical Pharmacology 8 (1): 34.
De Sutter, A. I., van Driel, M. L., Kumar, A. A., Lesslar, O. & Skrt, A. Oral antihistamine-decongestant-analgesic combinations for the common cold. Cochrane Database Syst. Rev. (2012). doi:10.1002/14651858.CD004976.pub3
Овчинников А. Ю. и др. Продуктивный кашель при ОРВИ. Возможности современной терапии //РМЖ. – 2014. – Т. 22. – №. 6. – С. 445–448.
Малявин А.Г. Мифы острого бронхита. Non nocere. 2019; 9:19-24.
Малявин А.Г. Острый бронхит и роль вирусной инфекции при этом заболевании. Non nocere. 2020; 11: 84–93.
Лусс Л. В. Современные взгляды на иммуномодулирующую терапию при респираторных инфекциях у взрослых и детей: преимущества Полиоксидония / Л. В. Лусс // Эффективная фармакотерапия. Аллергология и иммунология. – 2015. – № 2–3 (48). – С. 24–32.
Белан, Э.Б., и А.А. Желтова. «Применение иммуномодуляторов в лечении заболеваний дыхательных путей». ФАРМАТЕКА, вып. 4 (2017 г.). https://pharmateca.ru/ru/archive/article/34670.
Булгакова, В. А. «Иммуномодуляторы для профилактики и лечения острых респираторных инфекций: эффективность азоксимера бромида». Терапевтический архив (архив до 2018 г.) 86, вып. 12 (1 декабрь 2014 г.): 92–97. https://doi.org/10/gg6rsh.
Глушкова, Е. Ф., и Т. Н. Суровенко. «Иммуномодулирующая терапия у пациентов с инфекциями верхних дыхательных путей и ЛОР-органов». Медицинский Совет, вып. 16 (2016 г.). https://doi.org/10/gg6rsn.
Якимова, С.С. «Рациональная фармакотерапия и профилактика гриппа». CONSILIUM MEDICUM, вып. 11 (2011 г.): 28–32.
Варфоломеева, М. И., и Б. В. Пинегин. «Обоснование назначения и применение Полиоксидония в лечении и профилактике ОРВИ». Трудный Пациент 9, вып. 6 (2011 г.). https://www.elibrary.ru/item.asp?id=16921857.
Скачков, М. В. «Безопасность и эффективность Полиоксидония для профилактики ОРЗ у длительно и часто болеющих пациентов». РМЖ 16, вып. 22 (2008 г.). https://www.elibrary.ru/item.asp?id=22934420.
Булгакова, В. А., И. И. Балаболкин, и А. С. Игнатова. «Иммуномодуляция как стратегия профилактики и лечения респираторных инфекций». Consilium Medicum 18, вып. 11 (2016 г.). https://www.elibrary.ru/item.asp?id=28804362.
Зырянов, С. К., О. И. Бутранова, А. В. Ершов, и З. Ш. Манасова. «Эффективность азоксимера бромида в терапии госпитализированных пациентов с внебольничной пневмонией среднетяжелого и тяжелого течения». Медицинский Совет, вып. 18 (2021 г.). https://doi.org/10.21518/2079-701X-2021-18-106-117.
Варфоломеева, М.И., и Н.Х. Сетдикова. «Современные возможности иммуномодулирующей терапии в профилактике и лечении острых респираторных инфекций». Consilium Medicum 17, вып. 3 (2015 г.). https://elibrary.ru/item.asp?id=23209647.
Временные методические рекомендации "Лекарственная терапия острых респираторных вирусных инфекций (ОРВИ) в амбулаторной практике в период эпидемии COVID-19. Версия 2 (16.04.2020). Министерство Здравоохранения Российской Федерации
Овчинников А. Ю. и др. Комплексное лечение острых респираторных заболеваний. Взгляд оториноларинголога на возможности современной фармакотерапии //Фарматека. – 2014. – №. 20. – С. 81-84.
Кирилюк А. А. Особенности клинической фармакологии комбинированных противопростудных лекарственных средств //Вестник фармации. – 2020. – №. 1 (87). – С. 18-36.
Токин И. И., Цветков В. В., Голобоков Г. С. Использование средств патогенетической терапии при гриппе и ОРВИ //Инфекционные болезни. – 2015. – Т. 13. – №. 4. – С. 62-66.
Клячкина И. Л. Лечение кашля при ОРВИ и гриппе //РМЖ. – 2012. – Т. 20. – №. 6. – С. 278-284.
Mitha E. et al. Safety, resistance, and efficacy results from a phase IIIb study of conventional-and double-dose oseltamivir regimens for treatment of influenza in immunocompromised patients //Infectious diseases and therapy. – 2019. – Т. 8. – №. 4. – С. 613-626.
Osterholm M. T. et al. Efficacy and effectiveness of influenza vaccines: a systematic review and meta-analysis //The Lancet infectious diseases. – 2012. – Т. 12. – №. 1. – С. 36-44.
Ramsay L. C. et al. The impact of repeated vaccination on influenza vaccine effectiveness: a systematic review and meta-analysis //BMC medicine. – 2019. – Т. 17. – №. 1. – С. 1-16.
Jackson R. J. et al. Oseltamivir, zanamivir and amantadine in the prevention of influenza: a systematic review //Journal of Infection. – 2011. – Т. 62. – №. 1. – С. 14-25.
Максакова В. Л., Васильева И. А., Ерофеева М. К. Применение препарата «Кагоцел» для лечения и профилактики гриппа и других острых респираторных вирусных инфекций //Медлайн экспресс. – 2009. – Т. 1. – №. 201. – С. 42-46.MLA
Treanor J. J. et al. Intranasally administered interferon as prophylaxis against experimentally induced influenza A virus infection in humans //The Journal of infectious diseases. – 1987. – Т. 156. – №. 2. – С. 379-383.
Розенберг О. А. и др. Сурфактант терапия в комплексном лечении тяжелой двусторонней пневмонии и ОРДС, вызванных вирусом гриппа A/H1N1 //МВ Швечкова и др.//Дело Жизни. – 2016. – №. 2. – С. 10.
Розенберг О.А. Препараты легочного сурфактанта и сурфактанттерапия ОРДС в условиях хирургической реанимации (обзор литературы). Креативная хирургия и онкология. 2019;9(1):50-65. https://doi.org/10.24060/2076-3093-2019-9-1-50-65
Яковлев А. А. и др. Грипп A Н1N1/2009 калифорнияreassortment of vRNAs как медицинская проблема //Вестник Санкт-Петербургского университета. Медицина. – 2010. – №. 3. – С. 45-55.
Athlin S., Lidman C., Lundqvist A., et al. Management of community-acquired pneumonia in immunocompetent adults: updated Swedish guidelines 2017. Infect Dis (Lond) 2018;50(4):247-272.
Boyles T.H., Brink A,, Calligaro G.L., et al. South African guideline for the management of community- acquired pneumonia in adults. J Thorac Dis 2017;9(6):1469-1502.
Metlay J.P., Watere G.W., Long A.C., et al. Diagnosis and Treatment of Adults With Community-acquired Pneumonia. An Official Clinical Practice Guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med 2019;200(7):e45-e67.
Борзанова М.В., Алпенидзе Д.Н., Горелышева Н.Е. Обзор эффективности препаратов интерферона альфа–2b при интраназальном применении. РМЖ. 2012;24:1208.
Алпенидзе Д.Н., Борзанова М.В., Маклакова Е.В. и др. Современные подходы к терапии ОРВИ у взрослых – опыт клинического применения назального спрея интерферона альфа // Справочник поликлинического врача. – 2010. – №.9. – С.19–23.
Васильев А.Н., Дерябин П.Г., Галегов Г.А. Антивирусная активность рекомбинантного интерферона альфа-2b в комбинации с некоторыми антиоксидантами. Антибиотики и Химиотерапия. 2011;56(9-10):27-32.
Методические рекомендации "Грипп и другие ОРВИ в период продолжающейся пандемии COVID-19: профилактика и лечение" (утв. Федеральным медико-биологическим агентством 10 ноября 2022 г.)
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Бабак С. Л. – доцент, профессор кафедры фтизиатрии и пульмонологии лечебного факультета ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России Минздрава России
Горелов А. В. – академик РАН, профессор, заместитель директора по научной работе ФБУН Центральный НИИ эпидемиологии Роспотребнадзора
Зайцев А.А. – д.м.н. профессор ФГКУ «Главный военный клинический госпиталь им. академика Н.Н. Бурденко» главный пульмонолог МО РФ
Зырянов С.К.– д. м. н., профессор, заведующий кафедрой общей и клинической фармакологии ФГАОУ ВО «Российский университет дружбы народов»
Климова Е. А. – д.м.н., профессор кафедры инфекционных болезней и эпидемиологии ФГБОУ ВО «Московский государственный медико-стоматологический университет» им. А.И. Евдокимова Минздрава России
Кравченко И. Э. –д.м.н.. профессор кафедры инфекционных болезней ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России
Лиознов Д. А. – д.м.н., директор ФГБУ НИИ гриппа им. А.А. Смородинцева Минздрава России
Малеев В. В. – академик РАН, д.м.н., профессор, Советник директора по научной работе ФБУН Центральный НИИ эпидемиологии Роспотребнадзора,
Малявин А. Г. – д.м.н., профессор, профессор кафедры фтизиатрии и пульмонологии лечебного факультета ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, руководитель Центра респираторной медицины
Никифоров В.В. –д.м.н., профессор, заведующий кафедрой инфекционных болезней и эпидемиологии ФГБОУ ВО «Российского национального исследовательского медицинского университета им. Н.И. Пирогова» Минздрава России
Новак К.Е. к.м.н. доцент кафедры инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
Попов А.Ф. – д.м.н., профессор, профессор кафедры инфекционных болезней ФГБОУ ВО «Тихоокеанский государственный медицинский университет» МЗ РФ
Пшеничная Н. Ю. – д.м.н., профессор, заместитель директора по клинико-аналитической работе ФБУН Центральный НИИ эпидемиологии Роспотребнадзора
Чуланов В. П. – д.м.н., профессор, заместитель директора по научной работе и инновационному развитию ФГБУ НМИЦ Фтизиопульмонологии и инфекционных болезней МЗ РФ
Эсауленко Е.В., д.м.н., профессор, заведующая кафедрой инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
Усенко Д. В. – д. м. н., руководитель образовательного центра, ведущий научный сотрудник клинического отдела инфекционной патологии ФБУН Центральный НИИ эпидемиологии Роспотребнадзора
Яковлев А. А. – д.м.н., профессор, зав. кафедрой инфекционных болезней, эпидемиологии и дерматовенерологии Санкт-Петербургский государственный университет
Все члены рабочей группы являются членами Национальной ассоциации специалистов по инфекционным болезням имени академика В.И.Покровского (НАСИБ) или Российского научного медицинского общества терапевтов (РНМОТ)
Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория клинических рекомендаций:
1. Врач-инфекционист;
2. Врач-терапевт;
3. Врач-гастроэнтеролог;
4. Врач общей практики;
5. Студенты медицинских ВУЗов, ординаторы, аспиранты.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Определение уровней достоверности доказательств и убедительности рекомендаций для диагностических вмешательств
Таблица П1 – Уровни достоверности доказательности для диагностических вмешательств
УДД | Иерархия дизайнов клинических исследований по убыванию уровня достоверности доказательств от 1 до 5 |
|---|---|
1 | Систематические обзоры исследований с контролем референсным методом1 |
2 | Отдельные исследования с контролем референсным методом |
3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода |
4 | Несравнительные исследования, описание клинического случая |
5 | Имеется лишь обоснование механизма действия или мнение экспертов |
1Общепринятым стандартом КИ диагностических вмешательств является одномоментный дизайн исследования, в котором к каждому включённому пациенту параллельно и в одинаковых условиях применяются исследуемый диагностический метод и референсный метод, являющийся «золотым стандартом» диагностики изучаемого заболевания или состояния, при этом исследуемый и референсный методы должны применяться независимо друг от друга (т.е. исследуемый метод не может быть частью референсного) и должны интерпретироваться исследователем без знания результатов применения другого метода (рекомендуется использовать ослепление)
Таблица П2 – Шкала определения УУР для диагностических вмешательств
УУР | Иерархия дизайнов клинических исследований по убыванию уровня достоверности доказательств от 1 до 5 |
|---|---|
А | Однозначная (сильная) рекомендация (все исследования имеют высокое или удовлетворительное методологическое качеств, их выводы по интересующим исходам являются согласованными) |
В | Неоднозначная (условная) рекомендация (не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
С | Низкая (слабая) рекомендация – отсутствие доказательств надлежащего качества (все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Таблица П3. Возможные комбинации УДД и УУР для диагностических вмешательств
УДД | Критерии определения УУР | Итоговый УУР |
|---|---|---|
1=Наиболее достоверные доказательства: систематические обзоры исследований с контролем референсным методом | Одновременное выполнение двух условий: 1. Все исследования имеют высокое или удовлетворительное методологическое качество; 2. Выводы исследований по интересующим исходам являются согласованными* | А |
Выполнение хотя бы одного из условий: 1. Не все исследования имеют высокое или удовлетворительное методологическое качество; 2. Выводы исследований по интересующим исходам не являются согласованными* | В | |
Выполнение хотя бы одного из условий: 1. Все исследования имеют низкое методологическое качество; 2. Выводы исследований по интересующим исходам не являются согласованными* | С | |
2=Отдельные исследования с контролем референсным методом | Одновременное выполнение двух условий: 1. Все исследования имеют высокое или удовлетворительное методологическое качество; 2. Выводы исследований по интересующим исходам являются согласованными* | А |
Выполнение хотя бы одного из условий: 1. Не все исследования имеют высокое или удовлетворительное методологическое качество; 2. Выводы исследований по интересующим исходам не являются согласованными* | В | |
Выполнение хотя бы одного из условий: 1. Все исследования имеют низкое методологическое качество; 2. Выводы исследований по интересующим исходам не являются согласованными* | С | |
3=Исследования без последовательного контроля референсным методом или исследования с референсным методом не являющимся независимым от исследуемого метода | Выполнение хотя бы одного из условий: 1. Не все исследования имеют высокое или удовлетворительное методологическое качество; 2. Выводы исследований по интересующим исходам не являются согласованными* | В |
Выполнение хотя бы одного из условий: 1. Все исследования имеют низкое методологическое качество; 2. Выводы исследований по интересующим исходам не являются согласованными* | С | |
4=Несравнительные исследования, описание клинического случая | С | |
5=Наименее достоверные доказательства: имеется лишь обоснование механизма действия или мнение экспертов | С | |
*Если оценивается одно КИ, то данное условие не учитывается
Определение уровня достоверности доказательств и убедительности рекомендаций для лечебных, реабилитационных, профилактических вмешательств
Таблица П4 - Уровни достоверности доказательности для лечебных, реабилитационных, профилактических вмешательств
УДД | Иерархия дизайнов клинических исследований по убыванию уровня достоверности доказательств от 1 до 5 |
|---|---|
1 | Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
2 | Отдельные рандомизированные клинические исследования и системные обзоры исследований любого дизайна за исключением рандомизированных клинических исследований с применением мета-анализа |
3 | Нерандомизированные сравнительные исследования, в том числе когортные исследования |
4 | Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай-контроль» |
5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнения экспертов |
Таблица П5–Шкала определения уровни убедительности рекомендаций для лечебных, реабилитационных, профилактических вмешательств
УУР | Расшифровка |
|---|---|
А | Однозначная (сильная) рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
В | Неоднозначная (условная) рекомендация (не все критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выходы по интересующим исходам не являются согласованными) |
С | Низкая (слабая) рекомендация – отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций
Клинические рекомендации обновляются каждые 3 года.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
Федеральный закон от 17 сентября 1998г. №157-ФЗ «Об иммунопрофилактике инфекционных заболеваний».
Федеральный закон Российской Федерации от 29 ноября 2010г. №326-ФЗ «Об обязательном медицинском страховании в Российской Федерации».
Федеральный закон от 21 ноября 2011г. №323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации».
Приказ Минздравсоцразвития России от 9 августа 2005г. №494 «О порядке применения лекарственных средств у больных по жизненным показаниям».
Приказ Минздравсоцразвития России от 27 декабря 2011г. №1664н «Об утверждении номенклатуры медицинских услуг».
Приказ Минздравсоцразвития России от 31 января 2012г. № 69н «Об утверждении Порядка оказания медицинской помощи взрослым больным при инфекционных заболеваниях».
Приказ Минздрава России от 20 декабря 2012г. №1183н «Об утверждении Номенклатуры должностей медицинских работников и фармацевтических работников»
Приказ Минздрава России от 07 октября 2015г. №700н «О номенклатуре специальностей специалистов, имеющих высшее медицинское и фармацевтическое образование».
Приказ Минздрава России от 17 декабря 2015г. № 1024н «О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы».
Приказ Минздрава России от 10 мая 2017г. №203н «Об утверждении критериев оценки качества медицинской помощи».
СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней». XXXIV. Профилактика гриппа и других острых респираторных вирусных инфекций (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
Соответствие клинических синдромов патогенетическим механизмам и морфологическому субстрату
№ | Синдром | Клинические проявления | Патогенетическое обоснование | Морфологический субстрат |
|---|---|---|---|---|
11 | Интоксикация (постоянно при эпидемическом гриппе, в межэпидемический период может быть выражена минимально или отсутствовать) | Выраженная слабость, снижение аппетита, головная боль, боли в глазных яблоках, миалгия, артралгия | «Цитокиновый шторм» - гиперпродукция провоспалительных цитокинов на фоне недостаточности противовоспалительных. Наиболее типична их гиперпродукция пораженными вирусом альвеолярными макрофагами. Рассматривается и как неспецифическая системная воспалительная реакция. | Неравномерное полнокровие, обратимые альтеративные изменения изменения клеток в различных органах. Характерные вирусиндуцированные изменения в респираторных отделах легких. |
22 | Лихорадка (постоянно при эпидемическом гриппе, в межэпидемический период может быть выражена минимально или отсутствовать) | Повышение температуры тела до 38,5 – 40°С | Типовой патологический процесс, возникающий при действии пирогенов, вследствие перестройки центров терморегуляции на новый уровень функционирования. | Отсутствует |
33 | Трахеит (очень характерен для тяжелого течения в любой период). В межэпидемический период возможен назофарингит. | Ощущение “першения”, “саднения”, “жжения” за грудиной (по ходу трахеи), мучительный сухой кашель. | Гематогенное или контактное распространение вируса на эпителий респираторных путей. Вирус гриппа тропен к мерцательному эпителий респираторного тракта. | Вирус гриппа, размножаясь в клетках цилиндрического эпителия, вызывает их альтернативные изменения. Некроз эпителия может приводить к вирусемии и способствует присоединению вторичной бактериальной микробиоты, прежде всего стафилокков. |
44 | Геморрагический (только в эпидемический период, частота существенно варьирует) | Носовые кровотечения, геморрагические высыпания. При тяжелом и нарастающем токсикозе уже в течение 1—2 суток заболевания может развиться бронхит с геморрагическим компонентом | Обусловлен тропностью вируса гриппа к сосудистой стенке, приводящее к нарушению тонуса, эластичности, проницаемости сосудистой стенки, ломкости капилляров. Нарушение микроциркуляции. | Распространенные полнокровие и кровоизлияния (чаще диапедезные, петехиальные) в легких и других органах. |
55 | Диспепсический (только в некоторые эпидемические периоды)
| Диарея - отличительная особенность гриппа, вызванного вирусом гриппа A/H1N1 pdm09. Больные отмечают дискомфорт в животе, диарея развивается на 2–3-и сутки от начала болезни. Характер стула водянистый, без патологических примесей, с частотой 2–11 раз/сут. Функция кишечника, как правило, нормализуется через 1-2 сутки. Снижение аппетита до анорексии, тошнота иногда рвота, боли в животе чаще в эпигастральной области. | Тропизм некоторых штаммов вируса гриппа к эпителию тонкой кишки | При гистологическом изучении отмечаются цитопролиферативные изменения энтероцитов, в которых вирус может определяться различными методами. Отмечается их увеличение в объеме и бледное окрашивание. В лимфатическом аппарате кишечника вначале определяется умеренная гиперплазия дендритных клеток. В дальнейшем энтероциты, иногда на значительном протяжении, некротизируются. |
66 | Менингеальный (обычно в эпидемический период, частота в разные годы варьирует) | Головная боль, рвота, легкая ригидность затылочных мышц, иногда «затуманенное» сознание | Существование нейротропных штаммов, способных индуцировать появление в ликворе антител и интерферона | Наличие в ЦНС: - гемо- и ликвородинамических изменений -прямого цитопатического действия вируса на головной мозг (прежде всего в мягких мозговых оболочках и хориодальных сплетениях). |
77 | Иммунодефицит (может развиваться как в эпидемический, так и межэпидемический периоды) | Легкость развития «постгриппозных» осложнений, прежде всего пневмоний. | Способность многих штаммов вируса гриппа к цитопатическому эффекту в центральных и периферических органах иммуногенеза | Выявление вируса (его РНК или антигенов) в органах иммуногенеза, наряду с характерными цитопатическими изменениями.
|
88 | Респираторный дистресс-синдром: или тяжелое альвеолярное повреждение (характерно для некоторых эпидемических периодов). | Острая дыхательная недостаточность развивается в течение нескольких дней, часов или даже минут. Сначала человек испытывает одышку, обычно сопровождаемую быстрым поверхностным дыханием. Кожа покрывается пятнами или синеет. Затем наступает летальный исход. | Сочетание воспалительных, некробиотических , десквамативных, дистрофических изменений, циркуляторных расстройств и регенераторных процессов в легких | Альвеолы, заполненные отечной серозно-геморрагической жидкостью, содержащей фибрин, мононуклеары и нейтрофильные гранулоциты, с формированием “гиалиновых мембран”, гипоксемию, приводящих к летальному исходу. |
Критерии оценки тяжести течения гриппа
Таблица 1. Критерии оценки тяжести течения гриппа
Признак | Характеристика признака | |||
|---|---|---|---|---|
Легкая степень тяжести | Средняя степень тяжести | Тяжелая степень тяжести | Очень тяжелая степень | |
Лихорадка, проявления интоксикации | Лихорадка до 38,50С
| Лихорадка от 38,6 до 39,50С
| Лихорадка более 39,60С. Сильная головная боль, ломота во всем теле, бессонница, анорексия, (отсутствие аппетита). | Лихорадка свыше 40,00С. Бурно развивающиеся симптомы интоксикации. |
Пульс и систолическое артериальное давление (САД) | Пульс – менее 90 уд/мин. САД - 110 мм рт. ст. и выше | Пульс 90 – 120 уд/мин. САД менее 110 мм рт. ст. | Пульс более 120 уд/мин, нередко аритмичен. САД менее 90 мм рт. ст. Тоны сердца глухие. | Пульс более 120 уд/мин, нередко аритмичен. САД менее 90 мм рт. ст. Тоны сердца глухие. |
ЧДД | 16 – 23 | Более 24 | Более 28 | Более 28 |
Выраженность катаральных явлений | Умеренная головная боль и катаральные явления (умеренный кашель, насморк) | Сухой мучительный кашель с болями за грудиной | Болезненный, мучительный кашель, боли за грудиной | Катаральные явления не выражены |
Тошнота | Отсутствует | Возможна | Часто | Возможна |
Рвота | Отсутствует | Отсутствует | Возможна | Часто |
Осложнения | Нет | Имеются | Имеются | Неотложные состояния. Геморрагический токсический отек легких и смертельный исход от дыхательной и сердечно-сосудистой недостаточности |
Менингеальный синдром | Отсутствует | Отсутствует | Возможен | Часто |
Нарушение сознания | Отсутствует | Отсутствует | Оглушение, сопор | Сопор, кома |
Судороги | Отсутствуют | Отсутствуют | Возможны | Возможны |
Бред, делирий | Отсутствуют | Отсутствуют | Возможны | Часто |
Длительность заболевания | До 6 дней | 6-8 дней | 9 дней и более | Молниеносное течение |
Таблица 2. Классификация гриппа по тяжести в соответствии с рекомендациями ВОЗ [62]
Форма тяжести | Клинические признаки |
|---|---|
Неосложненный грипп | |
Легкая Среднетяжелая Тяжелая
| Лихорадка, кашель, боль в горле, насморк, головная боль, мышечные боли, недомогание, отсутствие одышки. У больного могут присутствовать некоторые или все из перечисленных симптомов. |
Симптомы поражения желудочно-кишечного тракта: диарея или рвота, отсутствие признаков дегидратации организма. | |
Наличие у некоторых больных атипичных симптомов или атипичной клинической картины гриппа (например, отсутствие лихорадки). | |
Осложненный грипп | |
Тяжелая / Крайне тяжелая | Одышка, гипоксия и / или рентгенологические признаки поражения нижних дыхательных путей (пневмония), признаки поражения ЦНС (энцефалопатия, энцефалит), тяжелая дегидратация организма, наличие вторичных осложнений: почечная недостаточность, полиорганная недостаточность, септический шок. Наличие иных осложнений: рабдомиолиз, миокардиты |
Обострение хронических заболеваний: бронхиальной астмы, ХОБЛ, хронического гепатита, почечной недостаточности, сахарного диабета, сердечно-сосудистых заболеваний (например, застойной сердечной недостаточности) | |
Любые другие заболевания, требующие госпитализации (например, бактериальная пневмония) | |
Любые другие заболевания и симптомы, указывающие на прогрессирование заболевания | |
Правила забора материала для лабораторного исследования на грипп [75]
Мазки со слизистой оболочки носоглотки и задней стенки ротоглотки берут после полоскания полости рта кипяченой водой комнатной температуры. Если полость носа заполнена слизью, перед процедурой рекомендуется провести высмаркивание. В течение 6-ти часов перед процедурой нельзя использовать медикаменты, орошающие носоглотку или ротоглотку и препараты для рассасывания во рту. У взрослых мазки со слизистой носоглотки берут сухим стерильным назофарингеальным аппликатором-щеткой стерильной на пластиковой палочке или сухим стерильным зондом из полистирола с вискозным тампоном (предпочтительно для сбора биологического материала для ПЦР с целью последующей изоляции культуры вируса). Зонд вводят легким движением по наружной стенке носа на глубину 2 – 3 см до нижней раковины, слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину, делают вращательное движение и удаляют вдоль наружной стенки носа. Общая глубина введения зонда должна составлять примерно половину расстояния от ноздри до ушного отверстия (не менее 5 см).
Мазки из ротоглотки берут сухим стерильным зондом из полистирола с вискозным тампоном вращательными движениями с поверхности миндалин, небных дужек и задней стенки ротоглотки, прижимая язык пациента шпателем.
Мокроту (при глубоком откашливании) и эндотрахеальный аспират собирают в стерильные одноразовые герметично закрывающиеся контейнеры натощак после чистки зубов и полоскания полости рта водой. Пациента просят сделать несколько глубоких вдохов с задержкой дыхания на несколько секунд, затем с силой выдохнуть, что способствует появлению продуктивного кашля и очищению верхних дыхательных путей от мокроты. Для получения эндотрахеального аспирата затем присоединяют мукус-экстрактор через трубку-переходник к отсосу катетер вводится в глотку через полость рта, в результате чего провоцируется кашлевой рефлекс и проводится извлечение трахеального содержимого через стерильный катетер (6 – 7 размера) с помощью отсоса. Для получения индуцированной мокроты рекомендуется использовать упражнения дыхательной гимнастики и вибрационный массаж грудной клетки. Наибольшего эффекта достигают с помощью ингаляций с использованием гипертонического раствора хлорида натрия.
Аутопсийный материал забирают стерильным инструментом из зоны поврежденной ткани объемом 1-3 см3 инструментами (индивидуально для каждого органа).
Каждый образец помещают в отдельную транспортную емкость со стабилизирующей средой и/или в пробирку с транспортной средой. Материал для исследования должен быть нативным (без фиксации формалином).
Алгоритм клинической сортировки пациентов с ГПЗ
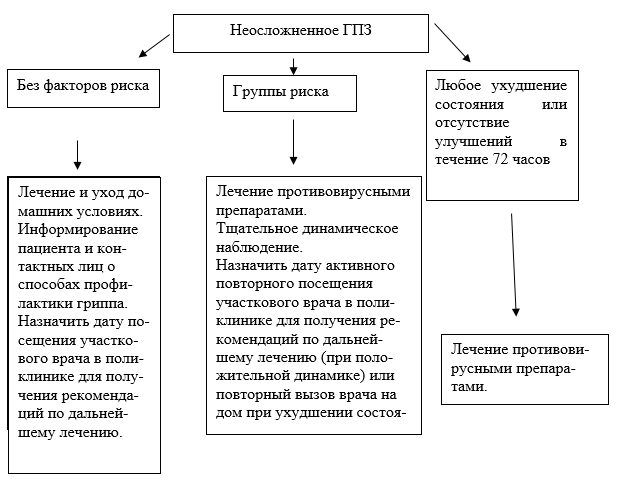
Показания для перевода в отделение реанимации при установленном диагнозе гриппа (достаточно одного из критериев)
начальные проявления и клиническая картина быстропргрессирующей острой дыхательной недостаточности;
нарастающая и выраженная одышка;
цианоз;
ЧД более 30 в минуту;
SpO2 менее90%;
артериальное давление АДсист. менее 90 мм.рт.ст.;
шок (мраморность конечностей, акроцианоз, холодные конечности, симптом замедленного сосудистого пятна (более 3 сек.), лактат более 2 ммоль/л);
дисфункция центральной нервной системы (оценка по щкале комы Глазго менее 15 баллов);
острая почечная недостаточность (мочеотделение менее 0,5 мл/кг/ч в течение 1 часа или повышение уровня креатинина в два раза от нормального значения);
печёночная дисфункция (увеличение содержания билирубина выше 20 мкмоль/л в течение 2-х дней или повышение уровня трансаминаз в два раза и более от нормы);
коагулопатия (число тромбоцитов менее 100 тыс/мкл или их снижение на 50% от наивысшего значения в течение 3-х дней)
Транспортировка пациента осуществляется силами профильного отделения после консультации и в сопровождении врача – анестезиолога - реаниматолога.
Принципы респираторной поддержки при ОРДС, вызванном вирусом гриппа
Респиратор
Респиратор для проведения респираторной поддержки больным с ОРДС, вызванном гриппом А(H1N1)pdm09, должен удовлетворять следующим условиям:
• Современный респиратор для интенсивной терапии;
• Автоматическая компенсация объема вследствие компрессии газа в контуре (или измерение в Y-трубке);
• Экран, позволяющий наблюдать за кривыми давление/время и поток/время;
• Мониторинг давления плато;
• Измерение «внутреннего» РЕЕР или общего РЕЕР (PEЕPtot = PЕEP + PЕEPi).
Для транспорта больных внутри стационара рекомендуется использование транспортных респираторов последнего поколения, позволяющих проводить точную настройку РЕЕР, дыхательного объема (VT) и фракции кислорода во вдыхаемой смеси (FiO2) и оснащенных системами мониторинга, близкими к таковым у реанимационных респираторов.
Режимы вентиляции
Так как ни один режим респираторной поддержки не продемонстрировал свое преимущество при ОРДС, рекомендован выбор вентиляции, контролируемой по объему, вспомогательно-контролируемый режим (VAC). Данный режим наиболее распространенный в современных ОРИТ и наиболее простой. Также рекомендован выбор постоянного инспираторного потока (прямоугольный профиль), 50-60 л/мин и использование инспираторной паузы 0,2-0,3 сек (для возможности проведения мониторинга давления плато).
Дыхательный
объем
Рекомендовано использование дыхательного объема (VT) 6 мл/кг должной массы тела. Должная масса тела рассчитывается по формуле:
• Должная масса тела = X + 0,91 (рост в см - 152,4).
Женщины: X = 45,5. Мужчины: X = 50.
В таблице ниже представлен рекомендуемый VT в зависимости от пола пациента и его роста:
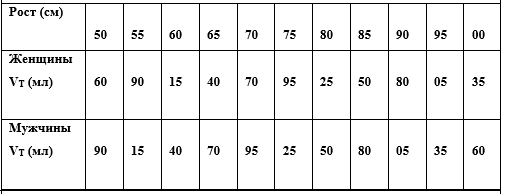
Частота дыхания
Рекомендовано использование частоты дыхания 20–35/мин, которая регулируется для достижения PCO2, при котором pH находится в диапазоне от 7,30 до 7,45. Изначально, выбирается частота дыхания, позволяющая добиться той же минутной вентиляции, что и до перевода больного на протективную вентиляцию (с VT 6 мл/кг)
РЕЕР
Рекомендован выбор такого уровня РЕЕР, чтобы добиться давления плато в диапазоне 28-30 см Н2O, и при этом, общее РЕЕР (PEEP + PEEPi) не превышало бы 20 см Н2O, и не было бы ниже 5 см Н2O, т.е. РЕЕР должно быть в диапазоне 5–20 см Н2O.
Изначально РЕЕР выставляется на 8–10 см Н2O, затем повышается на 2 см Н2O каждые 3-5 мин для достижения нужного давления плато (28-30 см Н2O).
При использовании VT 6 мл/кг, такой уровень PEEP обычно не вызывает нарушения гемодинамики. При возникновении артериальной гипотензии во время повышения уровня РЕЕР, рекомендована временная отсрочка повышения РЕЕР до восполнения объема циркулирующей жидкости.
FiO2
Рекомендовано использование FiO2 30–100%, которая регулируется для достижения показателей оксигенации:
• 88 % ≤ SpO2 ≤ 95 %
• 55 мм рт ст. ≤ PaO2 ≤ 80 мм рт ст.
Седация - миорелаксация
При тяжелых формах ОРДС в течение первых 24–48 часов рекомендована глубокая седация и начальная миорелаксация больного. Затем необходима адаптация седации для достижения частоты дыхания ≤ 35/мин, хорошей синхронизации больного с респиратором.
Маневры рекрутирования
Маневры рекрутирования не могут быть рекомендованы для всех больных ОРДС. Маневры рекрутирования рекомендованы при развитии тяжелой десатурации во время случайного отсоединения контура от респиратора или аспирации секрета. Так как проведение данной процедуры может осложниться гемодинамическими нарушениями и баротравмой, маневры рекрутирования должны проводиться врачом (не медсестрой!), под тщательным клиническим контролем параметров больного. Методика проведения маневра: CPAP 40 cм H2O в течение 40 сек или транзиторное повышение PЕEP (для достижения давления плато = 40 cм H2O).
Трахеальная аспирация
Для предотвращения дерекрутирования и десатурации рекомендовано проведение аспирации трахеобронхиального секрета без отсоединения контура от респиратора. Для защиты медицинского персонала рекомендовано использование закрытой системы аспирации.
Увлажнение вдыхаемой смеси
Метод выбора кондиционирования воздушной смеси в данной ситуации – тепловлагообменник (ТВО). При развитии респираторного ацидоза необходимо заменить ТВО на увлажнитель / подогреватель медицинского кислорода.
(для уменьшения инструментального мертвого пространства).
Фильтрация выдыхаемой смеси
Фильтр между экспираторным контуром и экспираторным блоком респиратора позволяет защитить окружающую среду от вирусной контаминации. Фильтр абсолютно необходим, если используется увлажнитель / подогреватель медицинского кислорода. Установка экспираторного фильтра позволяет избежать контаминации окружающей среды, независимо от способа увлажнения. В случае использования увлажнителя-подогревателя данный фильтр должен меняться регулярно, т.к. происходит его заполнение влагой.
Прональная позиция
• Сеансы от 6 до 18 часов;
• Оценка эффективности: PO2 через 1 и 4 часа;
• Фиксация интубационной трубки и катетеров во время смены позиции;
• Профилактика пролежней +++;
• Изменение положения головы и рук каждый час.
Ингаляционный NO
• Начальная доза: 5 ppm;
• Подача газа в инспираторную часть дыхательного контура
• Использование привычных систем доставки для отделения;
• Оптимально – синхронизация с инсуффляцией (OptiNO®);
• Ежедневные попытки снижения дозы (2.5, 1, 0.5 ppm).
Отлучение от респиратора
Рекомендовано ежедневное проведение сеанса спонтанной вентиляции у больных, которые соответствуют следующим критериям:
• Отсутствие потребности в вазопрессорах;
• Отсутствие седации;
• Выполнение простых команд.
Рекомендовано проводить сеанс спонтанной вентиляции в режиме: PS 7 cм H2O, PЕEP = 0, FiO2 от 21 до 40%. Максимальная продолжительность сеанса – 2 часа, при плохой переносимости спонтанной вентиляции необходимо его немедленное прекращение. При хорошей переносимости сеанса спонтанной вентиляции больному показана экстубация. Дифференциальная диагностика гриппа и других ОРВИ
Признаки
Нозологическая форма ОРВИ
Птичий грипп
Сезонный грипп
ТОРС*
Пара-грипп
РС-инфек-ция**
Аденови-русная инфекция
Ринови-русная инфек-ция
Возбудитель
Вирус гриппа А (H5N1)
Вирусы гриппа: 3 серотипа (А, В, С)
Короновирус SARS
Вирусы пара-гриппа:5 серотипов (1-5)
Респира-торно-синтици-альный вирус: 1 серотип
Аденови-русы: 49 серотипов (1-49)
Ринови-русы: 114 сероти-пов (1-114)
Инкубационный период
1-7 сут., в среднем 3 сут.
От несколь-ких часов до 1,5 суток
2-7 суток, иногда до 10 суток
2-7 сут, чаще 3- 4 сут
3-6 сут
4-14 сут
23 сут
Начало
Острое
Острое
Острое
Постепенное
Постепенное
Постепенное
Острое
Течение
Острое
Острое
Острое
Подост-рое
Подострое, иногда затяжное
Затяжное,
волнообразное
Острое
Ведущий
клинический
синдром
Инток-сикация
Интокси-кация
Дыхате-льная
недоста-точность
Катаральный
Катаральный,
дыхательная
недостаточность
Катараль-ный
Катара-льный
Выражен-ность
интоксикации
Сильная
Сильная
Сильно
выражен-ная
Слабая или умерен-ная
Умерен-ная или слабая
Умерен-ная
Слабая
Длительность
интоксикации
7-12 сут
2-5 сут
5-10 сут
1-3 сут
2-7 сут
8-10 сут
1-2 сут
Температура
тела
38°С и выше
Чаще 39°С и выше, но может быть субфебрильная
38°С и выше
37-38°С, может длительно сохраняться
Субфебрильная,
иногда
нормальная
Фебрильная или субфебрильная
Нормальная
или
субфебрильная
Катаральные
проявления
Отсутствуют
Умеренно
выражены,
присоединяются
позднее
Умеренно выражены, экссудация слабая
Выражены с первого дня течения заболевания. Осиплость голоса
Выражены
постепенно
нарастают
Сильно выражены с первого дня течения заболевания
Выражены с первого дня течения заболевания.
Ринит
Отсутствует
Затруднение носового дыхания, заложенность носа. Серозные, слизистые или
Возможен в начале заболевания
Затруднение
носового
дыхания,
заложенность
носа
Заложенность
носа,
необильное серо
зное отделяемое
Обильное
слизисто-
серозное
отделяемое,
резкое затруднение
носового
дыхания
Обильное
серозное
отделяемое,
носовое
дыхание затруднено или отсутствует
Кашель
Выраженный
Сухой, мучительный, надсадный, с болями за грудиной, на 3 сут. влажный, до 7-10 сут. течения заболевания
Сухой, умеренно выраженный
Сухой, лающий может сохранятся длительное время (иногда до 12-21 сут)
Сухой приступообразн ый (до 3 нед.), сопровождающи йся болями за грудиной
Влажный
Сухой, першение в глотке
Изменения
слизистых
оболочек
Отсутствуют
Слизис-тая оболочка глотки и миндалин синюш-ная, умеренно гиперемирована; инъекция сосудов.
Слабая или умерен-ная гипере-мия слизис-тых оболочек
Слабая или умерен-ная гипере-мия зева, мягкого неба, задней стенки глотки
Слабая
Гипере-мия
слизис-тых оболочек
Умерен-ная гиперемияотечность, гиперплазия фолликул миндалин и задней стенки глотки
Слабая
гиперемия
слизис-тых
оболочек
Физикальные
признаки
поражения
легких
Со 2-3-х сут течения заболевания
Отсутствуют, при наличии бронхита — сухие рассеянные хрипы
С 3-5-х сут течения заболевания часто выявляют признаки интерстициальной пневмо-нии
Отсутствуют
Рассеянные сухие и редко влажные среднепу-зырчатые хрипы, признаки пневмо-нии
Отсутствуют. При наличии бронхита — сухие, рассеянные хрипы.
Отсутствуют
Ведущий
синдром
респираторных
поражений
Нижний
респираторный
синдром
Трахеит
Бронхит, острый респираторный дистресс синдром
Ларингит, ложный круп выявляют крайне редко
Бронхит,
бронхиолит,
возможен
бронхоспазм
Ринофа-рингокон ъюнкти-вит или тонзиллит
Ринит
Увеличение
лимфатических
узлов
Отсутствует
Отсутствует
Отсутствует
Заднешейные, реже - подмышечные лимфатические лимфоузлы увеличены и умеренно болезненные
Отсутствует
Может быть полиаденит
Отсутствует
Увеличение печени и селезенки
Возможно
Отсутствует
Выявляют
Отсутствует
Симптомы
токсического
гепатита
Выражено
Отсутствует
Поражение глаз
Отсутствует
Инъекция сосудов склер
Редко
Отсутствует
Отсутствует
Конъюнктивит,
кератоконъюнктивит
Инъекция сосудов склер, век, слезотечение, конъюнктивит
Поражение других органов
Диарея, возможно поражение печени, почек, лейко-, лимфо-, тромбоцитопения
Отсутствует
Часто в начале заболевания развивается диарея
Отсутствует
Отсутствует
Может быть экзантема, иногда диарея
Отсутствует
* ТОРС – тяжелый острый респираторный синдром
** РС-инфекция – инфекция, вызванная респираторно-синцитиальным вирусом
Приложение Б. Алгоритмы действий врача
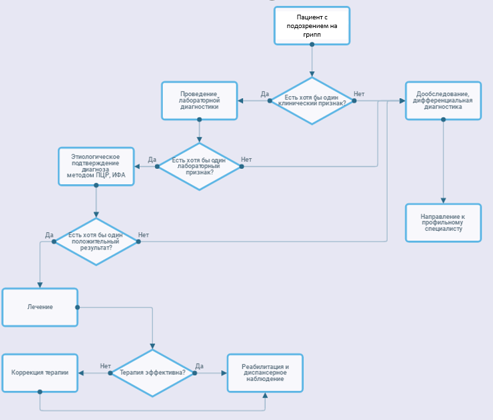
Приложение В. Информация для пациента
Грипп – острое вирусное заболевание, пик заболеваемости которым приходится на осеннее-зимний период.
Источник гриппозной инфекции является больной человек со стертыми или явными формами болезни. Путь передачи – воздушно-капельный. Максимально заразным человек является впервые дни заболевания, когда вирус с каплями слизи во время чихания и кашля начинает выделяться во внешнюю среду.
Грипп начинается остро с резкого подъема температуры до 380С и выше, с сухим кашлем или першением в горле, и сопровождается симптомами общей интоксикации: ознобом, болями в мышцах, головной болью (лобная область, область надбровных дуг), болью в глазных яблоках; насморк обычно начинается спустя 3 дня после снижения температуры тела. Кашель сопровождаться болью за грудиной. Грипп может протекать тяжело и представлять угрозу жизни человека. Тяжелое течение гриппа сопровождается поражением нижних дыхательных путей с развитием пневмонии и (или) признаками дыхательной недостаточности: появляется одышка или затрудненное дыхание в покое, цианоз носогубного треугольника. При тяжелых формах гриппа могут развиваться отек легких, сосудистый коллапс, отек мозга, геморрагический синдром, присоединяться вторичные бактериальные осложнения.
Помните, что симптомы гриппа не так уж и безобидны, как кажется на первый взгляд. Поэтому при этом заболевании важно не заниматься самолечением, а обратиться к врачу и выполнять все его назначения. Тогда с большой вероятностью заболевание пройдет без осложнений.
Как не заболеть гриппом:
• мыть руки как можно чаще, рекомендуется использование дезинфицирующих салфеток или кожного антисептика;
• избегать контакта лица, особенно носа, рта и глаз, с грязными и даже чистыми руками, другими объектами;
• при кашле, чихании прикрывать рот и нос одноразовыми салфетками, которые после использования нужно выбрасывать;
• сократить время пребывания в местах массового скопления людей и в общественном транспорте;
• избегать контактов с лицами, имеющими признаки заболевания;
• носить медицинскую маску. Маску необходимо менять каждые 4 часа;
• осуществлять влажную уборку в помещениях несколько раз в день, обеспечить проветривание и увлажнение воздуха;
• вести здоровый образ жизни (полноценный сон, сбалансированное питание, физическая активность).
В целях повышения устойчивости организма к респираторным вирусам, в первую очередь, к вирусам гриппа, как мера неспецифической профилактики, могут использоваться различные препараты и средства, повышающие иммунитет. Профилактические лекарственные препараты можно принимать только по рекомендации врача! В случаях появления признаков инфекционного заболевания необходимо немедленно обратиться к врачу за квалифицированной медицинской помощью.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Шкала ком Глазго
Название на русском языке: Шкала ком Глазго
Оригинальное название: Glasgow Coma Scale
Источник: Teasdale G.M., Jennett В., 1974
Пирадов М.А., Супонева Н.А., Рябинкина Ю.В., Гнедовская Е.В., Ильина К.А., Юсупова Д.Г. и др. Шкала комы Глазго (Glasgow Coma Scale, GCS): лингвокультурная адаптация русскоязычной версии.Журнал им. Н.В. Склифосовского Неотложная медицинская помощь. 2021;10(1):91–99. https://doi.org/10.23934/2223-9022-2021-10-1-91-99
Тип: шкала оценки
Содержание:
Признак | Баллы |
|---|---|
1. Открывание глаз: |
|
спонтанное | 4 |
на вербальную стимуляцию | 3 |
на боль | 2 |
нет реакции | 1 |
2. Вербальная реакция: |
|
соответствующая | 5 |
спутанная | 4 |
бессвязные слова | 3 |
нечленораздельные звуки | 2 |
нет реакции | 1 |
3. Двигательная реакция: |
|
выполняет словесные команды | 6 |
локализует боль | 5 |
реакция одергивания в ответ на боль | 4 |
сгибание верхних конечностей в ответ на боль (поза декортикации) | 3 |
разгибание верхних конечностей в ответ на боль | 2 |
нет реакции | 1 |
Ключ:
Начальная оценка по шкале Глазго коррелирует с тяжестью церебрального повреждения и прогнозом.
Шкала состоит из трёх тестов, оценивающих реакцию открывания глаз, а также речевые и двигательные реакции. За каждый тест начисляется определённое количество баллов. В тесте открывания глаз от 1 до 4, в тесте речевых реакций от 1 до 5, а в тесте на двигательные реакции от 1 до 6 баллов.
Таким образом, шкала Глазго является важным критерием для оценки уровня сознания. Каждая отдельная реакция оценивается в баллах, а уровень сознания выражается суммой баллов по каждому из параметров. Самая низкая оценка — 3 балла, а самая высокая — 15 баллов. Оценка 8 баллов и ниже определяется как кома.
Оценка по шкале 3-5 баллов прогностически крайне неблагоприятна, особенно если она сочетается с широкими зрачками и отсутствием окуловестибулярного рефлекса.
Приложение Г2. Шкала SOFA
Оригинальное название: Sequential Organ Failure Assessment (SOFA)
Русское название: шкала SOFA
Источник (официальный сайт разработчиков, публикация с валидацией): https://pubmed.ncbi.nlm.nih.gov/29443733/
Tee Y.S., Fang H.Y., Kuo I.M., Lin Y.S., Huang S.F., Yu M.C. Serial evaluation of the SOFA score is reliable for predicting mortality in acute severe pancreatitis. Medicine (Baltimore). 2018 Feb; 97(7):e9654. doi: 10.1097/MD.0000000000009654.
Тип (подчеркнуть):
- шкала оценки
- индекс
- вопросник
Назначение: определение органной недостаточности
Показатели | Оценка | ||||
|---|---|---|---|---|---|
0 | 1 | 2 | 3 | 4 | |
PaO2/FiO2 | >400 | 300-399 | 200-299 | 100-199 | <100 |
Количество тромбоцитов в мл | >150000 | 100000-149000 | 50000 - 99999 | 20000-49999 | <20000 |
Билирубин сыворотки | <20 | 20-32 | 33-101 | 102-204 | >204 |
Среднее артериальное давление | >70 мм рт. ст. | <70 мм рт. ст. без использования вазопрессоров | Использование любой дозы добутамина. Допамин <5 мкг/кг в минуту | Допамин 5-15 мкг/кг в минуту. Адреналин <0.1 мкг/кг в минуту. Норадреналин <0.1 мкг/кг в минуту. | Допамин> 15 мкг/кг в минуту. Адреналин> 0.1 мкг/кг в минуту. Норадреналин> 0.1 мкг/кг в минуту. |
Оценка тяжести комы по Глазго | 15 | 13-14 | 10-12 | 6-9 | 3-5 |
Креатинин сыворотки или диурез | Креатинин сыворотки <100 мкмоль/л | Креатинин сыворотки 100-170 мкмоль/л | Креатинин сыворотки 171-299 мозоль/л | Креатинин сыворотки 300-400 мкмоль/л. Суточный диурез 200 - 499 мл | Креатинин сыворотки > 440 мкмоль/л. Суточный диурез < 200 мл |
Ключ (интерпретация):
PaO2 в мм. рт. ст. FiO2 от 0.21 до 1.00.
Адренергические средства применялись хотя бы 1 час. Дозировка – в мкг/кг в минуту.
0 – наиболее оптимальный параметр, 4 – наиболее аномальный параметр.
Информация должна собираться и оцениваться 1 раз в сутки в течение всего времени нахождения пациента в отделении интенсивной терапии.
Среднее (системное) артериальное давление рассчитывается по формуле: САД = (АДсист + АДдиаст) / 3.
SOFA индекс равен сумме всех шести показателей.
Комментарии • 0
Чтобы оставить комментарий, пожалуйста, войдите или зарегистрируйтесь.