Топический рофумпласт одобрен для лечения псориаза
Местная терапия остается основным вариантом лечения для большинства людей с бляшечным псориазом, распространенным иммуноопосредованным заболеванием кожи. Хотя болезнь может поражать любую область тела, бляшки в определенных областях, таких как лицо, локти и колени, гениталии и интертригинозные области (области кожного контакта), представляют собой уникальные проблемы лечения. В результате людям с псориазом часто назначают несколько местных препаратов для разных областей, что усложняет схему лечения[1].
Рофлумиласт — селективный ингибитор фосфодиэстеразы 4 (ФДЭ4), первый одобренный препарат этой группы для лечения псориаза. Пероральный рофлумиласт (Далиресп) одобрили в 2011 году для лечения хронической обструктивной болезни легких. Он не имеет побочных эффектов, которые характерны для стероидов, и его можно использовать длительно[2].
Данные исследований
Одобрение FDA основывается на данных двух рандомизированных, двойных слепых контролируемых испытаний III фазы. Пациентов разделили на две группы, одна из которых получала крем рофлумиласт, а другая — крем-плацебо. Первичной конечной точкой был успех Глобальной оценки исследователя (investigator's global assessment, IGA), определяемый как чистая или почти чистая кожа с улучшением по крайней мере на 2 балла по сравнению с исходным уровнем и улучшением по крайней мере на 2 балла по шкале IGA по сравнению с исходным уровнем через 8 недель. В качестве вторичных исходов оценивали изменения индекса PASI-75 (Psoriasis Area and Severity Index — индекс распространенности и тяжести псориаза), уменьшение зуда в зависимости от наихудшего результата, изменение баллов по числовой рейтинговой шкале зуда (The Worst Itch Numeric Rating Scale, WI-NRS) и дневник симптомов псориаза.
Через 8 недель у 42,4% и 37,5% участников, использовавших крем рофлумиласт, наблюдалось улучшение по сравнению с 6,1% и 6,9% в группах плацебо (P < 0,0001 для обоих исследований). Также положительная динамика при использовании псориаза наблюдалась и для вторичных показателей — индекса PASI-75, WI-NRS и дневника симптомов.
В исследованиях 72% и 68% пациентов, получавших рофлумиласт, достигли конечной точки I-IGA через 8 недель по сравнению с 14% и 17% пациентов, получавших плацебо (P < 0,0001 для обоих исследований). Ко 2-й неделе испытания у некоторых участников, получавших рофлумиласт в обоих исследованиях, уменьшился зуд. Через 8 недель среди пациентов с оценкой ≥4 баллов по WI-NRS на исходном уровне у 67% и 69% пролеченных участников наблюдалось снижение показателя WI-NRS не менее чем на 4 балла по сравнению с 26% и 33% участников групп плацебо (P < 0,0001 для обоих исследований).
Побочные эффекты и безопасность
В целом большинство пациентов хорошо переносили применение рофлумиласта. Были сообщения о диарее (3%), головной боли (2%), бессоннице (1%), тошноте (1%), боли в месте нанесения (1%), инфекциях верхних дыхательных путей (1%) и инфекциях мочевыводящих путей (1%). Но авторы исследования отметили, что эти явления встречались и в контрольной группе. Распространенность симптомов представлена на рис. 1.
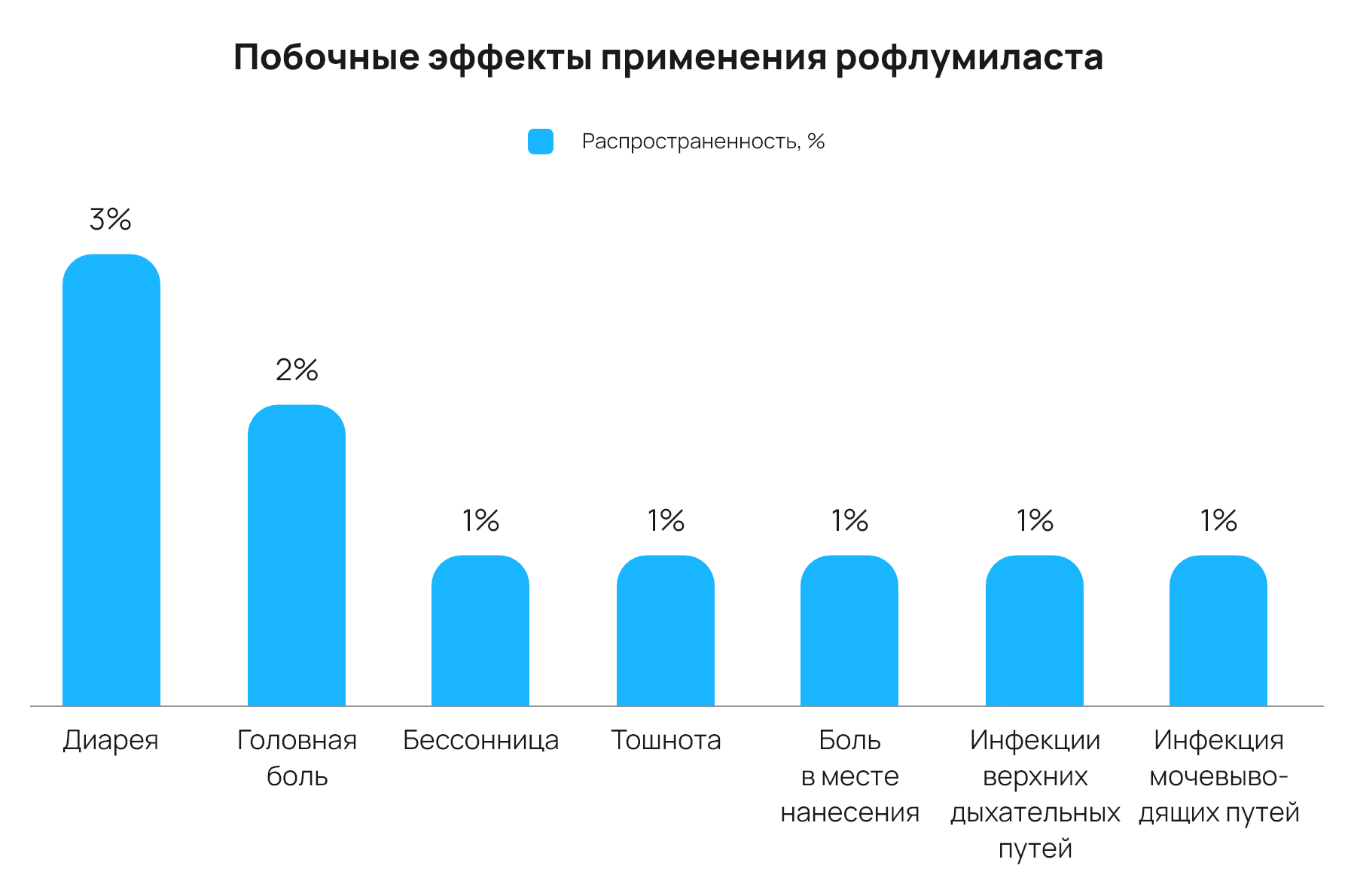
Выводы
- Рофлумиласт — ингибитор ФДЭ4, который может использоваться для лечения бляшечного псориаза с поражением интертригинозных областей.
- ФДЭ4 — фермент, усиливающий воспаление и снижающий уровень противовоспалительных медиаторов, и ингибирование ФДЭ4 может прервать некоторые воспалительные реакции, ответственные за симптомы псориаза, как и при других состояниях, таких как атопический дерматит .
- У пациентов наблюдалось существенное улучшение симптомов при применении рофлумиласта по сравнению с группой плацебо.

Доступ к комментариям ограничен 😔
Чтобы посмотреть комментарии других врачей и поделиться своим мнением, пожалуйста, войдите на Medpoint