Федеральные клинические рекомендации по диагностике и лечению крапивницы. – М.: Российская ассоциация аллергологов и клинических иммунологов, 2015. – 34 с.
Zuberbier T, Abdul Latiff AH, Abuzakouk M, et al. The international EAACI/GA²LEN/EuroGuiDerm/APAAACI guideline for the definition, classification, diagnosis, and management of urticaria. Allergy. 2022; 77(3):734-766. doi:10.1111/all.15090
Bracken SJ, Abraham S, MacLeod AS. Autoimmune Theories of Chronic Spontaneous Urticaria. Front Immunol. 2019; 10:627. Published 2019 Mar 29. doi:10.3389/fimmu.2019.00627
Maurer M, Altrichter S, Schmetzer O, Scheffel J, Church MK, Metz M. Immunoglobulin E-Mediated Autoimmunity. Front Immunol. 2018;9:689. Published 2018 Apr 9. doi:10.3389/fimmu.2018.00689
Kolkhir P, Church MK, Weller K, Metz M, Schmetzer O, Maurer M. Autoimmune chronic spontaneous urticaria: What we know and what we do not know. J Allergy Clin Immunol. 2017;139 (6):1772-1781.e1. doi:10.1016/j.jaci.2016.08.050
Vonakis BM, Vasagar K, Gibbons SP Jr, et al. Basophil FcepsilonRI histamine release parallels expression of Src-homology 2-containing inositol phosphatases in chronic idiopathic urticaria. J Allergy Clin Immunol. 2007;119 (2):441-448. doi:10.1016/j.jaci.2006.09.035
Luquin E, Kaplan AP, Ferrer M. Increased responsiveness of basophils of patients with chronic urticaria to sera but hypo-responsiveness to other stimuli. Clin Exp Allergy. 2005;35 (4):456-460. doi:10.1111/j.1365-2222.2005.02212.x
Gibbs BF, Räthling A, Zillikens D, Huber M, Haas H. Initial Fc epsilon RI-mediated signal strength plays a key role in regulating basophil signaling and deactivation. J Allergy Clin Immunol. 2006;118(5):1060-1067. doi:10.1016/j.jaci.2006.07.022
Maurer M, Church MK, Gonçalo M, Sussman G, Sánchez-Borges M. Management and treatment of chronic urticaria (CU). J Eur Acad Dermatol Venereol. 2015;29(3):16-32. doi:10.1111/jdv.13198
Greenberger PA. Chronic urticaria: new management options. World Allergy Organ J. 2014;7 (1):31. doi:10.1186/1939-4551-7-31.
Bernstein JA, Lang DM, Khan DA, et al. The diagnosis and management of acute and chronic urticaria: 2014 update. J Allergy Clin Immunol. 2014; 133 (5):1270-1277. doi:10.1016/j.jaci.2014.02.036
Pite H, Wedi B, Borrego LM, Kapp A, Raap U. Management of childhood urticaria: current knowledge and practical recommendations. Acta Derm Venereol. 2013; 93 (5):500-508. doi:10.2340/00015555-1573
Maurer M, Weller K, Bindslev-Jensen C, et al. Unmet clinical needs in chronic spontaneous urticaria. A GA²LEN task force report. Allergy. 2011; 66 (3):317-330. doi:10.1111/j.1398-9995.2010.02496.x
Fricke J, Ávila G, Keller T, et al. Prevalence of chronic urticaria in children and adults across the globe: Systematic review with meta-analysis. Allergy. 2020; 75 (2):423-432. doi:10.1111/all.14037
Saini S, Shams M, Bernstein JA, Maurer M. Urticaria and angioedema across the ages. J Allergy Clin Immunol Pract. 2020;8 (6):1866–1874. doi:10.1016/j.jaip.2020.03.0302–6.
Goldstein S, Gabriel S, Kianifard F, Ortiz B, Skoner DP. Clinical features of adolescents with chronic idiopathic or spontaneous urticaria: review of omalizumab clinical trials. Ann Allergy Asthma Immunol. 2017; 118 (4):500–504. doi:10.1016/j.anai.2017.02.0035.
Curto-Barredo L, Pujol RM, Roura-Vives G, Gimenez-Arnau AM. Chronic urticaria phenotypes: clinical differences regarding triggers, activity, prognosis and therapeutic response. Eur J Dermatol. 2019;29(6):627–635. doi:10.1684/ejd.2019.3674 6.
Netchiporouk E, Sasseville D, Moreau L, et al. Evaluating comorbidities, natural history, and predictors of early resolution in a cohort of children with chronic urticaria. JAMA Dermatol. 2017;153(12):1236–1242. doi:10.10 01/jamadermatol.2017.3182
Kaplan AP. Clinical practice. Chronic urticaria and angioedema. N Engl J Med. 2002;346(3):175-179. doi:10.1056/NEJMcp011186
Caffarelli C, Paravati F, El Hachem M, et al. Management of chronic urticaria in children: a clinical guideline. Ital J Pediatr. 2019;45(1):101. doi: 10.1186/s13052-019-0695-x.
Toubi E, Kessel A, Avshovich N, et al. Clinical and laboratory parameters in predicting chronic urticaria duration: a prospective study of 139 patients. Allergy. 2004;59(8):869-873. doi: 10.1111/j.1398-9995.2004.00473.x.
Schoepke N, Doumoulakis G, Maurer M. Diagnosis of urticaria. Indian J Dermatol. 2013;58(3):211-218. doi:10.4103/0019-5154.110831
Намазова-Баранова Л.С. Аллергия у детей: от теории к практике. М.: Союз педиатров. России.2010–2011. 668 с.
Nettis E, Foti C, Ambrifi M, et al. Urticaria: recommendations from the Italian Society of Allergology, Asthma and Clinical Immunology and the Italian Society of Allergological, Occupational and Environmental Dermatology. Clin Mol Allergy. 2020;18:8. doi:10.1186/s12948-020-00123-8
Metz M, Altrichter S, Buttgereit T, et al. The Diagnostic Workup in Chronic Spontaneous Urticaria-What to Test and Why. J Allergy Clin Immunol Pract. 2021;9(6):2274-2283. doi:10.1016/j.jaip.2021.03.049
Kolkhir P, André F, Church MK, Maurer M, Metz M. Potential blood biomarkers in chronic spontaneous urticaria. Clin Exp Allergy. 2017;47(1):19-36. doi: 10.1111/cea.12870.
Altrichter S, Fok JS, Jiao Q, et al. Total IgE as a Marker for Chronic Spontaneous Urticaria. Allergy Asthma Immunol Res. 2021;13(2):206-218. doi:10.4168/aair.2021.13.2.206,
Fok JS, Kolkhir P, Church MK, Maurer M. Predictors of treatment response in chronic spontaneous urticaria. Allergy. 2021;76(10):2965-2981. doi:10.1111/all.14757
Kolkhir P, Altrichter S, Asero R, et al. Autoimmune Diseases Are Linked to Type IIb Autoimmune Chronic Spontaneous Urticaria. Allergy Asthma Immunol Res. 2021;13(4):545-559. doi:10.4168/aair.2021.13.4.545,
Cornillier H, Giraudeau B, Munck S, et al. Chronic spontaneous urticaria in children - a systematic review on interventions and comorbidities. Pediatr Allergy Immunol. 2018;29(3):303-310. doi:10.1111/pai.12870
Spickett G. Urticaria and angioedema. J R Coll Physicians Edinb. 2014;44(1):50-54. doi:10.4997/JRCPE.2014.112
Kolkhir P, Balakirski G, Merk HF, Olisova O, Maurer M. Chronic spontaneous urticaria and internal parasites--a systematic review. Allergy. 2016;71(3):308-322. doi:10.1111/all.12818
Minciullo PL, Cascio A, Gangemi S. Association between urticaria and nematode infections. Allergy Asthma Proc. 2018;39(2):86-95. doi:10.2500/aap.2018.38.4104
Fedorova OS, Fedotova MM, Zvonareva OI, et al. Opisthorchis felineus infection, risks, and morbidity in rural Western Siberia, Russian Federation. PLoS Negl Trop Dis. 2020;14(6):e0008421. doi:10.1371/journal.pntd.0008421.
Sayasone S, Odermatt P, Phoumindr N, et al. Epidemiology of Opisthorchis viverrini in a rural district of southern Lao PDR. Trans R Soc Trop Med Hyg. 2007;101(1):40-47. doi:10.1016/j.trstmh.2006.02.018
Antiparasitic treatment recommendations. A practical guide to clinical parasitology. Editor: Andreas Neumayr. Publisher: Tredition, ISBN: 3734508223. 2016. p. 173
Ataseven A, Durmaz K, Ozer I, Dursun R. Gallstones at chronic spontaneous urticaria patients: A retrospective clinical study. Dermatol Ther. 2020;33(2):e13212. doi:10.1111/dth.13212
Minciullo PL, Cascio A, Barberi G, Gangemi S. Urticaria and bacterial infections. Allergy Asthma Proc. 2014;35(4):295-302. doi:10.2500/aap.2014.35.3764
Imbalzano E, Casciaro M, Quartuccio S, et al. Association between urticaria and virus infections: A systematic review. Allergy Asthma Proc. 2016;37(1):18-22. doi:10.2500/aap.2016.37.3915
Sugrañes-Montalván A, Barreto-Suárez E, Nicolau-Pestana E, Quesada-Leyva L. Relación entre infección por Helicobacter pylori y urticaria crónica [Relation between Helicobacter pylori infection and chronic urticaria]. Rev Alerg Mex. 2017;64(4):396-402. doi:10.29262/ram.v64i4.283
Kim HJ, Kim YJ, Lee HJ, et al. Systematic review and meta-analysis: Effect of Helicobacter pylori eradication on chronic spontaneous urticaria. Helicobacter. 2019;24(6):e12661. doi:10.1111/hel.12661
Maurer M, Magerl M, Ansotegui I, et al. The international WAO/EAACI guideline for the management of hereditary angioedema-The 2017 revision and update. Allergy. 2018;73(8):1575-1596. doi:10.1111/all.13384
aballero T, Baeza ML, Cabañas R, et al. Consensus statement on the diagnosis, management, and treatment of angioedema mediated by bradykinin. Part II. Treatment, follow-up, and special situations [published correction appears in J Investig Allergol Clin Immunol. 2012;22(2):3 p following 153]. J Investig Allergol Clin Immunol. 2011;21(6):422-443.
Cicardi M, Aberer W, Banerji A, et al. Classification, diagnosis, and approach to treatment for angioedema: consensus report from the Hereditary Angioedema International Working Group. Allergy. 2014;69(5):602-616. doi:10.1111/all.12380
Bowen T, Cicardi M, Farkas H, et al. 2010 International consensus algorithm for the diagnosis, therapy and management of hereditary angioedema. Allergy Asthma Clin Immunol. 2010;6(1):24. doi:10.1186/1710-1492-6-24
Agostoni A, Aygören-Pürsün E, Binkley KE, et al. Hereditary and acquired angioedema: problems and progress: proceedings of the third C1 esterase inhibitor deficiency workshop and beyond. J Allergy Clin Immunol. 2004;114(3 Suppl):S51-S131. doi:10.1016/j.jaci.2004.06.047
Peroni A, Colato C, Schena D, Girolomoni G. Urticarial lesions: if not urticaria, what else? The differential diagnosis of urticaria: part 1. Cutaneous diseases. J Am Acad Dermatol. 2010;62:541–555. doi: 10.1016/j.jaad.2009.11.686
Niu XL, Zhu LL, Shi MH, et al. Association of positive and negative autologous serum skin test responses with clinical features of chronic spontaneous urticaria in Asian patients: A systematic review and meta-analysis. Exp Ther Med. 2019;17(4):2603-2613. doi: 10.3892/etm.2019.7266.
Kulthanan K, Subchookul C, Hunnangkul S, Chularojanamontri L, Tuchinda P. Factors Predicting the Response to Cyclosporin Treatment in Patients With Chronic Spontaneous Urticaria: A Systematic Review. Allergy Asthma Immunol Res. 2019;11(5):736-755. doi:10.4168/aair.2019.11.5.736
George M, Balachandran C, Prabhu S. Chronic idiopathic urticaria: comparison of clinical features with positive autologous serum skin test. Indian J Dermatol Venereol Leprol. 2008;74(2):105-108. doi:10.4103/0378-6323.39690
Chronic spontaneous urticaria: Standard management and patient education David A Khan (last updated: Dec 21, 2022). URL: https://www.uptodate.com/contents/chronic-spontaneous-urticaria-standard-management-and-patient-education?search=urticaria&source=search_result&selectedTitle=2~150&usage_type=default&display_rank=2
Cicardi M, Bellis P, Bertazzoni G, et al. Guidance for diagnosis and treatment of acute angioedema in the emergency department: consensus statement by a panel of Italian experts. Intern Emerg Med. 2014;9(1):85-92. doi: 10.1007/s11739-013-0993-z.
Depetri F, Tedeschi A, Cugno M. Angioedema and emergency medicine: From pathophysiology to diagnosis and treatment. Eur J Intern Med. 2019;59:8-13. doi: 10.1016/j.ejim.2018.09.004.
Adeyeni TA, Domack A, Britt C. What Is the Role of Laryngoscopy in Angioedema Isolated to the Lips, Without Laryngeal Symptoms? Laryngoscope. 2020;130(12):2740-2741. doi: 10.1002/lary.28664
Weller K, Groffik A, Magerl M, et al. Development, validation, and initial results of the Angioedema Activity Score. Allergy. 2013;68(9):1185-1192. doi:10.1111/all.12209
Shikiar R, Harding G, Leahy M, Lennox RD. Minimal important difference (MID) of the Dermatology Life Quality Index (DLQI): results from patients with chronic idiopathic urticaria. Health Qual Life Outcomes. 2005;3:36. doi:10.1186/1477-7525-3-36
Prosty C, Gabrielli S, Mule P, et al. Validation of the Urticaria Control Test (UCT) in Children With Chronic Urticaria. J Allergy Clin Immunol Pract. 2022;10(12):3293-3298.e2. doi:10.1016/j.jaip.2022.07.037
Młynek A, Zalewska-Janowska A, Martus P, Staubach P, Zuberbier T, Maurer M. How to assess disease activity in patients with chronic urticaria?. Allergy. 2008;63(6):777-780. doi:10.1111/j.1398-9995.2008.01726.x
Patruno C, Napolitano M, Ferrucci S, et al. Four-week Urticaria Activity Score-7 as a Useful Patient-reported Outcome to Assess Chronic Spontaneous Urticaria: A Multicentre Study Evaluation of Adherence and Patients" Perspective. Acta Derm Venereol. 2019;99(10):903-904. doi: 10.2340/00015555-3231
Caffarelli C, Paravati F, El Hachem M, et al. Management of chronic urticaria in children: a clinical guideline. Ital J Pediatr. 2019;45(1):101. doi: 10.1186/s13052-019-0695-x
Е. Ю. Борзова, C.О. Салугина. Актуальные вопросы дифференциальной диагностики крапивницы. Эффективная фармакотерапия. Аллергология и иммунология. 2017;7(1): 34-44.
Soter N.A. Chronic urticaria as a manifestation of necrotizing venulitis. N Engl J Med 1977; 296: 1440—1442.
Данилычева И.В., Борзова Е.Ю., Ильина Н.И. Уртикарный васкулит. От диагностики к лечению. Российский аллергологический журнал. 2012;5(1):71–76.
Brodell LA, Beck LA. Differential diagnosis of chronic urticaria. Ann Allergy Asthma Immunol. 2008;100(3):181-215. doi:10.1016/S1081-1206(10)60438-3
Махнева Н. В. Современный взгляд на диагностику и лечение буллезных дерматозов. Международный журнал прикладных и фундаментальных исследований. 2011;9:15–17.
Банченко Г.В., Флейшер Г.М., Горин А.А. Опыт лечения многоформной экссудативной эритемы. Медицинский алфавит. 2013;1(1):44–46.
Patel S, Patel R, Draikiwicz S, Capitle E. Peripheral T-cell lymphoma: a challenging mimicker of angioedema and urticaria. Ann Allergy Asthma Immunol. 2015;115(2):94-95. doi:10.1016/j.anai.2015.06.013
Brockow K. Urticaria pigmentosa. Immunol Allergy Clin North Am. 2004;24(2):287-vii. doi:10.1016/j.iac.2004.01.002
Халиулин Ю.Г. Мастоцитоз: клинические проявления, методы диагностики и тактика ведения пациентов. Лечащий врач. 2012;8:83–89
Мухин Н., Моисеев C., Попова Е., и др. Поздние проявления Лаймской болезни. Врач. 2006;5:35–38
Кочергин Н., Никитина Е., Цыкин А. Некоторые особенности дерматозов беременных. Врач. 2010;1:51–55
Новиков Д.К., Сергеев Ю.В., Новиков П.Д., Сергеев А.Ю. Побочные аллергические реакции на медикаменты в дерматологии. Иммунопатология, аллергология и инфектология. 2003;3:45–57.1
Foer D, Buchheit KM, Gargiulo AR, Lynch DM, Castells M, Wickner PG. Progestogen Hypersensitivity in 24 Cases: Diagnosis, Management, and Proposed Renaming and Classification. J Allergy Clin Immunol Pract. 2016;4(4):723-729. doi:10.1016/j.jaip.2016.03.003
Антонова О.В., Трофимов П.Н., Белоусова И.Э., Самцов А.В. Ретикулярный эритематозный муциноз. Вестник дерматологии и венерологии. 2014;5:96–99
Kolkhir P, Pogorelov D, Olisova O, Maurer M. Comorbidity and pathogenic links of chronic spontaneous urticaria and systemic lupus erythematosus--a systematic review. Clin Exp Allergy. 2016;46(2):275-287. doi:10.1111/cea.12673
Хамаганова И.В. Трудности диагностики различных форм красной волчанки. Клиницист. 2006;1: 64–68
Кузьмина Н.Н., Салугина C.О., Федоров E.C. Аутовоспалительные заболевания и синдромы у детей: Учебно-методическое пособие. М.: ИМА-ПРЕСС, 2012.
Barron K., Athreya B., Kastner D. Periodic fever syndromes and other inherited autoinflammatory diseases // Textbook of pediatric rheumatology. Ed. by J.T. Cassidy, R.E. Petty. 7th ed. Elsevier Saunders, 2015. p. 609–641.
Toplak N, Frenkel J, Ozen S, et al. An international registry on autoinflammatory diseases: the Eurofever experience. Ann Rheum Dis. 2012;71(7):1177-1182. doi:10.1136/annrheumdis-2011-200549
Simon A, Asli B, Braun-Falco M, et al. Schnitzler"s syndrome: diagnosis, treatment, and follow-up. Allergy. 2013;68(5):562-568. doi:10.1111/all.12129
De Castro F.R., Masouye I., Winkelmann R.K., Saurat J.H. Urticarial pathology in Schnitzler’s (hyper-IgM) syndrome. Dermatology. 1996;193(2):94–99
Знаменская Л.Ф., Осокина Д.Е., Вавилов А.М. Синдром Свита. Вестник дерматологии и венерологии. 2008;2:94–96
Butterfield J.H. Flushing and urticarial syndromes presenting as anaphylaxis // Anaphylaxis and hypersensitivity reactions. Ed. by M. Castells. Springer, 2010. P. 271–284.
Петер Г. Хегер. Детская дерматология. М.: Издательство Панфилова/Бином. Лаборатория знаний, 2013. — 634 с
Аллергология и иммунология (Практические рекомендации для педиатров). Под ред. А.А. Баранова и Р.М. Хаитова. М.: Союз педиатров России, 2020. 512 с
Hocqueloux L, Guinard J, Buret J, Causse X, Guigon A. Do penicillins really increase the frequency of a rash when given during Epstein-Barr Virus primary infection?. Clin Infect Dis. 2013;57(11):1661-1662. doi:10.1093/cid/cit553
Dibek Misirlioglu E, Guvenir H, Ozkaya Parlakay A, et al. Incidence of Antibiotic-Related Rash in Children with Epstein-Barr Virus Infection and Evaluation of the Frequency of Confirmed Antibiotic Hypersensitivity. Int Arch Allergy Immunol. 2018;176(1):33-38. doi:10.1159/000481988
Kowalski ML, Woessner K, Sanak M. Approaches to the diagnosis and management of patients with a history of nonsteroidal anti-inflammatory drug-related urticaria and angioedema. J Allergy Clin Immunol. 2015;136(2):245-251. doi:10.1016/j.jaci.2015.06.021
Shakouri A, Compalati E, Lang DM, Khan DA. Effectiveness of Helicobacter pylori eradication in chronic urticaria: evidence-based analysis using the Grading of Recommendations Assessment, Development, and Evaluation system. Curr Opin Allergy Clin Immunol. 2010;10(4):362-369. doi:10.1097/ACI.0b013e32833c79d7
Ishaq S, Nunn L. Helicobacter pylori and gastric cancer: a state of the art review. Gastroenerol Hepatol Bed Bench 2015;8(l1):6-14
Arik Yilmaz E, Karaatmaca B, Sackesen C, et al. Parasitic Infections in Children with Chronic Spontaneous Urticaria. Int Arch Allergy Immunol. 2016;171(2):130-135. doi: 10.1159/000450953
Zuberbier T, Chantraine Kess S, Hartmann K, Czarnetzki BM. Pseudoallergen-free diet in the treatment of chronic urticaria – a prospective study. Acta Derm Venereol 1995; 75:484-487
Cornillier H, Giraudeau B, Samimi M, et al. Effect of Diet in Chronic Spontaneous Urticaria: A Systematic Review. Acta Derm Venereol. 2019;99(2):127-132. doi:10.2340/00015555-3015
Nettis E, Colanardi MC, Ferrannini A, Tursi A. Sodium benzoate-induced repeated episodes of acute urticaria/angio-oedema: randomized controlled trial. Br J Dermatol. 2004;151(4):898-902. doi:10.1111/j.1365-2133.2004.06095.x
Akoglu G, Atakan N, Cakır B, Kalayci O, Hayran M. Effects of low pseudoallergen diet on urticarial activity and leukotriene levels in chronic urticaria. Arch Dermatol Res. 2012;304(4):257-262. doi:10.1007/s00403-011-1203-3
Son JH, Chung BY, Kim HO, Park CW. A Histamine-Free Diet Is Helpful for Treatment of Adult Patients with Chronic Spontaneous Urticaria. Ann Dermatol. 2018;30(2):164-172. doi:10.5021/ad.2018.30.2.164
Sánchez-Pérez S, Comas-Basté O, Veciana-Nogués MT, Latorre-Moratalla ML, Vidal-Carou MC. Low-Histamine Diets: Is the Exclusion of Foods Justified by Their Histamine Content?. Nutrients. 2021;13(5):1395.. doi:10.3390/nu13051395
Аллергология. Федеральные клинические рекомендации. главные редакторы: акад. РАН Р.М. Хаитов, проф. Н.И. Ильина. М.: «Фармарус Принт медиа». 2014, 126 с.
Zuberbier T, Abdul Latiff AH, Abuzakouk M, et al. The international EAACI/GA²LEN/EuroGuiDerm/APAAACI guideline for the definition, classification, diagnosis, and management of urticaria. Allergy. 2021. doi: 10.1111/all.15090.
100.Beissert S, Ständer H, Schwarz T. UVA rush hardening for the treatment of solar urticaria. J Am Acad Dermatol. 2000;42(6):1030-1032. doi:10.1016/s0190-9622(00)90299-8
101.Kring Tannert L, Stahl Skov P, Bjerremann Jensen L, et al. Cold urticaria patients exhibit normal skin levels of functional mast cells and histamine after tolerance induction. Dermatology. 2012;224(2):101-5. doi: 10.1159/000336572.
102.Sharma M, Bennett C, Cohen SN, Carter B. H1-antihistamines for chronic spontaneous urticaria. Cochrane Database Syst Rev. 2014;2014(11):CD006137. doi: 10.1002/14651858.CD006137
103.Williams PV. Pharmacologic Management of Chronic Urticaria in Pediatric Patients: The Gap Between Guidelines and Practice. Paediatr Drugs. 2020;22(1):21-28. doi: 10.1007/s40272-019-00365-3
104.Kudryavtseva AV, Neskorodova KA, Staubach P. Urticaria in children and adolescents: An updated review of the pathogenesis and management. Pediatr Allergy Immunol. 2019;30(1):17-24. doi: 10.1111/pai.12967.
105.Nakamura T, Hiraoka K, Harada R, et al. Brain histamine H1 receptor occupancy after oral administration of desloratadine and loratadine. Pharmacol Res Perspect. 2019;7(4):e00499. doi: 10.1002/prp2.499
106.Haria M, Fitton A, Peters DH. Loratadine. A reappraisal of its pharmacological properties and therapeutic use in allergic disorders. Drugs. 1994;48(4):617-37. doi: 10.2165/00003495-199448040-00009
107.An overview of angioedema: Clinical features, diagnosis, and management (last updated: Dec 21, 2022). URL: https://www.uptodate.com/contents/an-overview-of-angioedema-clinical-features-diagnosis-and-management?search=urticaria&topicRef=8108&source=related_link
108.Федеральные клинические рекомендации «Анафилактический шок» – М.: Российская ассоциация аллергологов и клинических иммунологов, Общероссийская общественная организация "Федерация анестезиологов и реаниматологов", 2022.
109.Zuberbier T, Iffländer J, Semmler C, Henz BM. Acute urticaria: clinical aspects and therapeutic responsiveness. Acta Derm Venereol. 1996;76(4):295-297. doi:10.2340/0001555576295297
110.Asero R, Tedeschi A. Usefulness of a short course of oral prednisone in antihistamine-resistant chronic urticaria: a retrospective analysis. J Investig Allergol Clin Immunol. 2010;20(5):386-390.
111.Talarico V, Marseglia GL, Lanari M, et al. Pediatric urticaria in the Emergency Department: epidemiological characteristics and predictive factors for its persistence in children. Eur Ann Allergy Clin Immunol. 2021;53(2):80-85. doi:10.23822/EurAnnACI.1764-1489.148
112.Long BJ, Koyfman A, Gottlieb M. Evaluation and Management of Angioedema in the Emergency Department. West J Emerg Med. 2019 Jul;20(4):587-600. doi: 10.5811/westjem.2019.5.42650.
113.Agache I, Rocha C, Pereira A, et al. Efficacy and safety of treatment with omalizumab for chronic spontaneous urticaria: A systematic review for the EAACI Biologicals Guidelines. Allergy. 2021;76(1):59-70. doi: 10.1111/all.14547
114.Aleksandraviciute L, Malinauskiene L, Cerniauskas K, Chomiciene A. Plasmapheresis: Is it a potential alternative treatment for chronic urticaria?. Open Med (Wars). 2021;17(1):113-118. doi:10.1515/med-2021-0399
115.Altrichter S, Salow J, Ardelean E, et al. Development of a standardized pulse-controlled ergometry test for diagnosing and investigating cholinergic urticaria. J Dermatol Sci. 2014;75(2):88-93. doi: 10.1016/j.jdermsci.2014.04.007
116.Lee EE, Maibach HI. Treatment of urticaria. An evidence-based evaluation of antihistamines. Am J Clin Dermatol. 2001;2(1):27-32. doi: 10.2165/00128071-200102010-00005. PMID: 11702618,
117.Grob JJ, Auquier P, Dreyfus I, Ortonne JP. How to prescribe antihistamines for chronic idiopathic urticaria: desloratadine daily vs PRN and quality of life. Allergy. 2009;64(4):605-612. doi:10.1111/j.1398-9995.2008.01913.x
118.Weller K, Ardelean E, Scholz E, et al. Can On-demand Non-sedating Antihistamines Improve Urticaria Symptoms? A Double-blind, Randomized, Single-dose Study. Acta Derm Venereol. 2013;93(2):168-174. doi: 10.2340/00015555-1434
119.Murota H, Kitaba S, Tani M, et al. Impact of sedative and non-sedative antihistamines on the impaired productivity and quality of life in patients with pruritic skin diseases. Allergol Int. 2010;59(4):345-54. doi: 10.2332/allergolint.10-OA-0182.
120.Fein MN, Fischer DA, O"Keefe AW, Sussman GL. CSACI position statement: newer generation H1-antihistamines are safer than first-generation H1-antihistamines and should be the first-line antihistamines for the treatment of allergic rhinitis and urticaria. Allergy Asthma Clin Immunol. 2019;15:61. doi: 10.1186/s13223-019-0375-9.
121.Chu DK, Oykhman P, Sussman GL. How to use antihistamines. CMAJ. 2021;193(14): E478-E479. doi: 10.1503/cmaj.201959
122.Staevska M, Popov TA, Kralimarkova T, et al. The effectiveness of levocetirizine and desloratadine in up to 4 times conventional doses in difficult-to-treat urticaria. J Allergy Clin Immunol. 2010;125: 676-682.
123.Siebenhaar F, Degener F, Zuberbier T, Martus P, Maurer M. High-dose desloratadine decreases wheal volume and improves cold provocation thresholds compared with standard-dose treatment in patients with acquired cold urticaria: a randomized, placebo-controlled, crossover study. J Allergy Clin Immunol. 2009;123(3):672-679. doi:10.1016/j.jaci.2008.12.008
124.Giménez-Arnau A, Izquierdo I, Maurer M. The use of a responder analysis to identify clinically meaningful differences in chronic urticaria patients following placebo- controlled treatment with rupatadine 10 and 20 mg. J Eur Acad Dermatol Venereol. 2009;23(9):1088-1091. doi:10.1111/j.1468-3083.2009.03289.x
125.Phinyo P, Koompawichit P, Nochaiwong S, et al. Comparative Efficacy and Acceptability of Licensed Dose Second-Generation Antihistamines in Chronic Spontaneous Urticaria: A Network Meta-Analysis. J Allergy Clin Immunol Pract. 2021;9(2):956-970.e57. doi: 10.1016/j.jaip.2020.08.055
126.Iriarte Sotés P, Armisén M, Usero-Bárcena T, et al.; Urtigal, the Galician Group of Interest in Urticaria. Efficacy and Safety of Up-dosing Antihistamines in Chronic Spontaneous Urticaria: A Systematic Review of the Literature. J Investig Allergol Clin Immunol. 2021;31(4):282-291. doi: 10.18176/jiaci.0649
127.Guillén-Aguinaga S, Jáuregui Presa I, Aguinaga-Ontoso E, et al. Updosing nonsedating antihistamines in patients with chronic spontaneous urticaria: a systematic review and meta-analysis. Br J Dermatol. 2016;175(6):1153-1165. doi: 10.1111/bjd.14768
128.Church MK, Tiongco-Recto M, Ridolo E, Novák Z. Bilastine: a lifetime companion for the treatment of allergies. Curr Med Res Opin. 2020;36(3):445-454. doi: 10.1080/03007995.2019.1681134
129.Kontou-Fili K, Maniatakou G, Demaka P, et al. Therapeutic effects of cetirizine in delayed pressure urticaria: clinicopathologic findings. J Am Acad Dermatol. 1991;24(6 Pt 2):1090-1093. doi:10.1016/0190-9622(91)70163-v
130.Zuberbier T, Münzberger C, Haustein U, et al. Double-blind crossover study of high-dose cetirizine in cholinergic urticaria. Dermatology. 1996;193(4):324-327. doi:10.1159/000246281
131.Gimenez- Arnau A, Izquierdo I, Maurer M. The use of a responder analysis to identify clinically meaningful differences in chronic urticaria patients following placebo- controlled treatment with rupatadine 10 and 20 mg. J Eur Acad Dermatol Venereol. 2009;23(9):1088- 1091. doi:10.1111/j.1468- 3083.2009.03289.x
132.Guillen-Aguinaga S, Jauregui Presa I, Aguinaga- Ontoso E, et al. Updosing nonsedating antihistamines in patients with chronic spontaneous urticaria: a systematic review and meta- analysis. Br J Dermatol. 2016;175(6):1153-1165. doi:10.1111/bjd.14768
133.Zhang L, Wu J, Qi Y, et al. Long-term combinations and updosing of second-generation H1-antihistamines show efficacy and safety in the treatment of chronic spontaneous urticaria: A multicenter real-life pilot study. J Allergy Clin Immunol Pract. 2020;8(5):1733-1736.e11. doi:10.1016/j.jaip.2019.12.006
134.Sarti L, Barni S, Giovannini M, Liccioli G, Novembre E, Mori F. Efficacy and tolerability of the updosing of second-generation non-sedating H1 antihistamines in children with chronic spontaneous urticaria. Pediatr Allergy Immunol. 2021;32(1):153-160. doi:10.1111/pai.13325
135.Koosakulchai V, Yuenyongviwat A, Sangsupawanich P. Risk factors of uncontrolled symptoms using the standard dose of second-generation H1 -antihistamines in chronic spontaneous urticaria children. Asian Pac J Allergy Immunol. 2022;40(2):121-125
136.Zhao ZT, Ji CM, Yu WJ, et al. Omalizumab for the treatment of chronic spontaneous urticaria: A meta-analysis of randomized clinical trials. J Allergy Clin Immunol. 2016;137(6):1742-1750.e4. doi:10.1016/j.jaci.2015.12.1342
137.Maurer M, Metz M, Brehler R, et al. Omalizumab treatment in patients with chronic inducible urticaria: A systematic review of published evidence. J Allergy Clin Immunol. 2018;141(2):638-649. doi:10.1016/j.jaci.2017.06.032
138.Tharp MD, Bernstein JA, Kavati A, et al. Benefits and Harms of Omalizumab Treatment in Adolescent and Adult Patients With Chronic Idiopathic (Spontaneous) Urticaria: A Meta-analysis of "Real-world" Evidence. JAMA Dermatol. 2019;155(1):29-38. doi:10.1001/jamadermatol.2018.3447
139.Saini S, Rosen KE, Hsieh HJ, et al. A randomized, placebo-controlled, dose-ranging study of single-dose omalizumab in patients with H1-antihistamine-refractory chronic idiopathic urticaria. J Allergy Clin Immunol. 2011;128(3):567-73.e1. doi:10.1016/j.jaci.2011.06.010
140.Maurer M, Altrichter S, Bieber T, et al. Efficacy and safety of omalizumab in patients with chronic urticaria who exhibit IgE against thyroperoxidase. J Allergy Clin Immunol. 2011;128(1):202-209.e5. doi:10.1016/j.jaci.2011.04.038
141.Saini SS, Bindslev-Jensen C, Maurer M, et al. Efficacy and safety of omalizumab in patients with chronic idiopathic/spontaneous urticaria who remain symptomatic on H1 antihistamines: a randomized, placebo-controlled study [published correction appears in J Invest Dermatol. 2015 Mar;135(3):925]. J Invest Dermatol. 2015;135(1):67-75. doi:10.1038/jid.2014.306
142.Maurer M, Rosén K, Hsieh HJ, et al. Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria [published correction appears in N Engl J Med. 2013 Jun 13;368(24):2340-1]. N Engl J Med. 2013;368(10):924-935. doi:10.1056/NEJMoa1215372
143.Kaplan A, Ledford D, Ashby M, et al. Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy. J Allergy Clin Immunol. 2013;132(1):101-109. doi:10.1016/j.jaci.2013.05.013
144.Urgert MC, van den Elzen MT, Knulst AC, et al. Omalizumab in patients with chronic spontaneous urticaria: a systematic review and GRADE assessment. Br J Dermatol. 2015;173(2):404-15. doi: 10.1111/bjd.13845.
145.Rubini NPM, Ensina LFC, Silva EMK, et al. Effectiveness and safety of Omalizumab in the treatment of chronic spontaneous urticaria: Systematic review and meta-analysis. Allergol Immunopathol (Madr). 2019;47(6):515-522. doi: 10.1016/j.aller.2019.05.003
146.Jia HX, He YL. Efficacy and Safety of Omalizumab for Chronic Spontaneous Urticaria: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Am J Ther. 2020;27(5): e455-e467. doi: 10.1097/MJT.0000000000000912
147.Summary of Product Characteristics – Xolair (omalizumab). Novartis Europharm Limited (last updated: Dec 21, 2022). URL: https://www.ema.europa.eu/en/documents/product-information/xolair-epar-productinformation_en.pdf
148.Kocatürk E, Deza G, Kızıltaç K, Giménez-Arnau AM. Omalizumab Updosing for Better Disease Control in Chronic Spontaneous Urticaria Patients. Int Arch Allergy Immunol. 2018;177(4):360-364. doi: 10.1159/000491530.
149.Metz M, Vadasz Z, Kocatürk E, Giménez-Arnau AM. Omalizumab Updosing in Chronic Spontaneous Urticaria: an Overview of Real-World Evidence. Clin Rev Allergy Immunol. 2020;59(1):38-45. doi: 10.1007/s12016-020-08794-6
150.Manzoor H, Razi F, Rasheed A, et al. Efficacy of Different Dosing Regimens of IgE Targeted Biologic Omalizumab for Chronic Spontaneous Urticaria in Adult and Pediatric Populations: A Meta-Analysis. Healthcare (Basel). 2022;10(12):2579. doi:10.3390/healthcare10122579
151.Staubach P, Peveling-Oberhag A, Lang BM, Zimmer S, Sohn A, Mann C. Severe chronic spontaneous urticaria in children - treatment options according to the guidelines and beyond - a 10 years review. J Dermatolog Treat. 2022;33(2):1119-1122. doi:10.1080/09546634.2020.1782326
152.Stellato C, de Paulis A, Ciccarelli A, et al. Anti-inflammatory effect of cyclosporin A on human skin mast cells. J Invest Dermatol. 1992;98(5):800-804. doi:10.1111/1523-1747.ep12499960
153.Harrison CA, Bastan R, Peirce MJ, Munday MR, Peachell PT. Role of calcineurin in the regulation of human lung mast cell and basophil function by cyclosporine and FK506. Br J Pharmacol. 2007;150(4):509-518. doi:10.1038/sj.bjp.0707002
154.Boubouka CD, Charissi C, Kouimintzis D, Kalogeromitros D, Stavropoulos PG, Katsarou A. Treatment of autoimmune urticaria with low-dose cyclosporin A: A one-year follow-up. Acta Derm Venereol. 2011;91(1):50-54. doi:10.2340/00015555-0939
155.Grattan CE, O"Donnell BF, Francis DM, et al. Randomized double-blind study of cyclosporin in chronic "idiopathic" urticaria. Br J Dermatol. 2000;143(2):365-372. doi:10.1046/j.1365-2133.2000.03664.x
156.Vena GA, Cassano N, Colombo D, Peruzzi E, Pigatto P; Neo-I-30 Study Group. Cyclosporine in chronic idiopathic urticaria: a double-blind, randomized, placebo-controlled trial. J Am Acad Dermatol. 2006;55(4):705-709. doi:10.1016/j.jaad.2006.04.078
157.Kulthanan K, Chaweekulrat P, Komoltri C, et al. Cyclosporine for Chronic Spontaneous Urticaria: A Meta-Analysis and Systematic Review. J Allergy Clin Immunol Pract. 2018;6(2):586-599. doi:10.1016/j.jaip.2017.07.017
158.Doshi DR, Weinberger MM. Experience with cyclosporine in children with chronic idiopathic urticaria. Pediatr Dermatol. 2009;26(4):409-413. doi:10.1111/j.1525-1470.2009.00869.x
159.Sánchez J, Alvarez L, Cardona R. Cyclosporine and omalizumab together: A new option for chronic refractory urticaria. J Allergy Clin Immunol Pract. 2020;8(6):2101-2103. doi:10.1016/j.jaip.2020.02.012
160.Rosenblum JD, Nassau S, Fonacier L, Mawhirt SL. Concomitant treatment with omalizumab and cyclosporine for chronic spontaneous urticaria. Ann Allergy Asthma Immunol. 2020;125(1):111-112. doi:10.1016/j.anai.2020.04.020
161.Mitchell S, Balp MM, Samuel M, McBride D, Maurer M. Systematic review of treatments for chronic spontaneous urticaria with inadequate response to licensed first-line treatments. Int J Dermatol. 2015 Sep;54(9):1088-104. doi: 10.1111/ijd.12727
162.Ryan C, Amor KT, Menter A. The use of cyclosporine in dermatology: part II. J Am Acad Dermatol. 2010;63(6):949-974. doi:10.1016/j.jaad.2010.02.062
163.Vena GA, Cassano N, D"Argento V, Milani M. Clobetasol propionate 0.05% in a novel foam formulation is safe and effective in the short-term treatment of patients with delayed pressure urticaria: a randomized, double-blind, placebo-controlled trial. Br J Dermatol. 2006;154(2):353-6. doi: 10.1111/j.1365-2133.2005.06986.x
164.Kozel M. M. A., Sabroe R. A. Chronic urticaria: aetiology, management and current and future treatment options. Drugs, 2004. Р. 2515-2536
165.Barlow RJ, Macdonald DM, Black AK, Greaves MW. The effects of topical corticosteroids on delayed pressure urticaria. Arch Dermatol Res. 1995;287(3-4):285-288. doi:10.1007/BF01105080
166.Holm JG, Ivyanskiy I, Thomsen SF. Use of nonbiologic treatments in antihistamine-refractory chronic urticaria: a review of published evidence. J Dermatolog Treat. 2018;29(1):80-97. doi: 10.1080/09546634.2017.1329505
167.Morgan M, Cooke A, Rogers L, Adams-Huet B, Khan DA. Double-blind placebo-controlled trial of dapsone in antihistamine refractory chronic idiopathic urticaria. J Allergy Clin Immunol Pract. 2014 Sep-Oct;2(5):601-6. doi: 10.1016/j.jaip.2014.06.004
168.Alkeraye S, AlRuhaimi DK. The Addition of Montelukast for the Treatment of Chronic Idiopathic Urticaria. Cureus. 2021;13(7):e16137. doi: 10.7759/cureus.16137
169.Akenroye AT, McEwan C, Saini SS. Montelukast reduces symptom severity and frequency in patients with angioedema-predominant chronic spontaneous urticaria. J Allergy Clin Immunol Pract. 2018;6(4):1403-1405. doi: 10.1016/j.jaip.2018.04.026
170.Grattan CE, Francis DM, Slater NG, Barlow RJ, Greaves MW. Plasmapheresis for severe, unremitting, chronic urticaria. Lancet. 1992;339(8801):1078-1080. doi:10.1016/0140-6736(92)90666-q
171.Etwel F, Faught LH, Rieder MJ, Koren G. The Risk of Adverse Pregnancy Outcome After First Trimester Exposure to H1 Antihistamines: A Systematic Review and Meta-Analysis. Drug Saf. 2017;40(2):121-132. doi: 10.1007/s40264-016-0479-9
172.Gonzalez-Estrada A, Geraci SA. Allergy Medications During Pregnancy. Am J Med Sci. 2016;352(3):326-31. doi: 10.1016/j.amjms.2016.05.030
173.Weber-Schoendorfer C, Schaefer C. The safety of cetirizine during pregnancy. A prospective observational cohort study. Reprod Toxicol. 2008;26:19-23
174.Østensen M, Lockshin M, Doria A, et al. Update on safety during pregnancy of biological agents and some immunosuppressive anti-rheumatic drugs. Rheumatology (Oxford). 2008;47 Suppl 3:iii28-iii31. doi:10.1093/rheumatology/ken168
175.Golembesky A, Cooney M, Boev R, Schlit AF, Bentz JWG. Safety of cetirizine in pregnancy. J Obstet Gynaecol. 2018;38(7):940-945. doi:10.1080/01443615.2018.1441271
176.Schwarz EB, Moretti ME, Nayak S, Koren G. Risk of hypospadias in offspring of women using loratadine during pregnancy: a systematic review and meta-analysis. Drug Saf. 2008;31(9):775-788. doi:10.2165/00002018-200831090-00006
177.Namazy J, Cabana MD, Scheuerle AE, et al. The Xolair Pregnancy Registry (EXPECT): the safety of omalizumab use during pregnancy. J Allergy Clin Immunol. 2015;135(2):407-412. doi:10.1016/j.jaci.2014.08.025
178.González-Medina M, Curto-Barredo L, Labrador-Horrillo M, Giménez-Arnau A. Omalizumab use during pregnancy for chronic spontaneous urticaria (CSU): report of two cases. J Eur Acad Dermatol Venereol. 2017;31(5):e245-e246. doi:10.1111/jdv.14034
179.Ghazanfar MN, Thomsen SF. Successful and Safe Treatment of Chronic Spontaneous Urticaria with Omalizumab in a Woman during Two Consecutive Pregnancies. Case Rep Med. 2015;2015:368053. doi:10.1155/2015/368053
180.Namazy JA, Blais L, Andrews EB, et al. Pregnancy outcomes in the omalizumab pregnancy registry and a disease-matched comparator cohort. J Allergy Clin Immunol. 2020;145(2):528-536.e1. doi:10.1016/j.jaci.2019.05.019
181.Ramsey-Goldman R, Schilling E. Immunosuppressive drug use during pregnancy. Rheum Dis Clin North Am. 1997;23(1):149-167. doi:10.1016/s0889-857x(05)70320-3
182.Bar Oz B, Hackman R, Einarson T, Koren G. Pregnancy outcome after cyclosporine therapy during pregnancy: a meta-analysis. Transplantation. 2001;71(8):1051-1055. doi:10.1097/00007890-200104270-00006
183.Paziana K, Del Monaco M, Cardonick E, et al. Ciclosporin use during pregnancy. Drug Saf. 2013;36(5):279-94. doi: 10.1007/s40264-013-0034-x
184.Sánchez-Borges M, Ansotegui IJ, Baiardini I, et al. The challenges of chronic urticaria part 2: Pharmacological treatment, chronic inducible urticaria, urticaria in special situations. World Allergy Organ J. 2021;14(6):100546. Published 2021 Jun 3. doi:10.1016/j.waojou.2021.100546
185.Hacard F, Martin C, Verdu V, et al. Therapeutic patient education improves knowledge and skills for patients with chronic spontaneous urticaria. Eur J Dermatol. 2018;28(6):823-827. doi: 10.1684/ejd.2018.3442
186.Friedman AJ, Cosby R, Boyko S, et al. Effective teaching strategies and methods of delivery for patient education: a systematic review and practice guideline recommendations. J Cancer Educ. 2011;26(1):12-21. doi: 10.1007/s13187-010-0183-x
187.Rooney MK, Santiago G, Perni S, et al. Readability of Patient Education Materials From High-Impact Medical Journals: A 20-Year Analysis. J Patient Exp. 2021;8:2374373521998847. doi: 10.1177/2374373521998847
188.Konstantinou GN, Konstantinou GN. Psychiatric comorbidity in chronic urticaria patients: a systematic review and meta-analysis. Clin Transl Allergy. 2019;9:42. doi: 10.1186/s13601-019-0278-3
189.Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок: Методические указания. М.: Федеральный центр госсанэпиднадзора Минздрава России, 2002.— 16 с.
190.Nebiolo F, Bergia R, Bommarito L, et al. Effect of arterial hypertension on chronic urticaria duration. Ann Allergy Asthma Immunol. 2009;103(5):407-410. doi:10.1016/S1081-1206(10)60360-2
191.Kulthanan K, Jiamton S, Thumpimukvatana N, Pinkaew S. Chronic idiopathic urticaria: prevalence and clinical course. J Dermatol. 2007;34(5):294-301. doi:10.1111/j.1346-8138.2007.00276.x
192.Kozel MM, Mekkes JR, Bossuyt PM, Bos JD. Natural course of physical and chronic urticaria and angioedema in 220 patients. J Am Acad Dermatol. 2001;45(3):387-391. doi:10.1067/mjd.2001.116217
193.Hiragun M, Hiragun T, Mihara S, et al.. Prognosis of chronic spontaneous urticaria in 117 patients not controlled by a standard dose of antihistamine. Allergy. 2013;68(2):229-235. doi:10.1111/all.12078
194.Cortellazzo Wiel L, Conversano E, Giangreco M, et al. Natural history and predictors of recovery in children with chronic spontaneous urticaria. Pediatr Allergy Immunol. 2021;32(1):201-204. doi: 10.1111/pai.13299
195.Özyılmaz-Bozat G, Şahiner ÜM, Buyuktiryaki B, et al. Children with chronic spontaneous urticaria: Recurrence after remission and its predictors. J Allergy Clin Immunol Pract. 2020;8(2):796-798.e1. doi: 10.1016/j.jaip.2019.08.010
196.Van der Valk PG, Moret G, Kiemeney LA. The natural history of chronic urticaria and angioedema in patients visiting a tertiary referral centre. Br J Dermatol. 2002;146(1):110-113. doi:10.1046/j.1365-2133.2002.04582.x
197.Hawro T, Ohanyan T, Schoepke N, et al. Comparison and interpretability of the available urticaria activity scores. Allergy. 2018;73(1):251-255. doi:10.1111/all.13271
198.Ohanyan T, Schoepke N, Bolukbasi B, et al. Responsiveness and minimal important difference of the urticaria control test. J Allergy Clin Immunol. 2017;140(6):1710-1713.e11. doi:10.1016/j.jaci.2017.04.050
199.Weller K, Groffik A, Church MK, et al. Development and validation of the Urticaria Control Test: a patient-reported outcome instrument for assessing urticaria control. J Allergy Clin Immunol. 2014;133(5):1365-1372.e13726. doi:10.1016/j.jaci.2013.12.1076
200.Weller K, Groffik A, Magerl M, et al. Development, validation, and initial results of the Angioedema Activity Score. Allergy. 2013;68(9):1185-1192. doi:10.1111/all.12209



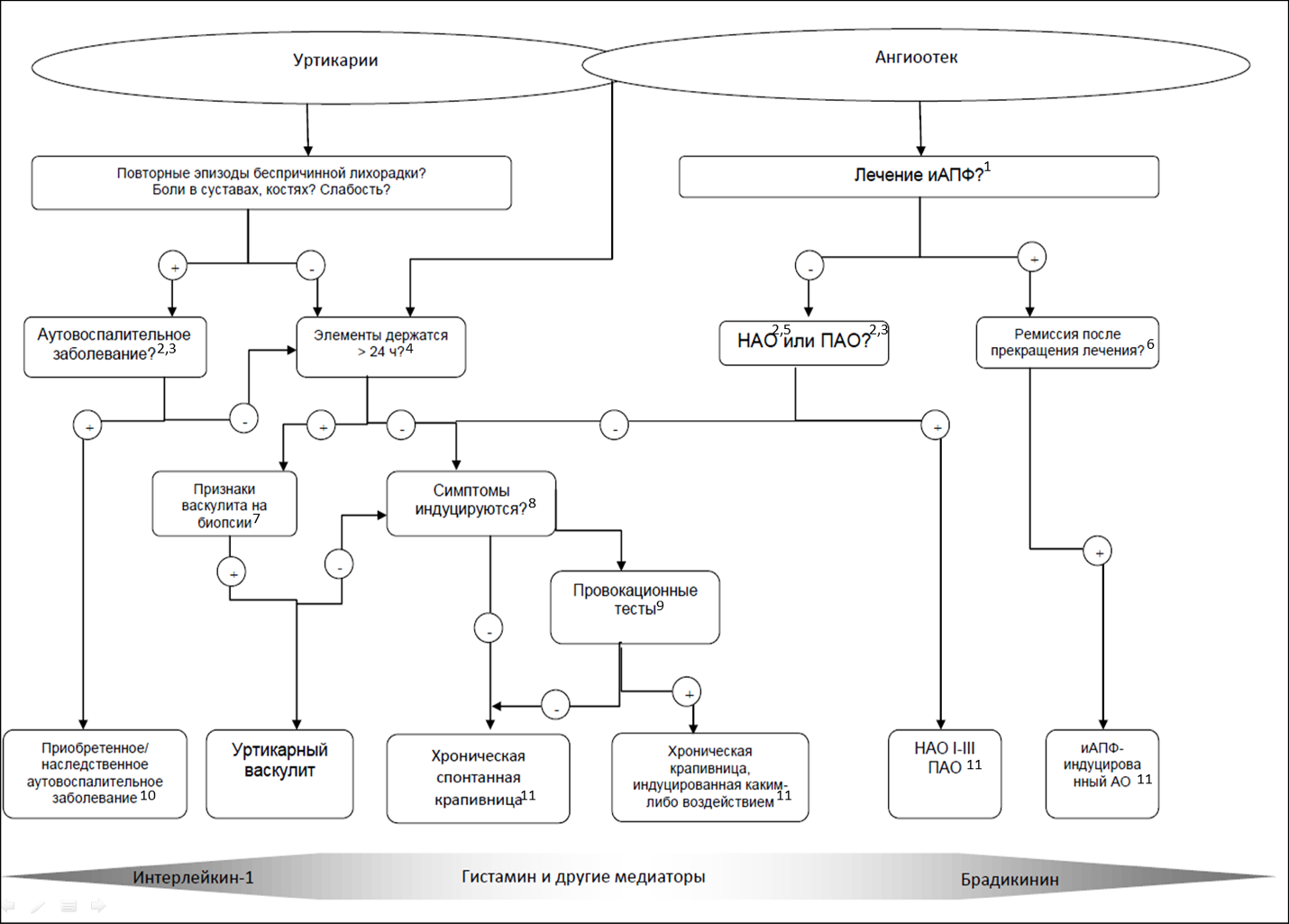

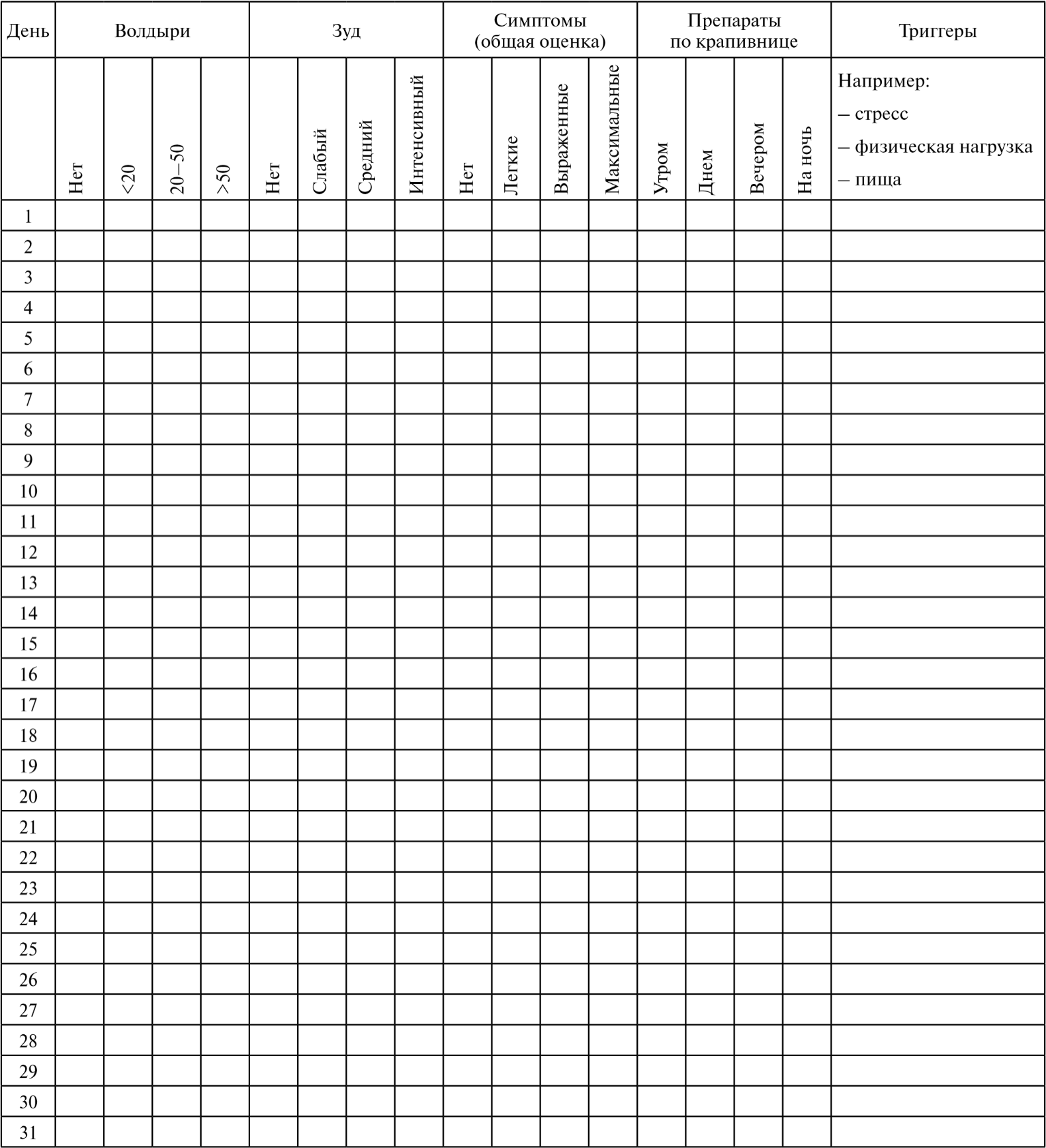 Ключ (интерпретация):
Ключ (интерпретация):