Новая коронавирусная инфекция SARS-CoV-2 у пациентов пожилого и старческого возраста: особенности профилактики, диагностики и лечения. Согласованная позиция экспертов Российской ассоциации геронтологов и гериатров
Авторы
Ткачева О. Н., Котовская Ю. В., Алексанян Л. А., Мильто А. С., Наумов А. В., Стражеско И. Д., Воробьева Н. М., Дудинская Е. Н., Малая И. П., Крылов К. Ю., Тюхменев Е. А., Розанов А. В., Остапенко В. С., Маневич Т. М., Щедрина А. Ю., Семенов Ф. А., Мхитарян Э. А., Ховасова Н. О., Ерусланова Е. А., Котовская Н. В., Шарашкина Н. В.
Российская ассоциация геронтологов и гериатров. Москва, Россия
Профессиональные ассоциации:
Российская ассоциация геронтологов и гериатров
Введение
Вспышка новой коронавирусной инфекции, вызванная вирусом SARS-CoV-2 (COVID-19), является вызовом системам здравоохранения всех стран мира и представляет особую угрозу людям пожилого и старческого возраста. SARS-CoV-2 отличается от других вирусов, вызывающих заболевания верхних дыхательных путей, высокой вирулентностью. При равной вероятности встречи с вирусом люди пожилого и старческого возраста характеризуются более тяжелым течением заболевания по сравнению с молодыми людьми. Уже первые данные из Китая указывали на колос- сальные различия смертности в зависимости от возраста — 0,2-0,4% в возрасте до 50 лет, 1,3 — 50-59 лет, 3,6% — 60-69 лет, 14,3% — 80 лет и старше [1, 2]. В Италии, где 23% населения старше 65 лет, 89% случаев смерти от COVID-19 приходится на лиц старше 70 лет (31% в возрасте от 70 до 79 лет и 58% — старше 80 лет) [3, 4].
Средний срок от появления симптомов до смерти у лиц 70 лет и старше составляет 11,5 дней, в то время как у более молодых — 14 дней [5]. Риск тяжелого течения заболевания и неблагоприятных исходов у пациентов старших возрастных групп связывают со снижением функций иммунной системы, происходящих с возрастом, снижением физиологических резервов, полиморбидностью.
Данный документ сфокусирован на особенностях профилактики, диагностики и лечения пациентов пожилого и старческого возраста.
Профилактические меры у пациентов пожилого и старческого возраста в период распространения COVID-19
Профилактические мероприятия в отношении людей пожилого и старческого возраста должны охватывать три ключевых взаимосвязанных аспекта:
1) профилактика собственно инфицирования вирусом,
2) сохранение функционального статуса и профилактика гериатрических синдромов, включая использование мер социальной поддержки,
3) контроль коморбидных состояний.
Профилактика инфицирования
Самоизоляция, социальное дистанцирование и соблюдение правил личной гигиены являются важнейшими компонентами профилактики инфицирования (таблица 1). В условиях изоляции во время карантина люди пожилого и старческого возраста, особенно со снижением когнитивных функций/деменцией, могут становится более тревожными, раздраженными, беспокойными. В этих условиях особое значение для их состояния играет социальная поддержка, поддержка со стороны семьи и работников здравоохранения. Необходимо простыми словами и на простых примерах ясно доносить до людей пожилого возраста с и без когнитивных нарушений, каким образом можно снизить риск заражения. Полезно визуальное представление информации.
Организациям, в коллективах которых работают люди пожилого возраста, рекомендуется перевести сотрудников пожилого возраста на удаленную работу. В медицинских организациях, оказывающих помощь пациентам пожилого и старческого возраста, в домах престарелых следует неукоснительно соблюдать противоэпидемические и санитарные меры.
Таблица 1. Памятка для людей пожилого и старческого возраста для предупреждения инфицирования COVID-19

Сохранение функционального статуса и профи- лактика гериатрических синдромов
В период распространения COVID-19 людям старшего возраста необходимо соблюдать основополагающие меры по сохранению своего здоровья и функционального статуса. Для поддержания функционального статуса, профилактики саркопении необходимо рекомендовать пожилым людям максимально возможную физическую активность (ФА), продолжение в домашних условиях физических упражнений, направленных на укрепление мышечной силы, выносливости и равновесия, в т.ч. с использованием видеоуроков по физическим упражнениями для пожилых.
Питание пожилого человека должно быть полноценным с обязательным потреблением продуктов, содержащих белок, в каждый прием пищи; употребление жидкости не менее 1,5 л в сут. [6-8]. Важна организация безопасного быта для предотвращения падений. Общий ориентир по энергетической ценности рациона для людей пожилого возраста составляет 30 ккал/кг массы тела/сут., потребность в белке у здорового пожилого человека 1,0 г (1,0-1,2 г) на кг массы тела в сутки. Для обеспечения потребностей пациентов в энергии и белке, а также в важнейших микронутриентах (витамин Д), целесообразно применять препараты перорального энтерального питания (ПЭП) [6-8] в качестве дополнения к обычной пище. Эта рекомендация особенно актуальная для пациентов со старческой астенией с риском мальнутриции.
У здоровых людей пожилого и старческого возраста рекомендуется восполнять дефицит отдельных микронутриентов с помощью пищевых добавок и/или лекарственных средств в случаях, если этот дефицит подтвержден клиническими и/или лабораторными данным [7, 8]. В других случаях содержание микронутриентов в ежедневном рационе лиц пожилого и старческого возраста должно соответствовать нормам физиологических потребностей в энергии и пищевых веществах для лиц пожилого и старческого возраста. Обычно в периоды распространения сезонных вирусных инфекций нередко обсуждается использование витаминсодержащих добавок с целью профилактики и/или уменьшения негативных последствий заболевания. Следует признать неубедительность данных об их эффективности [8].
Согласно клиническим рекомендациям “Старческая астения” у пациентов пожилого и старческого возраста следует уделать особое внимание коррекции дефицита витамина Д с целью профилактики падений, переломов, а также в комплекс- ной терапии заболеваний костно-мышечной системы и хронического болевого синдрома, которые могут обостриться в период самоизоляции/карантина [9]. Дефицит витамина Д широко распространен в российской популяции лиц пожилого и старческого возраста [10].
В условиях распространения COVID-19 потенциальная роль дефицита витамина Д обсуждается в контексте многих факторов, наиболее важным их которых является тот, что большое количество случаев смерти при COVID-19 наблюдается у полиморбидных пациентов старшего возраста, т.е. при состояниях, ассоциированных с более низкой концентрацией 25(OH)D [11].
Витамин Д является важным модулятором функционирования иммунной системы человека. Дефицит витамина Д ассоциирован с высокой активностью воспаления [11-13] и может вносить непосредственный вклад в развитие острого респираторного дистресс синдрома, который является одной из ведущих причин смерти пациентов с COVID-19 [14, 15].
Механизмы, благодаря которым, витамин Д потенциально может снизить риск заражения и облегчить течение заболеваниями, включают стимуляцию продукции кателицидинов (семейство антимикробных белков, которые главным образом обнаружены в пероксидаза-отрицательных гранулах нейтрофилов) и дефензинов (катионные пептиды иммунной системы, активные в отношении бактерий, грибков и многих оболочечных и безоболочечных вирусов), которые могут подавлять скорость репликации вируса, а также снижение уровня про- воспалительных цитокинов (ключевой механизм поражения легочной ткани при COVID-19) и повышение уровня противовоспалительных цитокинов [11]. Ряд экспертов рекомендуют рассмотреть в период распространения COVID-19 с целью профилактики заражения назначение витамина Д в дозе 10000 МЕ/сут. на несколько недель для того, чтобы быстро поднять его концентрацию в сыворотке, а затем через месяц перейти на поддерживающую дозу 5000 МЕ/сут. Цель — достичь концентрации 40-60 нг/мл (100-150 нмоль/л), что несколько превышает традиционный порог (30 нг/мл), который рекомендуется поддерживать при назначении витамина Д [16]. Рассматривается и назначение нагрузочных доз 200000-300000 ЕД и применение более высоких поддерживающих доз для снижения тяжести заболевания [16]. Для подтверждения указанных рекомендаций необходимо проведение рандомизированных контролируемых и больших популяционных исследований с целью оценки эффективности такого вмешательства.
Социальная поддержка
Люди пожилого и старческого возраста нуждаются в социальной поддержке и помощи. Вынужденное, но необходимое ограничение социальных контактов может отрицательно сказаться на психоэмоциональном и функциональном статусе пожилого человека. Помощь социальных служб и волонтеров важна, но должна быть безопасной. Социальные работники и волонтеры должны помнить о том, что они могут быть потенциальными носителями вируса и предпринимать все меры для предотвращения заражения пожилого человека, которому они оказывают помощь. Для обеспечения безопасности рекомендуется использование средств индивидуальной защиты (маски, перчатки), обеспечивать бесконтактную передачу продуктов или предметов. Родственникам пожилых людей необходимо как можно чаще общаться с ними с использованием современных возможностей связи: по телефону, интернету.
Ведение коморбидных заболеваний
В период самоизоляции в силу изменения режима привычной активности, психоэмоционального стресса у пациентов пожилого и старческого возможна декомпенсация течения хронических заболеваний. Следует информировать об этом пациента и мотивировать строго соблюдать рекомендации по приему лекарственных препаратов.
Сердечно-сосудистые заболевания (ССЗ) (артериальная гипертония (АГ), ишемическая болезнь сердца (ИБС), хроническая сердечная недостаточность (ХСН), фибрилляция предсердий (ФП)), сахарный диабет (СД), хроническая обструктивная болезнь легких (ХОБЛ), болевой синдром вследствие заболеваний опорно-двигательного аппарата являются наиболее распространенным коморбидными состояниями у пациентов пожилого и старческого возраста. Следует отметить, что многие из этих заболеваний расcматриваются в качестве факторов риска неблагоприятного течения COVID-19.
АГ. Следует рекомендовать продолжение приема антигипертензивных препаратов, ориентируясь на целевой диапазон артериального давления (АД) 130-139/70-79 мм рт.ст. у пациентов пожилого и старческого возраста без старческой астении. У пациентов со старческой астенией также следует продолжить антигипертензивную терапию с учетом индивидуального целевого уровня АД, определенного с учетом функционального статуса пациента [17].
ИБС. У пациентов с ИБС следует продолжить ранее подобранную терапию, включая прием статинов, блокаторов ренинангиотензиновой системы, бета-адреноблокаторов, антитромбоцитарных препаратов. В случае заражения коронавирусной инфекцией и назначении лопиновира/ритонавира следует помнить о возможности развития лекарственных взаимодействий, и не назначать его совместно с клопидогрелем, тикагрелором, ивабрадином, ранолазином, симвастатином. При назначении лопинавира/ритонавира максимальная суточная доза розувастатина составляет 10 мг/сут., аторвастатина — 20 мг/сут., может потребоваться снижение дозы бета-адреноблокаторов. Для эзетимиба лекарственные взаимодействия с лопинавиром/ритонавиром не описаны. При назначении гидроксихлорохина может потребоваться снижение дозы метопролола и небиволола [17].
ХСН. Следует продолжить назначенную терапию блокаторами ренин-ангиотензиновой системы (РААС), бета-адреноблокаторами. При назначении лопинавира/ритонавира может потребоваться коррекция дозы валсартана, сакубитрила/валсартана, небиволола, метопролола. Не следует совместно назначать лопинавир/ритонавир с эплереноном [17]. Применение блокаторов РААС. Источником дискуссии о применении блокаторов РААС в период распространения COVID-19 стали данные о механизме проникновения вируса в клетку через рецептор к ангиотензинпревращающему ферменту-2. Ведущие экспертные кардиологические сообщества подчеркивают, что в настоящее время нет экспериментальных или клинических данных, свидетельствующих о благоприятном или неблагоприятном влиянии терапии блокаторами РААС на исходы у пациентов с COVID-19 или у пациентов с COVID- 19, имеющих ССЗ и получающих терапию этими препаратами. Рекомендуется продолжить терапию блокаторами РААС у пациентов, уже получающих их по показаниям (АГ, ИБС, ХСН, СД, хроническая болезнь почек). Если у пациента с ССЗ диагностируется COVID-19, решение о продолжении терапии принимается индивидуально, исходя из статуса гемодинамики и клинических проявлений. Назначение или отмена блокаторов производится РААС согласно стандартной клинической практике [18-20].
В отношении применения блокаторов РААС для у пациентов пожилого возраста (>65 лет) с АГ получены данные ретроспективного метаанализа о том, что прием блокаторов РААС был ассоциирован со снижением риска тяжелого течения COVID- 19, в т.ч. со смертельным исходом, по сравнению с пациентами, которые не принимали антигипертензивной терапии [21, 22].
ФП. Пациентам с ФП рекомендуется продолжить прием оральных антикоагулянтов с соблюдением обычных мер предосторожности и контроля безопасности. Продолжение приема оральных антикоагулянтов в период угрозы заражения COVID-19 представляется особенно важным в виду высокой частоты тромботических осложнений, которые наблюдаются при этом заболевании, и их вклада в неблагоприятный прогноз. В виду риска развития лекарственных взаимодействий при назначении лопинавира/ритонавира не следует назначать его совместно с ривароксабаном. При совместном назначении с лопиновиром/ритонавиром апиксабан следует использовать в половинной дозе и не назначать в случаях, если показана доза 2,5 мг 2 раза/сут., дабигатран и варфарин назначать с осторожностью. Гидроксихлорохин не взаимодействует с перечисленными лекарственными препаратами [17, 23].
СД. Следует избегать избыточного снижения уровня глюкозы, особенно <3,9 ммоль/л. Целевой уровень гликемии для больных COVID-19 не установлен, в виду чего следует использовать стандартные целевые уровни гликемии для пациентов СД с учётом возраста и коморбидной патологии. Следует напомнить пациенту о необходимости строгого выполнения диетических рекомендаций, соблюдения питьевого режима, рекомендовать более частый контроль уровня глюкозы и ведение дневника самоконтроля [24].
ХОБЛ. Наличие ХОБЛ повышает риск развития тяжелой COVID-19 в 4,38 раз, курение — в 1,98 раза [25]. Имеются данные об up-регуляции рецепторов ангиотензинпревращающего фермента-2 никотином, что подтверждает важность отказа от курения. Рекомендации экспертных сообществ подчеркивают важность продолжения базисной терапии ХОБЛ. Постоянный прием глюкокортикостероидов (ГКС) при ХОБЛ не рекомендуется, однако у некоторых пациентов ингаляционные ГКС могут быть назначены при риске обострения, системные ГКС — коротким курсом (5-10 дней) при обострении заболевания. В настоящее время нет убедительных данных в пользу изменений рекомендаций по применению базисной терапии ХОБЛ у пациентов, не зараженных COVID-19. При заражении COVID-19 рекомендуется отменять системные ГКС и применять их только по витальным показаниям [26].
Применение нестероидных противовоспалительных препаратов (НПВП). В клинических рекомендациях “Старческая астения” [9] четко сформулированы положения о существенных ограничениях и противопоказаниях применения НПВП у пациентов пожилого и старческого возраста. Активно обсуждалось предположение, что применение НПВП в начале лечения COVID-19 может усугублять течение заболевания и возможно ассоциироваться с неблагоприятными исходами. Предположение основывалось на предыдущем опыте ухудшения течения ветряной оспы и некоторых бактериальных инфекций при использовании ибупрофена и кетотифена, а также на том, что инструкции по приме- нению НПВП содержат предупреждение о том, что их противовоспалительное действие может маскировать симптомы прогрессирования инфекции [27]. В настоящее время нет научных доказательств, устанавливающих связь между терапией ибупрофеном или другими НПВП и ухудшением COVID-19. Европейское медицинское агентство предполагает возможность использования НПВП при COVID-19 в минимально эффективной дозе в течение воз- можно кратчайшего периода времени, что полностью согласуется с положениями клинических рекомендаций “Старческая астения” [9, 28].
Лечение заболеваний желудочно-кишечного тракта (ЖКТ) и защита слизистых оболочек. Учитывая необходимость приема атитромбоцитарных препаратов с целью вторичной профилактики у пациентов пожилого и старческого возраста в условиях COVID-19, вероятность обострения болевого синдрома в период самоизоляции с потребностью в краткосрочном применении НПВП, актуален вопрос профилактики осложнений со стороны ЖКТ. С этой целью широко рекомендуется и используются ингибиторы протонной помпы (ИПП) и ребамипид [29]. Однако применение ИПП лимитировано у пациентов пожилого и старческого возраста и в ряде случаев может рассматриваться их отмена [30]. Кроме того, ИПП не обеспечивают защиты от НПВП-индуцированных энтероколопатий. В качестве альтернативы может быть использован ребамипид, являющийся средством выбора и при НПВП-индуцированной энтероколопатии [29, 31]. Ребамипид восстанавливает защитный барьер не только слизистых ЖКТ, но и других слизистых оболочек, включая количественный и качественный состав слизи дыхательных путей, а также обладает потенциалом для снижения воспаления в легких путем ингибирования эпидермального фактора роста и снижения содержания провоспалительных цитокинов (интерлейкины: ИЛ-1, ИЛ-6, ИЛ-8, фактор некроза опухоли-альфа), способствует сохранению альвеолярного эпителия [32-35]. Эти данные дают возможность предполагать, что назначение ребамипида с целью лечения заболеваний ЖКТ/профилактики осложнений со стороны ЖКТ при назначении НПВП или антитромботической терапии, которая является неотъемлемой частью лечения пациентов с COVID-19
Особенности клинической картины COVID-19 у лиц пожилого и старческого возраста
Для лиц старших возрастных групп характерна атипичность проявления многих заболеваний, и COVID-19 не является исключением. Атипичная клиническая картина может быть связана с физиологическими изменениями в органах и системах организма, происходящих с возрастом, старческой астенией, сопутствующими заболеваниями [36], а также неспособностью пожилого человека предоставить точную информацию вследствие когнитивного снижения. В виду атипичных проявлений заболевания, у пациентов пожилого и старческого возраста может быть затруднена диагностика COVID-19.
Лихорадка и другие симптомы
К числу типичных симптомов COVID-19 относятся лихорадка (наблюдается в 9 из 10 случаев), слабость, сухой кашель, одышка, снижение вкуса и обоняния, дискомфорт в грудной клетке, озноб, диарея [1]. Наиболее распространенные типичные симптомы, такие как лихорадка, могут отсутствовать у пожилых людей [5]. Более того, симптомы COVID-19 могут быть легкими и не соответствовать тяжести заболевания и серьезности прогноза.
Лихорадка является наиболее частым симптомом COVID-19 и основным признаком для скрининга заболевших. При этом лихорадка отмечается более чем у 80% заболевших моложе 70 лет и только у 20-30% гериатрических пациентов [5, 37].
Лихорадка может быть недостаточно чувствительным признаком у пожилых людей, особенно при старческой астении, и часто отсутствует даже при серьезной инфекции в виду возраст ассоциированного физиологического снижения пиретического ответа. В связи с этим считается целесообразным использовать у людей пожилого возраста более низкий порог уровня температуры тела для диагностики лихорадки.
Американское общество по инфекционным болезням рекомендует применять следующее определение лихорадки у пациентов пожилого и старческого возраста при измерении температуры тела во рту: однократное повышение температуры 37,8° С и выше, или 2 повторных повышения 37,2° С и выше, или повышение температуры на 1,3° С по сравнению с обычной температурой тела. Для температуры в подмышечной впадине может использоваться порог 37,3° С [38, 39].
Атипичные симптомы COVID-19 у пациентов пожилого и старческого возраста включают делирий, падения, функциональное снижение, конъюнктивит. Могут наблюдаться тахипноэ, бред, тахикардия или снижение артериального давления [39, 40].
В виду атипичности проявлений COVID-19 пациенты пожилого возраста могут быть недооценены с точки зрения наличия у них этого заболевания и случайно помещены в обычное отделение, а не в специализированный стационар. Важно, чтобы медицинский персонал понимал возможность атипичных проявлений COVID-19 у пациентов пожилого и старческого возраста.
Делирий у пациентов с COVID-19
У пациентов пожилого и старческого возраста развитие делирия может быть манифестацией любого инфекционного процесса, включая COVID- 19 [41]. Делирий может наблюдаться у любого пациента старшего возраста с тяжелой инфекцией, респираторным дистресс-синдромом, при помещении в палату интенсивной терапии и на инвазивную искусственную вентиляцию легких (ИВЛ). Развитие делирия, особенно гиперактивной формы, может представлять собой дополнительные трудности и угрозы в контексте COVID-19. Стандартные нефармакологические меры профилактики и лечения делирия могут стать невозможным в условиях изоляции, при этом и сама изоляция может усугублять риск развития делирия и его течение.
В отношении делирия в условиях распространения COVID-19 актуальны две ключевые позиции. Во-первых, необходимо обеспечить высокое качество помощи и ухода, включая профилактику, раннее выявление и нефармакологическое ведение настолько, насколько это возможно в условиях системных мер противодействия распространению инфекции. Во-вторых, в условиях распространения COVID-19 риск причинения вреда другим людям
Таблица 2. Рекомендации по профилактике, выявлению и ведению делирия в условиях распространения COVID-19

Таблица 3. Лекарственные средства, которые могут быть использованы при фармакологическом лечении делирия у пациентов пожилого и старческого возраста [41]

может преобладать над индивидуальным риском. Это дает основание для более раннего использования фармакологического лечения в случаях потенциально опасного поведения пациента (таблицы 2, 3) [41].
Недостаточность питания (мальнутриция)
COVID-19 усугубляет риск развития недостаточности питания. Повышение этого риска связано как с клиническими симптомами заболевания (снижение обоняния и вкуса, снижение аппетита, диарея, лихорадка, слабость), так и с социальными факторами (самоизоляция), которые в ряде случаев потенцируют уже предсуществующие проблемы пожилого человека. Риск развития недостаточности с саркопенией питания значительно повышается при тяжелом течении заболевания, длительной госпитализации, при необходимости в продленной ИВЛ [8, 42].
Несмотря на то, что COVID-19 поражает прежде всего дыхательную систему, заболевание сопровождается мульти-органными проявлениями. Осложнения со стороны дыхательной системы могут потребовать пролонгированной ИВЛ. Пациенты старших возрастных групп с полиморбидностью a priori в большей степени подвержены риску мальнутриции и ассоциированной с ней саркопении, именно у этой группы прогноз при COVID-19 наиболее неблагоприятен [6, 7].
ИВЛ, особенно пролонгированная, является хорошо документированной причиной мальнутриции с потерей мышечной массы и функции, что в свою очередь ассоциировано в дальнейшем со снижением качества жизни и утратой автономности после выписки из отделения интенсивной терапии [42]. Многие хронические заболевания (СД, ССЗ, ХСН и их сочетание), собственно пожилой возраст ассоциированы с повышением риска недостаточности питания и ухудшением прогноза жизни. Причины мальнутриции, ассоциированные с помещением в палату интенсивной терапии и хроническим заболеваниями, включают снижение мобильности, катаболические изменения скелетной мускулатуры, снижение потребления пищи — все те факторы, к которым особенно чувствительны люди пожилого и старческого возраста. Помимо этого, воспаление и развитие септического состояния могут вносить вклад в усугубление этих нарушений при COVID-19. Адекватная оценка пищевого статуса и коррекция недостаточности питания эффективно снижают риск осложнений и улучшают клинические исходы в разных ситуациях, включая нахождение в блоке интенсив- ной терапии. Таким образом, меры по профилактике, диагностике и лечению недостаточности питания должны обязательно входить в план ведения пациентов пожилого и старческого возраста
Таблица 4. Валидированные инструменты скрининга недостаточности питания

c COVID-19 с целью улучшения кратко- и долго- срочного прогноза [6-8].
Оценка риска развития или наличия недостаточности питания должна производиться. Для этого рекомендуется проводить скрининг мальнутриции с использованием валидированных инструментов (таблица 4, приложение 2). Выбор инструмента зависит от ситуации: для амбулаторных пациентов предпочтительно использование опросников Краткая шкала оценки пищевого статуса (Mini Nutritional assessment, MNA), Универсальный скрининг недостаточности питания (MUST), для госпитализированных — Скрининг недостаточности питания (NRS-2002) [8].
Если по результатам скрининга пациент относится к категориям “риск недостаточности питания” или “недостаточность питания”, проводится дальнейший поиск потенциальных этиологических и фенотипических критериев недостаточности питания. Диагноз недостаточности питания устанавливается при наличии 1 этиологического и 1 фенотипического критерия (приложение 2).
Эксперты European Society of Clinical Nutrition and Metabolism (ESPEN) рекомендуют исходить их следующих расчетов при составлении плана коррекции недостаточности питания у пациентов пожилого и старческого возраста с COVID-19. Рекомендуется рассчитывать энергетическую ценность рациона пациента пожилого и старческого возраста, ориентируясь на уровень 30 ккал на кг массы тела в сут. [6, 7]. Энергетическая потребность в 30 ккал на кг массы тела в сут. является приблизительной оценкой и общим ориентиром для пожилых людей. Эта вели- чина должна корректироваться в индивидуальном порядке с учетом различных факторов, таких как пол, пищевой статус, ФА и клиническое состояние.
Пожилые люди по сравнению с молодыми нуждаются в большем количестве белка для оптимального сохранения безжировой массы тела, функции жизненно важных органов и качества жизни. Если для людей молодого и среднего возраста рекомендуется потребление белка 0,8 г на кг массы тела в сут., то для здоровых людей пожилого и старческого возраста суточный уровень потребления белка должен составлять не менее 1,0 г (1,0-1,2 г) на кг массы тела в сут. При наличии острого или хронического заболевания, сопровождающегося воспалением (включая системное воспаление у пожилых людей, инфекции, раны, пролежни и т.д.), потребность в белке может быть еще выше, и составлять 1,2-1,5 г/кг массы тела, а для людей пожилого и старческого возраста с серьезными заболеваниями или недостаточностью питания — до 2,0 г/кг массы тела в сут. [6-8, 43, 44]. Таким образом, принимая во внимание, что COVID-19 является заболеванием с высокой активностью воспаления, следует исходить из потребности в белке 1,2-1,5 г/кг массы тела в сут., в случаях тяжелого течения заболевания у пациента с мальнутрицией — 2,0 г/кг массы тела в сут.
У амбулаторных и госпитализированных пациентов пожилого и старческого возраста с COVID-19 и с недостаточностью питания или риском ее развития, рекомендуется применение ПЭП с целью оптимизации уровня потребления питательных веществ и снижения риска осложнений [8]. ПЭП обладают высоким содержанием калорий и питательных веществ и разработаны специально для обеспечения ежедневной потребности в питательных веществах, когда обычной диеты для этого не хватает. Разнообразие препаратов ПЭП по консистенции (жидкость, порошок, пудинг, предварительно сгущенные продукты), объема, состава (с высоким
Таблица 5. Тяжесть течения COVID-19

содержанием белка, с пищевыми волокнами), калорийности (от одной до трех ккал/мл) и вкусу обеспечивает потребности разных пациентов. Выделяют ПЭП с высоким содержанием белка, в которых он составляет ≥20% калорийности, и с высоким содержанием калорий, содержащие >1,5 ккал на мл или г. Рекомендуется назначать препараты ПЭП, которые обеспечивают поступление в организм энергии не менее 400 ккал/сут. и белка ≥20% энергетической ценности [6-8]. При отсутствии противопоказаний для обеспечения оптимального функционирования ЖКТ предпочтительны ПЭП, содержащие пищевые волокна. В настоящее время в России доступны препараты ПЭП, полностью соответствующие приведенным выше рекомендациям. Например, Фрезубин напиток 2 ккал содержит 400 ккал и 20 г белка (20%) в одном флаконе объемом 200 мл, а Фрезубин напиток 3,2 ккал содержит такое же количество энергии и белка в одном флаконе объемом 125 мл, что делает прием ПЭП у пациентов пожилого и старческого возраста значительно удобнее и повышает их приверженность. Кроме того, в каждом флаконе Фрезубин напиток 2 ккал и 3,2 ккал содержится 10 мкг витамина Д, что составляет ½ рекомендованной суточной дозы.
У госпитализированных пациентов пожилого и старческого возраста с COVID-19 зондовое энтеральное питание (ЗЭП) рекомендуется начинать без промедлений в тех случаях, когда пероральное питание невозможно в течение 3 дней, либо покрывает менее половины энергетической потребности на протяжении >1 нед. несмотря на меры в поддержку перорального приема пищи [6-8]. У пациентов с предполагаемой длительностью ЗЭП <4 нед. предпочтительно кормление через назогастральный зонд. Всех пациентов, находящихся на зондовом питании, рекомендуется стимулировать к продолжению перорального приема пищи, обеспечивая безопасность.
При выписке из стационара пациентам с недостаточностью питания или риском ее развития рекомендуется применять ПЭП с целью оптимизации уровня потребления пищи и массы тела, а также с целью уменьшения риска снижения функциональных возможностей. Рекомендуется назначать ПЭП на срок не менее 1 мес. и оценивать эффективность и ожидаемую пользу 1 раз в мес. [6-8].
Лечение пациентов пожилого и старческого воз- раста с COVID-19
Тактика лечения пациента с COVID-19 зависит от тяжести течения заболевания (таблица 5) и наличия осложнений. Пациентам с легким течением заболевания госпитализация обычно не требуется, однако возраст 65 лет и старше рассматривается в качестве одного из факторов риска неблагоприятного прогноза, учитываемого при оценке показаний для госпитализации. Терапия более тяжелых случаев COVID-19 направлена на предупреждение развития жизнеугрожающих состояний — тяжелой пневмонии, острого респираторного дистресс синдрома (ОРДС), тромботических осложнений.
Лечение пациентов пожилого и старческого возраста с COVID-19 пневмонией средней и более
Таблица 6. Биологические препараты, которые могут быть назначены в рамках клинического исследования для лечения COVID-19
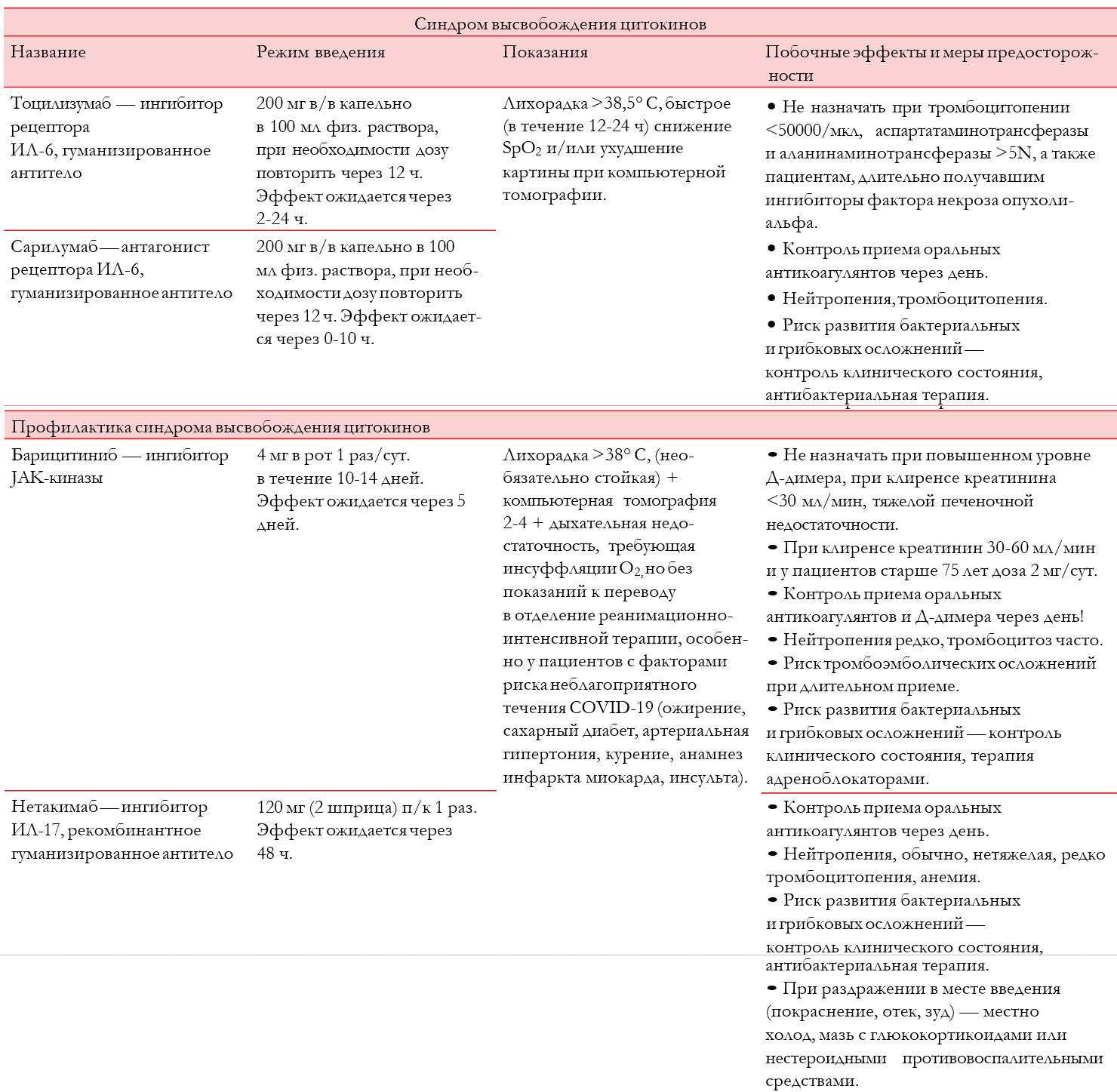
степени тяжести включает назначение этиотропной терапии, патогенетической и симптоматическую терапию. В текущих условиях распространения COVID-19 и ограниченности доказательной базы по лечению COVID-19, использование препаратов в режиме “off-label” для оказания медицинской помощи пациентам с COVID-19 базируется на международных рекомендациях, а также согласованных экспертных мнениях, основанных на оценке степени пользы и риска лечения.
Этиотропная терапия
В качестве этиотропной терапии используются хлорохин, гидроксихлорохин, лопинавир+ритонавир, азитромицин (в комбинации с гидроксихлорохином), препараты интерферонов. Следует отметить низкую доказанность эффективности применения этих препаратов для лечения COVID-19 у пациентов всех возрастных групп. Следует помнить об особой тщательности оценки потенциальной пользы и риска у пациентов пожилого возраста, необходимости оценки риска лекарственных взаимодействий и тщательного мониторинга безопасности терапии (интервала QTc, уровней калия и магния сыворотки, функции почек).
Противовоспалительная терапия
В патогенезе ОРДС вследствие COVID-19 основную роль играет избыточный ответ иммунной системы со стремительно развивающимся тяжелым жизнеугрожающим синдромом высвобождения цитокинов (“цитокиновым штормом”). У пациентов пожилого и старческого возраста вероятность развития синдрома высвобождения цитокинов ниже, чем у более молодых, что объясняется возраст-ассоциированными изменениями иммунной системы.
Цитокиновый шторм развивается как правило в период с 8 по 14 день заболевания. Признаками синдрома высвобождения цитокинов являются персистирование лихорадки >38° С в течение 5 дней без эффекта от жаропонижающих препаратов, уровень С-реактивного белка >60 мг/л или его рост в 3-4 раза на 8-14 день заболевания, лимфоциты <1×109/л и/или <15%, лейкоциты <3,0-3,5×109/л, ИЛ-6 >40 пк/мл, ферритин крови >1000 нг/мл. Наличие 2 и более перечисленных признаков у пациентов со стадией уплотнения легочной ткани по типу матового стекла в сочетании с очагами консолидации (КТ-3 поражения легких) и/или прогрессирующим снижением SpO2 является критерием для назначения биологических препаратов и/или ГКС (таблица 6) При назначении препаратов пациентам пожилого и старческого возраста следует с особой тщательностью оценивать риск нежелательных явлений и мониторировать безопасность терапии.
Антитромботическая терапия
Связанные с возрастом изменения системы гемостаза предрасполагают к повышению риска тромботических осложнений у пациентов пожилого и старческого возраста. Нарушения системы гемостаза характерны для COVID-19. В наиболее тяжелых случаях возникает диссеминированное внутрисосудистое свертывание и коагулопатия потребления [45, 46]. У пациентов с тяжелой COVID-19 отмечается высокая частота тромботических/тромбоэмболических осложнений в различных бассейнах сосудистого русла, преобладают венозные тромбозы над артериальными, а также выявляются признаки воспаления и микротромбозов в мелких сосудах, вероятно вследствие активации процессов иммунного воспаления и свёртывания крови [47- 51]. Остается не ясным, что является ли непосредственной причиной описанных нарушений — вирус SARS-CoV-2, прогрессирование инфекционного процесса или синдром высвобождения цитокинов. В лабораторных показателях отмечается повышение уровня D-димера, увеличение протромбинового времени, тромбинового времени и активированного частичного тромбопластинового времени, повышение концентрации фибриногена. По мере прогрессирования заболевания уровни фибриногена и антитромбина в крови могут снижаться. Нередко выявляется тромбоцитопения (обычно умеренная) или снижение числа тромбоцитов в динамике. Тромбоцитопения усугубляется при возникновении коагулопатии потребления [23, 45, 46]. Повышение уровня D-димера, отражающего как состоявшийся тромбоз, так и нарушения системы гемостаза в целом, ассоциировано с неблаго- приятным прогнозом COVID-19 [52], однако остается открытым вопрос об отрезных точках показателя, наиболее информативных для оценки тяжести заболевания и прогноза.
В целом, антитромботическая терапия при COVID-19 представляется патогенетически обоснованной.
Данных о целесообразности назначения антитромботической терапии для профилактики тромбоэмболических осложнений у пациентов, лечащихся по поводу COVID-19 дома (т.е. с легкими формами заболевания), нет. Однако с учетом особенностей патогенеза COVID-19 представляется, что назначение антитромботической терапии может рассматриваться у пациентов с высоким риском венозных тромбоэмболических осложнений (ВТЭО), невысоким риском кровотечений и не получающих антикоагулянты по другим показаниям. Это относится прежде всего к пациентам 70 лет и старше со значительно ограниченной мобильностью, анамнезом тромбоза глубоких вен/тромбоэмболии легочной артерии (ТГВ/ТЭЛА), с недавним (<1 мес. назад) оперативным вмешательством, активным злокачественным новообразованием [23, 45]. Важно подчеркнуть, что ни один из антикоагулянтов не одобрен в России для профилактики ТГВ/ТЭЛА у больных с острыми нехирургическими заболеваниями, которые лечатся вне стационара [23, 45]. Ключевой немедикаментозной мерой профилактики ТГВ/ТЭЛА у пациентов старших возрастных групп, которые находятся дома на режиме самоизоляции или лечатся дома с подозрением на COVID- 19 или с подтвержденной COVID-19, является адекватный режим ФА [45].
Экспертные сообщества едины во мнении, что всем госпитализированным пациентам с COVID-19, не имеющим противопоказаний, показано назначение низкомолекулярного гепарина, как минимум, в профилактических дозах [23, 45] (таблица 7). Рекомендации по широкому применению промежуточных или лечебных доз противоречивы. При этом данные о высокой частоте тромбоэмболических осложнений у пациентов, получающих профилактические дозы антикоагулянтов, появление данных об ассоциации применения лечебных доз антикоагулянтов с улучшением исходов у пациентов с тяжелой COVID-19, в т.ч. находящихся на ИВЛ, позволяют обсуждать перспективы более агрессивной тактики антикоагулянтной терапии [53, 54].
Антикоагулянты противопоказаны при продолжающемся кровотечении, уровне тромбоцитов в крови ниже 25×109/л. Следует учитывать ограничения по применению и необходимость коррекции
Таблица 7. Дозы антикоагулянтов для парентерального введения [23]

дозы низкомолекулярного гепарина при клиренсе креатинина ниже 15-30 мл/мин в зависимости от препарата, а также у больных с быстро меняющейся функцией почек. При тяжелой почечной недостаточности рекомендуется применение внутривенной инфузии нефракционированного гепарина [23, 45, 46].
При коагулопатии потребления и отсутствии кровотечений рекомендуется поддерживать уровень тромбоцитов выше 20×109/л, фибриногена — выше 1,5-2,0 г/л. При кровотечении или необходимости инвазивных процедур рекомендуется поддерживать уровень тромбоцитов выше 50×109/л, фибриногена — выше 1,5-2,0 г/л, протромбиновое отношение <1,5 за счет введения недостающих компонентов крови [23, 45, 46].
Решение о применении антиагрегантов принимается индивидуально с учетом риска коронарного тромбоза и кровотечений. У пациентов с недавним острым коронарным синдромом, а также в первые 3 мес. после коронарного стентирования рекомендуется продолжить двойную антитромбоцитарную терапию [23, 45], однако следует учитывать риск лекарственных взаимодействий с другими препаратами, применяющимися для лечения COVID-19 (таблица 8). На фоне лечения необходимо контролировать число тромбоцитов. При предполагаемом или несомненном диссеминированном внутрисосудистом свертывании антиагреганты желательно отменить, однако если это неприемлемо и нет кровотечений, можно рассмотреть продолжение двойной антитромбоцитарной терапии при уровне тромбоцитов в крови ≥50×109/л, переход на монотерапию при уровне от 25×109/л до <50×109/л и отмену антиагрегантов при уровне <25×109/л [23, 45]. Принимая во внимание тот факт, что риск кровотечений у пациентов пожилого и старческого возраста усугубляется гипоксией, представляется целесообразным использованием ингибиторов протонной помпы, ребамипида или их комбинации при назначении антитромботической терапии, учитывая риск лекарственных взаимодействий при выборе препарата. Ребамипид может оказывать дополнительные защитные и системные противовоспалительные эффекты [29, 32-35, 55].
Таблица 8. Лекарственные взаимодействия антитромботических и препаратов для лечения пациентов с COVID-19 [56]
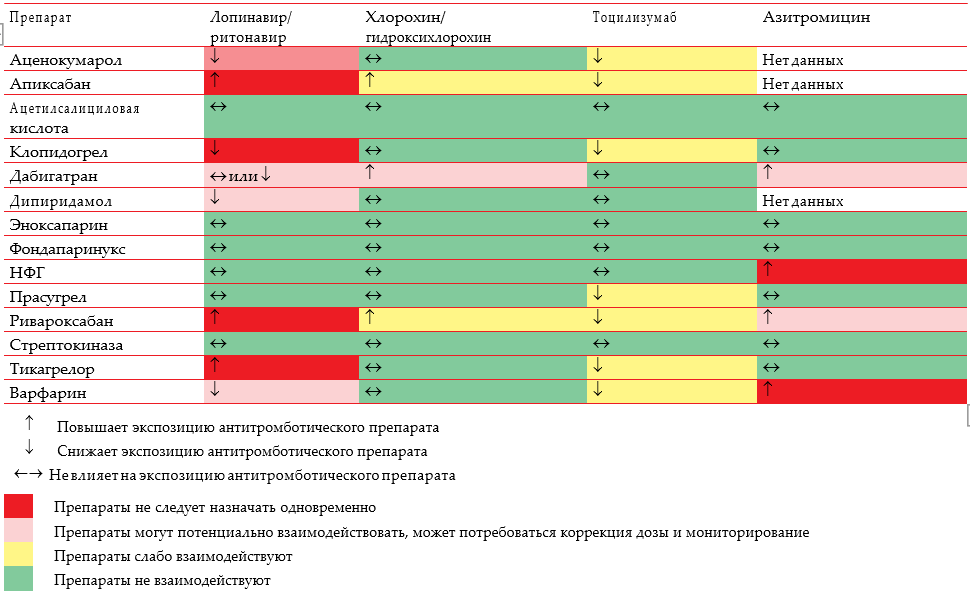
Целесообразность продолжения профилактики ВТЭО после выписки у пациентов с COVID-19 не изучена. Однако с учетом данных клинических исследований у пациентов, выписанных после острых нехирургических заболеваний, продлённая профилактика может быть оправдана при сохраняющемся повышенном риске ВТЭО и невысоком риске кровотечений в случаях, когда не требуются лечебные дозы антикоагулянтов по другим показаниям [23, 45]. В виду того, что возраст является одним из факторов, учитываемых при определении риска ВТЭО, пациенты пожилого и старческого возраста являются потенциальными кандидатами для продленного (вплоть до 45 дней) применения профилактических доз антикоагулянтов после выписки из стационара, особенно, если у них ограничена подвижность, имеется ВТЭО в анамнезе, активное злокачественное новообразование, тяже- лая сердечная недостаточность. Вероятно, что сохранение повышенного уровня D-димера, превышающего верхнюю границу нормы в ≥2 раза к моменту выписки, можно рассматривать в качестве дополнительного аргумента к продлению терапии антикоагулянтами [23, 45]. Польза продленной профилактики ВТЭО у терапевтических больных высокого риска продемонстрирована при использовании эноксапарина (подкожно 40 мг 1 раз/сут.), ривароксабана (внутрь 10 мг 1 раз/сут.) [23]. Однако следует подчеркнуть, что эффективность этих препаратов при COVID-19 не изучалась и ни один из них не одобрен в России для продленной профилактики ТГВ/ТЭЛА у больных с острыми нехирургическими заболеваниями после выписки из стационара. Всех пациентов надо поощрять к расширению ФА [23, 45, 57].
После возникновения ТГВ/ТЭЛА у больных COVID-19 следует продолжать использовать лечебные дозы антикоагулянтов в течение 3-6 мес. (при отсутствии противопоказаний рекомендуется пред- почесть прямые пероральные антикоагулянты) [23]. Пациенты с другими показаниями к длительной антикоагулянтной терапии (ФП, механические протезы клапанов сердца, другие тромботические/ тромбоэмболические осложнения) после выписки из стационара должны продолжать прием антикоагулянтов в рекомендованных ранее дозах [23, 57].
Оценка гериатрического статуса в принятии решений
При оказании медицинской помощи пациентам пожилого и старческого возраста с COVID-19 неизбежно встают вопросы: насколько агрессивной может быть тактика ведения, направленная на продление жизни? Следует ли пациента помещать
Таблица 9. Клиническая шкала старческой астении

Примечание: ФА - физическая активность
в отделение интенсивной терапии? Следует ли пациент помещать пациента на ИВЛ? Перенесет ли пациент инвазивные вмешательства, направленные на поддержание или спасение жизни, на фоне полиорганной недостаточности?
Интенсивной терапии может быть подвергнут пациент, у которого ожидается хорошее или приемлемое состояние здоровья и качество жизни после выписки. Вмешательство считается диспропорционально избыточным, если инвазивные процедуры, направленные на поддержание жизни, применяются у пациентов старшего возраста с плохим прогнозом в виду хронической органной дисфункции, коморбидности и/или плохим качеством жизни [58, 59]. Диспропорционально избыточного вмешательства следует избегать всегда, не только во время текущей эпидемии, когда потребность в реанимационных койках и нагрузка на них чрезвычайно высоки. В странах, где это закреплено законодательно, вопросы интенсивности вмешательства у людей старшего возраста могут быть решены при перспективном планирования ухода: пациент, еще находясь в приемлемом состоянии здоровья и когнитивного статуса, может заранее сделать распоряжения о том, насколько интенсивному вмешательству он желает быть подвержен, в т.ч. в ситуациях развития состояний, угрожающих жизни.
Возраст не является единственным фактором, который определяет тактику и интенсивность вмешательства, а также решение о помещении пациента в отделение реанимации и на ИВЛ [60, 61]. В этом контексте крайне важна предшествующая оценка гериатрического статуса пациента, использование инструментов для быстрой его оценки, например, клинической шкалы старческой астении (таблица 9). Однако при применении этой шкалы следует помнить об ограничениях оценки старческой астении на основании только одного метода.
Таблица 10. Оценка возраста

Необходимо подчеркнуть, что клиническая шкала старческой астении не должна использоваться изолированно [60].
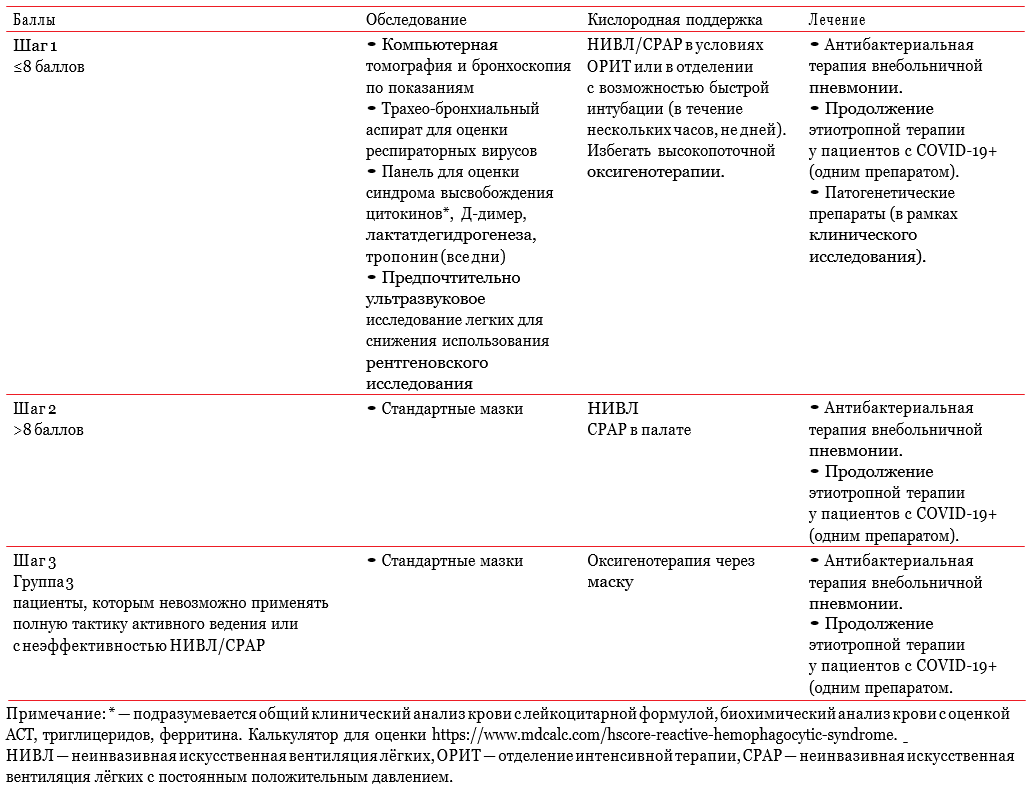
Принятие решения о помещении пациента пожилого и старческого возраста в отделение интенсивной терапии может быть основано на оценке трех доменов: возраста (таблица 10), старческой астении (таблица 9), коморбидности (таблица 11). Такой подход была предложена британскими клиницистами. Баллы, полученные при оценке факторов, перечисленных в таблицах 9-11, суммируются. У женщин из полученного результата вычитается 1 балл. Тактика обследования и ведения представлена в таблицах 12 и 13. Если пациент набирает 8 баллов и менее, то он может быть переведен в отделение реанимации и помещен на ИВЛ, в дальнейшем может рассматриваться экстракорпоральная мембранная оксигенация (ЭКМО). Таким пациентам рекомендуется оценивать критерии развития синдрома высвобождения цитокинов. Если пациент пожилого/старческого возраста набирает >8 баллов, тактика ведения должна быть менее агрессивной [60].
Определение тактики ведения с учетом клинической шкалы старческой астении применимо и в ситуациях, когда пациент находится в доме престарелых [61]. В домах престарелых Бельгии принят следующий протокол действий. При подозрении на COVID-19 оценивается гериатрический статус и критерии тяжести течения COVID-19: нарушение сознания, снижение SpO2 <90% у пациента без ХОБЛ, частота дыхательных движений (ЧДД) >25 в мин, увеличение частоты сердечных сокращений >100 уд./мин, снижение систолического АД (САД) <100 мм рт.ст. Если пациент относится к 1-6 группе старческой астении и имеет не более одного критерия, пациент должен быть изолирован, а медицинская помощь, включающая назначение антибактериальной терапии внебольничной пневмонии, оксигенотерапии со скоростью подачи кислорода до 3 л в мин, может быть оказана в условиях дома престарелых. При неэффективности в течение 48 ч, с учетом распоряжений/пожеланий пациента (или опекунов, если пациента недееспособен) принимается решение о госпитализации или оказании
Таблица 11. Оценка коморбидных состояний

паллиативной помощи. Если же у такого пациента присутствует 2 и более критерия тяжести, пациент госпитализируется (если ранее он не сделал иных распоряжений). Пациентам, относящимся к 7 группе старческой астении, может быть оказана паллиативная помощь (по решению резидента) или после консультации гериатра назначено лечение, направленное на продление жизни (например, антибактериальная терапия), и уход, если это не ухудшает качество жизни пациента. Интенсивная терапия таким пациентам не показана. Пациентам 8 и 9 групп старческой астении оказывается паллиативная помощь.
Меры по предотвращению распространения COVID-19 в домах престарелых
В начале развития пандемии COVID-19 в странах Европы и Северной Америки превентивные меры касались в первую очередь тех, кто проживает дома, в то время как рискам распространения вируса в домах престарелых уделялось меньше внимания [62]. Учитывая особенности организации ухода за такими людьми (совместное проживание, прием пищи, приходящий персонал и т.п.), отсутствие системного подхода обернулось быстрым распространения вируса. Поскольку жители домов престарелых — преимущественно люди с множеством заболеваний, смертность в этих организациях стала вносить существенный вклад в общую смертность от коронавируса. По данным Всемирной организации здравоохранения от 23 апреля 2020г до половины смертей от COVID-19 в Европе приходилось на дома престарелых [62, 63].
Таблица 12. Тактика ведения зависимости от результата оценки

Таблица 13. Обследование и лечение
Среди основных причин быстрого развития критических ситуаций в учреждениях ухода можно отметить:
● Контакты пациентов с обслуживающими персоналом и родными, которые оказались вирусоносителями.
● Заражение пациентов в медицинских учреждения во время экстренных и плановых госпитализаций.
● Быстрое распространение вируса в закрытом пространстве учреждения.
● Позднее выявление случаев заболевания, в т.ч. из-за бессимптомного течения у носителей COVID-19, а также дефицита сотрудников.
Более старший возраст пациентов домов престарелых и сопутствующие хронические заболевания, которые стали дополнительным фактором повышенной смертности.
Меры по предупреждению распространения COVID-19 в домах престарелых должны охватывать несколько направлений:
1) общие мероприятия по поддержке домов престарелых в условиях пандемии и подготовка к возможным вспышкам заболеваний;
2) меры, позволяющие предотвратить проникновение COVID-19 в учреждения социального обслуживания;
3) меры, связанные с мониторингом эпидемиологической ситуации в домах престарелых;
4) меры по борьбе с COVID-19 после выявления заболевших в учреждениях;
5) меры, призванные облегчить доступ к медицинской помощи для пациентов учреждений социального обслуживания с COVID-19;
6) меры, направленные на преодоление дефицита кадров;
7) мероприятия, компенсирующие негативные последствия физического дистанцирования в домах престарелых [62].
Конкретные меры включают ограничение или полное прекращение посещений в домах престарелых, об обязательном использовании средств индивидуальной защиты персоналом, об изоляции людей с подозрением/подтвержденным диагнозом COVID-19 или с симптомами острой респираторной вирусной инфекции, регулярном мониторинге симптомов COVID-19 у сотрудников и проживающих, организацию регулярного тестирования на COVID-19, карантине для пациентов, возвращающихся из медицинских учреждений. При реализации мер важен межведомственный подход, координация решений на всех уровнях (национальном, региональном и местном), интеграции ухода с гарантированным доступом к медицинским услугам и паллиативной помощи, своевременном принятии мер, позволяющих предотвратить возникновение очагов инфицирования COVID-19 в домах престарелых и в целом — о проактивных действиях в данной сфере [62]. Меры профилактики коронавирусной инфекции должны предприниматься не только в государственных учреждениях, но и в частных структурах, количество которых значительно выросло в последние годы в связи с растущей потребностью в уходе и ограниченными возможностями государственного социального обслуживания, а стандарты ухода в них широко варьируют.
Роль врача-гериатра в ведении пациентов пожилого и старческого возраста с COVID-19
Медицинская помощь пациентам пожилого и старческого возраста, госпитализированным c COVID-19, оказывается, как правило, мультидисциплинарной командой, включающей врачей-терапевтов, пульмонологов и анестезиологов реаниматологов. В идеале врач-гериатр должен быть членом этой команды для определения оптимальной тактики ведения пациента с учетом мультиморбидности, степени сохранности автономности и когнитивных функций, наличия сенсорных дефицитов и эмоциональных особенностей. Важно, что врачи-гериатры лучше врачей многих специальностей знают и умеют использовать принципы командной работы и действовать в соответствии с потребностями пациента в тесном сотрудничестве с другими специалистами, средним медицинским персоналом, социальными работниками и членами семьи пациента. Роль врача- гериатра важна на стационарном этапе для профилактики, диагностики и лечения гериатрических синдромов, прежде всего, недостаточности питания и делирия. После выписки из стационара врач-гериатр может разработать индивидуальный план ведения, направленный на сохранение автономности пациента и поддержание его качества жизни.
Отношения и деятельность: авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Литература
- Chinese Center for Control and Prevention. http://www.chinacdc. cn/en/COVID19/
- Vital Surveillances: The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19) — China, 2020 http://weekly.chinacdc.cn/en/article/id/e53946e2- c6c4-41e9-9a9b-fea8db1a8f51
- Remuzzi A, Remuzzi G. COVID-19 and Italy: what next? Lancet. 2020 11-17 April; 395(10231):1225-8. doi:10.1016/S0140- 6736(20)30627-9.
- Porcheddu R, Serra C, Kelvin D, et al. Similarity in Case Fatality Rates (CFR) of COVID-19/SARS-COV-2 in Italy and China J Infect Dev Ctries. 2020 Feb 29;14(2):125-8. doi:10.3855/jidc.12600.
- Liu K, Chen Y, Lin R, Han K. Clinical feature of COVID-19 in elderly patients: a comparison with young and middle-aged patients. J Infect. 2020 Mar 11. pii: S0163- 4453(20)30116-X. doi:10.1016/j. jinf.2020.03.005.
- Gomes F, Schuetz P, Bounoure L, et al. ESPEN guideline on nutritional support for polymorbid internal medicine patients. Clin Nutr 2018;37:336-53. doi:10.1016/j.clnu.2017.06.025.
- Volkert D, Beck AM, Cederholm T, et al. ESPEN guideline on clinical nutrition and hydration in geriatrics. Clin Nutr 2019;38:10- 47. doi:10.1016/j.clnu.2018.05.024.
- Barazzoni R, Bischoff SC, Krznaric Z, endorsed by the ESPEN Council. Espen expert statements and practical guidance for nutritional management of individuals with Sars-cov-2 infection. Clinical Nutrition. 2020;39(6):1631-1638. doi:10.1016/j. clnu.2020.03.022.
- Tkacheva ON, Kotovskaya YV, Runikhina NK, et al. Clinical guidelines frailty. Part 2. Russian Journal of Geriatric Medicine. 2020;(2):115-30. (In Russ.) Ткачева О. Н., Котовская Ю. В., Рунихина Н. К., и др. Клинические рекомендации “Старческая астения”. Часть 2. Российский журнал гериа-трической медицины. 2020;(2):115-30. doi:10.37586/2686- 8636-2-2020-115-130.
- Naumov AV, Tkacheva ON. What can apply for the role of basic therapy for chronic pain in comorbid patients? Meditsinskiy sovet Medical Council. 2018;(6):120-6. (In Russ.) Наумов А. В., Ткачева О. Н. Что может претендовать на роль базис- ной терапии хронической боли у коморбидных больных? Медицинский Совет. 2018;(6):120-6. doi:10.21518/2079- 701X-2018-6-120-126.
- Grant WB, Lahore H, McDonnell SL, et al. Evidence That Vitamin D Supplementation Could Reduce Risk of Influenza and COVID-19. Nutrients. 2020 Apr 2;12(4):E988. doi:10.3390/nu12040988.
- Poudel-Tandukar K, Poudel KC, Jimba M, et al. Serum 25-hydroxyvitamin d levels and C-reactive protein in persons with human immunodeficiency virus infection. AIDS Res. Hum. Retrovir. 2013;29:528-34. doi:10.1089/AID.2012.0120.
- Zhang M, Gao Y, Tian L, et al. Association of serum 25-hydroxyvitamin D3 with adipokines and inflammatory marker in persons with prediabetes mellitus. Clin. Chim. Acta. 2017;468:152- 8. doi:10.1016/j.cca.2017.02.022.
- Dancer RC, Parekh D, Lax S, et al. Vitamin D deficiency contributes directly to the acute respiratory distress syndrome (ARDS). Thorax. 2015;70:617-24. doi:10.1136/thoraxjnl-2014-206680.
- Thickett DR, Moromizato T, Litonjua AA, et al. Association between prehospital vitamin D status and incident acute respiratory failure in critically ill patients: A retrospective cohort study. BMJ Open Respir. Res. 2015;2:e000074. doi:10.1136/ bmjresp-2014-000074.
- Wimalawansa SJ. Global epidemic of coronavirus — COVID-19: What we can do to minimize risks. Eur. J. Biomed. Pharm. Sci. 2020;7:432-8.
- Driggin E, Madhavan MV, Bikdeli B, et al. Cardiovascular Considerations for Patients, Health Care Workers, and Health Systems During the COVID-19 Pandemic. J Am Coll Card Mar. 2020 May 12;75(18):2352-71. doi:10.1016/j.jacc.2020.03.031.
- Rossi GP, Sanga V, Barton M. Elife Potential harmful effects of discontinuing ACE-inhibitors and ARBs in COVID-19 patients. 2020 Apr 6;9:e57278. doi:10.7554/eLife.57278.
- Danser AHJ, Epstein M, Batlle D. Renin-Angiotensin System Blockers and the COVID-19 Pandemic. At Present There Is No Evidence to Abandon Renin-Angiotensin System Blockers Hypertension. 2020;75:1382-5.
- HFSA/ACC/AHA Statement Addresses Concerns Re: Using RAAS Antagonists in COVID-19. ttps://www.acc.org/latest-in- cardiology/articles/2020/03/17/08/59/hfsa-acc-aha-statement- addresses-concerns-re-using-raas-antagonists-in-COVID-19.
- Liu Y, Huang F, Xu J, et al. Anti-hypertensive Angiotensin II receptor blockers associated to mitigation of disease severity in elderly COVID-19 patients. medRxiv 2020.03.20.20039586; doi:10.1101/ 2020.03.20.20039586.
- Zhang P, Zhu L, Cai J, et al. Association of Inpatient Use of Angiotensin Converting Enzyme Inhibitors and Angiotensin II Receptor Blockers with Mortality Among Patients With Hypertension Hospitalized With COVID-19. Circulation Research. 2020. doi:10.1161/circresaha.120.317134.
- Arutyunov GP, Koziolova NA, Tarlovskaya EI, et al. Consensus of experts of the Eurasian Association of therapists on some new mechanisms of COVID-19 pathogenesis: focus on hemostasis, issues of hemotransfusion and blood gas transport system. Kardiologiya. 2020;60(6). (In Russ.) Арутюнов Г. П., Козиолова Н. А., Тарловская Е. И., и др. Согласованная позиция экспертов Евразийской ассоциации терапевтов по некоторым новым механизмам патогенеза COVID-19: фокус на гемостаз, вопросы гемотрансфузии и систему транспорта газов крови. Кардиология. 2020;60(6). doi:10.18087/cardio.2020.5.n1132.
- Gupta R, Ghosh A, Singh AK, Misra F. Clinical Considerations for Patients With Diabetes in Times of COVID-19 Epidemic. Diabetes Metab Syndr. 2020;14(3):211-2. doi:10.1016/j.dsx.2020.03.002.
- Zhao Q, Meng M, Kumar R, et al. The Impact of COPD and Smoking History on the Severity of Covid-19: A Systemic Review and Meta- Analysis. J Med Virol. 2020 Apr 15. doi:10.1002/jmv.25889.
- Tal-Singer R, Crapo JD. COPD at the time of COVID-19: a COPD Foundation perspective. Chronic Obstr Pulm Dis. 2020;7(2):73-5. doi:10.15326/jcopdf.7.2.2020.0149.
- Updated: WHO Now Doesn’t Recommend Avoiding Ibuprofen For COVID-19 Symptoms. https://www.sciencealert.com/who- recommends-to-avoid-taking-ibuprofen-for-covid-19-symptoms.
- EMA gives advice on the use of non-steroidal anti-inflammatories for COVID-19. https://www.ema.europa.eu/en/news/ema-gives- advice-use-non-steroidal-anti-inflammatories-covid-19.
- Hunt R, Lazebnik LB, Marakhouski YC, et al. International Consensus on Guiding Recommendations for Management of Patients with Nonsteroidal Anti-inflammatory Drugs Induced Gastropathy-ICON-G. Euroasian J Hepatogastroenterol, 2018;8(2):148-60.
- Tkacheva ON, Ostroumova OD, Kotovskaya YuV, et al. Deprescribing of proton pump inhibitors in elderly and senile patients. Clinical pharmacology and therapy. 2019;28(1):70-4. (In Russ.) Ткачева О. Н., Остроумова О. Д., Котовская Ю. В., и др. Депрескрайбинг ингибиторов протонной помпы у пациентов пожилого и старческого возраста. Клиническая фармакология и терапия. 2019;28(1):70-4. doi:10.32756/0869-5490-2019-1- 70-74.
- Zhang S, Qing Q, Bai Y, et al. Rebamipide helps defend against nonsteroidal anti-inflammatory drugs induced gastroenteropathy: a systematic review and meta-analysis. Dig Dis Sci. 2013 Jul;58(7):1991-2000. doi:10.1007/s10620-013-2606-0.
- Tajima K, Hattori T, Takahashi H, et al. Rebamipide suppresses TNF-α production and macrophage infiltration in the conjunctiva. Vet Ophthalmol. 2018 Jul;21(4):347-52. doi:10.1111/vop.12510. Epub 2017 Dec 18.
- Fukuda K, Ishida W, Tanaka H, et al. Inhibition by rebamipide of cytokine-induced or lipopolysaccharide-induced chemokine synthesis in human corneal fibroblasts. Br J Ophthalmol. 2014 Dec;98(12):1751-5. doi:10.1136/bjophthalmol-2014-305425.
- Fu R, Jiang Y, Zhou J, Zhang J. Rebamipide ophthalmic solution modulates the ratio of T helper cell 17/regulatory T cells in dry eye disease mice. Mol Med Rep. 2019 May;19(5):4011-8. doi:10.3892/mmr.2019.10068.
- Lee SY, Kang EJ, Hur GY, et al. The inhibitory effects of rebamipide on cigarette smoke-induced airway mucin production. Respir Med, 2006;100(3):503-11. doi:10.1016/j.rmed.2005.06.006.
- Clerkin KJ, Fried JA, Raikhelkar J, et al. Coronavirus Disease 2019 (COVID-19) and Cardiovascular Disease. Circulation 2020; doi:10.1161/CIRCULATIONAHA.120.046941.
- Сhen N, Zhou M, Dong X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. The Lancet. 2020;395(10223):507-5.
- Norman DC. Fever in the elderly. Clinical Infectious Diseases. 2000;31(1):148-51 doi:10.1086/313896.
- Shahid Z, Kalayanamitra R, McClafferty B, et al.COVID-19 and Older Adults: What We Know. J Am Geriatr Soc. 2020 May;68(5):926-9. doi:10.1111/jgs.16472.
- Atypical Covid-19 presentations in older people — the need for continued vigilance. https://www.bgs.org.uk/blog/atypical-covid-19-presentations-in-older-people-the-need-for-continued- vigilance.
- Coronavirus: Managing delirium in confirmed and suspected cases. https://www.bgs.org.uk/resources/coronavirus- managing-delirium-in-confirmed-and-suspected-cases.
- Singer P, Blaser AR, Berger MM, et al. ESPEN guideline on clinical nutrition in the intensive care unit. Clin Nutr. 2019;38:48-79. doi:10.1016/j.clnu.2018.08.037.
- Bauer J, Biolo G, Cederholm T, et al. Evidence-based recommendations for optimal dietary protein intake in older people: a position paper from the PROT-AGE Study Group. J Am Med Dir Assoc. 2013;14(8):542-59. doi:10.1016/j.jamda.2013.05.021.
- Deutz NE, Bauer JM, Barazzoni R, et al. Protein intake and exercise for optimal muscle function with aging: recommendations from the ESPEN Expert Group. Clin Nutr. 2014;33(6):929-36. doi:10.1016/j. clnu.2014.04.007.
- Bikdeli B, Madhavan MV, Jimenez D, et al. COVID-19 and Thrombotic or Thromboembolic Disease: Implications for Prevention, Antithrombotic Therapy, and Follow-up. JACC. 2020; doi:10.1016/j.jacc.2020.04.031.
- Thachil J, Tang N, Gando S, et al. ISTH interim guidance on recognition and management of coagulopathy in COVID‐19. J Thromb Haemost. 2020;18(5):1023-1026. doi:10.1111/jth.14810.
- Dolhnikoff M, Duarte-Neto AN, Monteiro RAA, et al. Pathological evidence of pulmonary thrombotic phenomena in severe COVID- 19. J Thromb Haemost. 2020; doi:10.1111/JTH.14844.
- Carsana L, Sonzogni A, Nasr A. Pulmonary post-mortem findings in a large series of COVID-19 cases from Northern Italy. doi:10.11 01/2020.04.19.20054262.
- Helms J, Tacquard C, Severac F, et al. High risk of thrombosis in patients with severe SARS-CoV-2 infection: a multicenter prospective cohort study. Intensive Care Med. 2020;1-10. doi:10.1007/s00134-020-06062-x
- Klok F, Kruip M, van der Meer NJM, et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb Res. 2020;191:145-147. doi:10.1016/j.thromres.2020.04.013.
- Menter T, Haslbauer J, Nienhold R, et al. Post-mortem examination of COVID19 patients reveals diffuse alveolar damage with severe capillary congestion and variegated findings of lungs and other organs suggesting vascular dysfunction. Histopathology. May 2020. doi:10.1111/his.14134. Online ahead of print.
- Tang N, Li D., Wang X, Sun Z. Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J Thromb Haemost. 2020;18:844-7. doi:10.1111/jth.14768.
- Llitjos J, Leclerc M, Chochois C, et al. High incidence of venous thromboembolic events in anticoagulated severe COVID-19 patients. J Thromb Haemost. April 2020. doi:10.1111/jth.14869.
- Paranjpe I, Fuster V, Lala A, et al. Association of Treatment Dose Anticoagulation with In-Hospital Survival Among Hospitalized Patients with COVID-19. Journal of the American College of Cardiology. May 2020. doi:10.1016/j.jacc.2020.05.001.
- KoyamaN,SasabeH,Miyamoto G. InvolvementofCytochromeP450 in the Metabolism of Rebamipide by the Human Liver. Xenobiotica. 2002 Jul;32(7):573-86. doi:10.1080/00498250210130591.
- Liverpool Drug Interaction Group. Interactions with Experimental COVID-19 Therapies. https://www.covid19-druginteractions.org.
- Кonstantinides SV, Meyer G, Becattini C, et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). The Task Force for the diagnosis and management of acute pulmonary embolism of the European Society of Cardiology (ESC). Eur Heart J. 2020;41:543-603. doi:10.1093/eurheartj/ehz405.
- Kompanje EJO, Piers RD, Benoit DD. Causes and consequences of disproportionate care in intensive care medicine. Curr Opin Crit Care. 2013;19:630-35. doi:10.1097/MCC.0000000000000026.
- EuGMS Task Force on COVID-19. Topic 4. Ethical principles concerning proportionality of critical care during the 2020 COVID- 19 pandemic in Belgium: advice by the Belgian Society of Intensive care medicine. https://www.eugms.org.
- COVID-19 rapid guideline: critical care in adults. https://www.nice. org.uk/guidance/ng159.
- Kunz R, Minder M. COVID-19 pandemic: palliative care for elderly and frail patients at home and in residential and nursing homes. Swiss Med Wkly. 2020 Mar 24;150:w20235. doi:10.4414/ smw.2020.20235. eCollection 2020 Mar 23.
- Analytical bulletin of the higher school of economics on the economic and social consequences of coronavirus in Russia and in the world, dated May 14, 2020. (In Russ.) Аналитический бюллетень НИУ ВШЭ об экономических и социальных послед- ствиях коронавируса в России и в мире от 14 мая 2020 г. https://www.hse.ru/mirror/pubs/share/364606313.pdf.
- Statement — Invest in the overlooked and unsung: build sustainable people-centred long-term care in the wake of COVID-19. http://www.euro.who.int/en/media-centre/sections/ statements/2020/statement-invest-in-the-overlooked-and- unsung-build-sustainable-people-centred-long-term-care-in- the-wake-of-covid-19.
Комментарии • 0
Чтобы оставить комментарий, пожалуйста, войдите на портал