1. Чучалин А.Г., Синопальников А.И., Козлов Р.С., и соавт. Внебольничная пневмония у взрослых. Практические рекомендации по диагностике, лечению и профилактике (пособие для врачей). Клин микробиол антимикроб химиотер 2010; 12: 186-225.
2. Рачина С.А., Синопальников А.И. Инфекционные заболевания нижних дыхательных путей. В кн.: Основы внутренней медицины. Под ред. В.С. Моисеева, Ж.Д. Кобалава, И.В. Маева и соавт. - М.: МИА, 2020, 2-е изд. Т.1. С.147-171.
3. American Thoracic Society/Infectious Diseases Society of America. Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. Am J Respir Crit Care Med 2005; 171:388–416.
4. Chalmers J.D., Rother C., Salih W., et al. Healthcare-associated pneumonia does not accurately identify potentially resistant pathogens: a systematic review and meta-analysis. Clin Infect Dis 2014; 58:330–9.
5. Gross A.E.,Van Schooneveld T.C., Olsen K.M., et al. Epidemiology and predictors of multidrug-resistant community-acquired and health care-associated pneumonia. Antimicrob Agents Chemother 2014; 58:5262–8.
6. Yap V., Datta D., Metersky M.L. Is the present definition of health care-associated pneumonia the best way to define risk of infection with antibiotic-resistant pathogens? Infect Dis Clin North Am 2013; 27:1–18.
7. orres A., Blasi F., Peetermans W.E., et al. The aetiology and antibiotic management of community-acquired pneumonia in adults in Europe: a literature review. Eur J Clin Microbiol Infect Dis 2014;33(7):1065-79.
8. Johansson N., Kalin M., Tiveljung-Lindell A., et al. Etiology of community-acquired pneumonia: increased microbiological yield with new diagnostic methods. Clin Infect Dis 2010;50:202–209.
9. Рачина С.А., Козлов Р.С., Шаль Е.П., и соавт. Структура бактериальных возбудителей внебольничной пневмонии в многопрофильных стационарах г. Смоленска. Пульмонология 2011; 1: 5-18.
10. Rachina S, Zakharenkov I, Dekhnich N, et al. Aetiology of severe community-acquired pneumonia and antimic-robial resistance of Steptococcus pneumoniae in adults in Russia. J Antimicrob Chemother. 2021 Feb 19:dkab014. doi: 10.1093/jac/dkab014.
11. Mandell L.M., Wunderink R.G, Anzueto A., et al. Infectious Diseases Society of America/American Thoracic Society Consensus Guidelines on the Management of Community-Acquired Pneumonia in Adults. Clin Infect Dis 2007; 44 (Suppl 2): S27-72.
12. Athlin S., Lidman C., Lundqvist A., et al. Management of community-acquired pneumonia in immunocompetent adults: updated Swedish guidelines 2017. Infect Dis (Lond) 2018;50(4):247-272.
13. Климко Н.Н., Васильева Н.В. Микозы легких. В кн.: Респираторная медицина. Под ред. А.Г. Чучалина М.: ГЭОТАР-Медиа. 2007. Т. 1, С. 549-576.
14. Pavia A.T. What is the Role of Respiratory Viruses in Community-Acquired Pneumonia? What is the Best Therapy for Influenza and Other Viral Causes of Community-Acquired Pneumonia? Infect Dis Clin N Am 2013; 27: 157–175.
15. Choi S.H., Hong S.B., Ko G.B., et al. Viral infection in patients with severe pneumonia requiring intensive care unit admission. Am J Respir Crit Care Med 2012;186: 325–332.
16. Bjarnason A., Westin J., Lindh M., et al. Incidence, Etiology, and Outcomes of Community-Acquired Pneumonia: A Population-Based Study. Open Forum Infect Dis 2018;5(2):ofy010. doi: 10.1093/ofid/ofy010.
17. de Roux A., Ewig S., Garcia E., et al. Mixed community-acquired pneumonia in hospitalized patients. Eur Respir J 2006; 27: 795-800.
18. Welte T., Torres A., Nathwani D. Clinical and economic burden of community-acquired pneumonia among adults in Europe. Thorax 2010. doi:10.1136/thx.2009.129502.
19. Ежлова Е.Б., Мельникова А.А., Фролова Н.В., и соавт. Эпидемиолоигческий надзор за внебольничными пневмоинями. Методические указания МУ 3.1.2/4.2. 3973-23. Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека. Москва, 2023.
20. Научный отчет НИИ антимикробной химиотерапии “Антибиотикорезис-тентность клинических штаммов Streptococcus pneumoniae, Haemophilus influenzae в России: результаты многоцентрового эпидемиологического исследования “ПЕГАС 2022-2023», Смоленск 2024 г.
21. Самохина А.С., Ерышова Д.С., Бурмистрова Е.Н., и соавт. Эпидемиология пневмококковых инфекций в многопрофильном стационаре Москвы.
Практическая пульмонология 2023; №1: 51-57.
22. Woodhead M., Blasi F., Ewig S. and the ERS/ESCMID Task Force. Guidelines for the management of adult lower respiratory tract infections. Clin Microbiol Infect 2011; 17 (Suppl. 6): 1-59.
23. Козлов Р.С. Пневмококки: уроки прошлого - взгляд в будущее. Смоленск: МАКМАХ, 2010, 127 с.
24. Rubinstein E., Kollef M., Nathwani D. Pneumonia caused by methicillin-resistant Staphylococcus aureus. Clin Infect Dis 2008;46:S378–85.
25. Faria N.A., Oliveira D.C., Westh H. Epidemiology of emerging methicillin-resistant Staphylococcus aureus (MRSA) in Denmark: a nationwide study in a country with low prevalence of MRSA infection. J Clin Microbiol 2005;43:1836–42.
26. Thomas R., Ferguson J., Coombs G., et al. Community-acquired methicillin-resistant Staphylococcus aureus pneumonia: a clinical audit. Respirology 2011;16:926–31.
27. Li H.T., Zhang T.T., Huang J., et al. Factors associated with the outcome of life-threatening necrotizing pneumonia due to community-acquired Staphylococcus aureus in adult and adolescent patients. Respiration 2011;81:448–60.
28. Gostev V., Kalinogorskaya O., Kruglov A., et al. Molecular epidemiology and antibiotic resistance of methicillin-resistant Staphylococcus aureus circulating in the Russian Federation. Infect Genet Evol. 2017;53:189-194.
29. Khokhlova O.E., Hung W.C., Wan T.W., et al. Healthcare- and Community-Associated Methicillin-Resistant Staphylococcus aureus (MRSA) and Fatal Pneumonia with Pediatric Deaths in Krasnoyarsk, Siberian Russia: Unique MRSA's Multiple Virulence Factors, Genome, and Stepwise Evolution. PLoS One 2015;10(6):e0128017.
30. Loewen K., Schreiber Y., Kirlew M., et al. Community-associated methicillin resistant Staphylococcus aureus infection: Literature review and clinical update. Can Fam Physician 2017;63(7):512-520.
31. Edelstein I., Romanov A., Edelstein M., et al. Development and application of real-time PCR assay for detection of mutations associated with macrolide resistance in Mycoplasma pneumoniae directly in clinical specimens. Proceedings of 27th European Congress of Clinical Microbiology and Infectious Diseases, Vienna, Austria. April 22-25, 2017. P#1604.
32. Sligl W.I., Marrie T.J. Severe Community-Acquired Pneumonia. Crit Care Clin 2013; 29: 563-601.
33. Чучалин А.Г., Синопальников А.И., Козлов Р.С. и др. Клинические рекомендации по диагностике, лечению и профилактике тяжелой внебольничной пневмонии у взрослых. Пульмонология 2014; 14(4):13-48.
34. Gordon C.L., Holmes N.E., Grayson M.L., et al. Comparison of immunoglobulin G subclass concentrations in severe community-acquired pneumonia and severe pandemic 2009 influenza A (H1N1) infection. Clin Vaccine Immunol 2012;19:446–8.
35. Eisen D.P., Stubbs J., Spilsbury D., et al. Low mannose-binding lectin complement activation function is associated with predisposition to Legionnaires’ disease. Clin Exp Immunol 2007;149:97–102.
36. Sole-Violan J., Garcia-Laorden M.I., Marcos-Ramos J.A., et al. The Fcgamma receptor IIA-H/H131 genotype is associated with bacteremia in pneumococcal community-acquired pneumonia. Crit Care Med 2011;39:1388–93.
37. Адаптировано из официальных данных Федеральной службы государственной статистики (РОССТАТ) от 17.05.2022 № 08-08 -6/1963-ДР.
38. Jackson M.L., Neuzil K.M., Thompson W.W., et al. The burden of community-acquired pneumonia in seniors: results of a population-based study Clin Infect Dis 2004; 39: 1642-50.
39. File T.M. Jr., Marrie T.J. Burden of community-acquired pneumonia in North American adults. Postgrad Med. 2010;122(2):130-41.
40. Ramirez J.A., Wiemken T.L., Peyrani P., et al. Adults Hospitalized With Pneumonia in the United States: Incidence, Epidemiology, and Mortality. Clin Infect Dis 2017;65(11):1806-1812.
41. Адаптировано из официальных данных Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Форма 2), 2022 г.
42. Rodriguez A., Lisboa T., Blot S., et al. Mortality ICU patients with bacterial community acquired pneumonia: when antibiotics are not enough. ICM 2009; 35: 430-438.
43. Almirall J., Mesalles E., Klamburg J., et al. Prognostic factors of pneumonia reqiring admission to the intensive care unit. Chest 1995;107:511-516.
44. Fine M.J., Smith M.A., Carson C.A., et al. Prognosis and outcome of patients with community-acquired pneumonia: a meta-analysis. JAMA 1996;275:134-141.
45. Трифанова Н.М., Лещенко И.В. Факторы риска летального исхода при тяжелой внебольничной пневмонии. Уральский медицинский журнал 2008; 13: 114-121.
46. Шаймуратов Р.И. Структурный анализ причин летальных исходов пациентов, госпитализированных с внебольничной пневмонией в стационары Татарстана. Автореф дисс. канд. Мед. наук. Санкт-Петербург, 2018.
47. Müller B., Harbarth S., Stolz D., et al. Diagnostic and prognostic accuracy of clinical and laboratory parameters in community-acquired pneumonia. BMC Infect Dis. 2007;7:10.
48. Zalacain R., Torres A., Celis R., et al. Community-acquired pneumonia in the elderly: Spanish multicentre study. Eur Respir J 2003; 21: 294–302.
49. Kaplan V., Angus D.C. Community-acquired pneumonia in the elderly. Crit Care Clin 2003;19: 729–748.
50. Tamayose M., Fujita J., Parrott G., et al. Correlations between extent of X-ray infiltration and levels of serum C-reactive protein in adult non-severe community-acquired pneumonia. J Infect Chemother 2015;21:456–463.
51. Schuetz P., Litke A., Albrich W.C., et al. Blood biomarkers for personalized treatment and patient management decisions in community-acquired pneumonia. Curr Opin Infect Dis 2013;26:159–167.
52. Bruns A.H., Oosterheert J.J., Hak E., et al. Usefulness of consecutive C-reactive protein measurements in follow-up of severe community-acquired pneumonia. Eur Respir J. 2008;32:726–732.
53. Nouvenne A., Ticinesi A., Folesani G., et al. The association of serum procalcitonin and high-sensitivity C-reactive protein with pneumonia in elderly multimorbid patients with respiratory symptoms: retrospective cohort study. BMC Geriatr. 2016;16:16.
54. Chalmers J.D., Singanayagam A., Hill A.T. C-reactive protein is an independent predictor of severity in community-acquired pneumonia. Am J Med 2008;121:219–225.
55. Nseir W., Farah R., Mograbi J., et al. Impact of serum C-reactive protein measurements in the first 2 days on the 30-day mortality in hospitalized patients with severe community-acquired pneumonia: a cohort study. J Crit Care. 2013;28:291–295.
56. de Jong E., van Oers J. A., Beishuizen A., et al. Efficacy and Safety of Procalcitonin Guidance in Reducing the Duration of Antibiotic Treatment in Critically Ill Patients: A Randomised, Controlled, Open-Label Trial. Lancet Infect Dis 2016;16(7):819-827.
57. Wiersinga W.J., BontenM.J., Boersma W.G., et al. Management of community-acquired pneumonia in adults: 2016 guideline update from the Dutch Working Party on Antibiotic Policy (SWAB) and Dutch Association of Chest Physicians (NVALT). The Netherlands Journal of Medicine 2018; 76(1): 1-13.
58. Рачина С.А., Иванчик Н.В., Козлов Р.С. Особенности микробиологической диагностики при внебольничной пневмонии у взрослых. Практическая пульмонология 2016; №4: 40-47.
59. Lim W.S., Baudouin S.V., George R.C., et al. British Thoracic Society guidelines for the management of community-acquired pneumonia in adults – update 2009. Thorax 2009; 64 (Suppl III): iii1-55.
60. Garcia L.S., Isenberg H.D. Clinical microbiology procedures handbook. Editor in chief, 3d ed. and 2007 update, L.S. Garcia. 2010; Washington, DC: ASM Press. C. 2681.
61. Рекомендации МАКМАХ «Определение чувствительности микроорганизмов к антимикробным препаратам (2024). Доступно на сайте: https://www.antibiotic.ru/minzdrav/category/clinical-recommendations/.
62. Campbell S.G., Marrie T.J., Anstey R., et al. The contribution of blood cultures to the clinical management of adult patients admitted to the hospital with community-acquired pneumonia: a prospective observational study. Chest 2003; 123: 1142-50.
63. Waterer G.W., Wunderink R.G. The influence of the severity of community-acquired pneumonia on the usefulness of blood cultures. Respir Med 2001; 95: 78-82.
64. Metersky M.L., Ma A., Bratzler D.W., et al. Predicting bacteremia in patients with community-acquired pneumonia. Am J Respir Crit Care Med 2004; 169: 342-7.
65. Writing Committee of the WHOCoCAoPI, Bautista E., Chotpitayasunondh T., et al. Clinical aspects of pandemic 2009 influenza A (H1N1) virus infection. N Engl J Med. 2010;362:1708-19.
66. Dunn J.J., Ginocchio C.C. Can newly developed, rapid immunochromatographic antigen detection tests be reliably used for the laboratory diagnosis of influenza virus infections? J Clin Microbiol 2015;53:1790-6.
67. Kashuba A.D., Ballow C.H. Legionella urinary antigen testing: potential impact on diagnosis and antibiotic therapy. Diagn Microbiol Infect Dis. 1996;24:129–139.
68. Blazquez R.M., Espinosa F.J., Martinez-Toldos C.M., et al. Sensitivity of urinary antigen test in relation to clinical severity in a large outbreak of Legionella pneumonia in Spain. Eur J Clin Microbiol Infect Dis 2005;24:488–491.
69. Чучалин А.Г., Синопальников А.И., Тартаковский И.С., и соавт. Практические рекомендации по диагностике и лечению легионеллезной инфекции, вызванной Legionella pneumophila серогруппы 1. Пособие для врачей. Москва, 2009 г.
70. Тартаковский И.С. Диагностика и профилактика легионеллеза. Лабораторная диагностика 2015; Спецвыпуск №6 «Лаборатория ЛПУ»: 40-3.
71. Harris AM, Beekmann SE, Polgreen PM., et al. Rapid urine antigen testing for Streptococcus pneumoniae in adults with community-acquired pneumonia: clinical use and barriers. Diagn Microbiol Infect Dis 2014;79:454-7.
72. Sinclair A., Xie X., Teltscher M., et al. Systematic review and meta-analysis of a urine-based pneumococcal antigen test for diagnosis of community-acquired pneumonia caused by Streptococcus pneumoniae. J Clin Microbiol. 2013; 51:2303–2310.
73. Horita N., Miyazawa N., Kojima R., et al. Sensitivity and specificity of the Streptococcus pneumoniae urinary antigen test for unconcentrated urine from adult patients with pneumonia: a meta-analysis. Respirology. 2013; 18:1177–1183.
74. Meduri G.U., Baselski V. The role of bronchoalveolar lavage in diagnosing nonopportunistic bacterial pneumonia. Chest 1991;100:179–190.
75. Pereira Gomes J.C., Pedreira W.L. Jr. Jr., Araujo E.M., et al. Impact of BAL in the management of pneumonia with treatment failure: positivity of BAL culture under antibiotic therapy. Chest. 2000;118:1739–1746.
76. Тюрин И.Е. Методы визуализации. В кн.: Респираторная медицина. 2 изд., переработанное и дополненное. Под ред. А.Г. Чучалина М.: ГЭОТАР-Медиа. 2017. Т. 1, С. 245-302.
77. Hayden G.E., Wrenn K.W. Chest radiograph vs. computed tomography scan in the evaluation for pneumonia. J Emerg Med. 2009;36:266–270.
78. Self W.H., Courtney D.M., McNaughton C.D., et al. High discordance of chest x-ray and computed tomography for detection of pulmonary opacities in ED patients: implications for diagnosing pneumonia. Am J Emerg Med. 2013; 31:401–405.
79. Bewick T., Greenwood S., Lim W.S. What is the role of pulse oximetry in the assessment of patients with community-acquired pneumonia in primary care? Prim Care Respir J. 2010;19(4):378-82.
80. Corrales-Medina V.F., Suh K.N., Rose G., et al. Cardiac complications in patients with community-acquired pneumonia: a systematic review and meta-analysis of observational studies. PLoS Med. 2011;8:e1001048.
81. Chavez M.A., Shams N., Ellington L.E., et al. Lung ultrasound for the diagnosis of pneumonia in adults: a systematic review and meta-analysis. Respir Res. 2014;15:50.
82. Ye X, Xiao H, Chen B, et al. Accuracy of lung ultrasonography versus chest radiography for the diagnosis of adult community-acquired pneumonia: review of the literature and meta-analysis. PLoS One. 2015;10:e0130066.
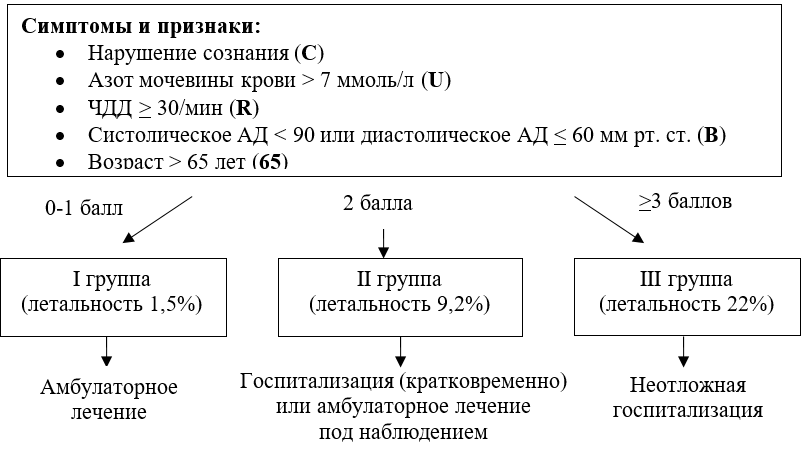
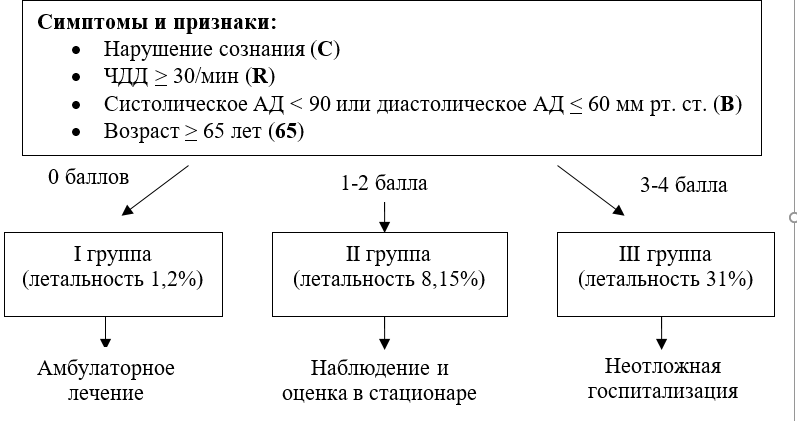
83. Lim W.S., van der Eerden M.M., Laing R., et al. Defining community acquired pneumonia severity on presentation to hospital: an international derivation and validation study. Thorax 2003; 58: 377-82.
84. Fine M.J., Auble T.E., Yealy D.M., et al. A prediction rule to identify low-risk patients with community-acquired pneumonia. N Engl J Med 1997; 336: 243-50.
85. Фесенко О.В., Синопальников А.И. Современные системы оценки внебольничной пневмонии тяжёлого течения: перспективы и ограничения. Клин микробиол антимикроб химиотер 2011; 13: 204-213.
86. Руднов В.А., Фесенко А.А., Дрозд А.В. Сравнительный анализ информационной значимости шкал для оценки тяжести состояния больных с внебольничной пневмонией, госпитализированных в ОРИТ. Клин микробиол антимикроб химиотер 2007; 9: 330-336.
87. Зайцев А.А., Овчинников Ю.В., Кондратьева Т.В. Анализ клинико-диагностических возможностей инструментов оценки тяжести и прогноза внебольничной пневмонии у пациентов молодого возраста из организованных коллективов. Пульмонология 2014; 5: 67–72.
88. Charles P.G.P., Wolfe R., Whitby M., et al. SMART-COP: a tool for predicting the need for intensive respiratory or vasopressor support in community-acquired pneumonia. Clin Infect Dis 2008; 47: 375-384.
89. Fukuyama H., Ishida T., Tachibana H., et al. Validation of scoring systems for predicting severe community-acquired pneumonia. Intern Med. 2011;50(18):1917-22.
90. Чучалин А.Г., Синопальников А.И., Козлов Р.С., и соавт. Антибактериальная терапия инфекций нижних дыхательных путей. В кн.: Практическое руководство по антиинфекционной химиотерапии // Под ред. Л.С. Страчунского, С.Н. Козлова, Ю.Б. Белоусова. Смоленск: МАКМАХ, 2007. C. 258-266.
91. Рачина С.А., Козлов Р.С., Дехнич Н.Н., и соавт. Антибактериальная терапия тяжелой внебольничной пневмонии у взрослых: обзор рекомендаций и клинические примеры. Архив внутренней медицины 2015; 23(3):63-74.
92. Справочник по антимикробной химиотерапии. Выпуск 3. Под ред. Р.С. Козлова, А.В. Дехнича. Смоленск: МАКМАХ, 2013.
93. Синопальников А.И., Фесенко О.В., Рачина С.А. Внебольничная пневмония у взрослых. В кн.: Респираторная медицина: руководство: в 4 т. / под ред. А. Г. Чучалина. – 3-е изд., доп. и перераб. – Москва: ПульмоМедиа, 2024. Т. 2, С. 508-551.
94. Carreno J.J., Lodise TP. Ceftaroline Fosamil for the Treatment of Community-Acquired Pneumonia: from FOCUS to CAPTURE. Infect Dis Ther. 2014 Dec;3(2):123-3.
95. Sligl W.I., Asadi L., Eurich D.T., et al. Macrolides and Mortality in Critically Ill Patients With Community-Acquired Pneumonia: A Systematic Review and Meta-Analysis. Crit Care Med 2014; 42: 420–432.
96. Lonks J.R., Garau J., Gomez L. et., al. Failure of macrolide antibiotic treatment in patients with bacteremia due to erythromycin-resistant Streptococcus pneumoniae. Clin Infect Dis 2002; 35: 556–564.
97. Haque N.Z., Zuniga L.C., Peyrani P., et al. Relationship of vancomycin minimum inhibitory concentration to mortality in patients with methicillin-resistant Staphylococcus aureus hospital-acquired, ventilator-associated, or health-care-associated pneumonia. Chest 2010;138(6):1356-62.
98. Dobson J., Whitley R.J., Pocock S., et al. Oseltamivir treatment for influenza in adults: a meta-analysis of rando- mised controlled trials. Lancet. 2015;385:1729–1737.
99. Louie J.K., Yang S., Acosta M., et al. Treatment with neuraminidase inhibitors for critically ill patients with influenza A (H1N1)pdm09. Clin Infect Dis. 2012;55:1198–1204.
100. Battleman D.S., Callahan M., Thaler H.T. Rapid antibiotic delivery and appropriate antibiotic selection reduce length of hospital stay of patients with community-acquired pneumonia: link between quality of care and resource utilization. Arch Intern Med. 2002;162: 682-688.
101. Houck P.M., Bratzler D.W., Nsa W., et al. Timing of antibiotic administration and outcomes for Medicare patients hospitalized with community-acquired pneumonia. Arch Intern Med. 2004; 164: 637-644.
102. Mortensen E.M., Restrepo M., Anzueto A., et al. Effects of guideline-concordant antimicrobial therapy on mortality among patients with community-acquired pneumonia. Am J Med 2004; 117: 726-31.
103. Menendez R., Ferrando D., Valles J.M., et al. Influence of deviation from guidelines on the outcome of community-acquired pneumonia. Chest 2002;122: 612-617.
104. Dean N.C., Silver M.P., Bateman K.A., et al. Decreased mortality after implementation of a treatment guideline for community-acquired pneumonia. Am J Med 2001; 110:451-457.
105. Fredlund H., Bodin L., Back E., et al. Antibiotic therapy in pneumonia: a comparative study of parenteral and oral administration of penicillin. Scand J Infect Dis. 1987;19:459-466.
106. Lode H., File T.M., Mandell L., et al. Oral gemifloxacin versus sequential therapy with intravenous ceftriaxone/oral cefuroxime with or without a macrolide in the treatment of patients hospitalized with community-acquired pneumonia: a randomized, open-label, multicenter study of clinical efficacy and tolerability. Clin Ther. 2002; 24:1915–1936.
107. Zuck P., Rio Y., Ichou F. Efficacy and tolerance of cefpodoxime proxetil compared with ceftriaxone in vulnerable patients with bronchopneumonia. J Antimicrob Chemother. 1990;26S:71–77.
108. Pakhale S., Mulpuru S., Verheij T.J., et al. Antibiotics for community-acquired pneumonia in adult outpatients. Cochrane Database Syst Rev 2014;(10):CD002109.
109. Maimon N., Nopmaneejumruslers C., Marras T.K. Antibacterial class is not obviously important in outpatient pneumonia: a meta-analysis. Eur Respir J. 2008;31(5):1068-76.
110. Boyles T.H., Brink A,, Calligaro G.L., et al. South African guideline for the management of community- acquired pneumonia in adults. J Thorac Dis 2017;9(6):1469-1502.
111. Daneman N., McGeer A., Green K., et al. Macrolide resistance in bacteremic pneumococcal disease: implications for patient management. Clin Infect Dis 2006; 43: 432–438.
112. Niederman M.S. In the Clinic: Community-Acquired Pneumonia. Ann Intern Med 2015;163:ITC1-17.
113. Dimopoulos G., Matthaiou D.K., Karageorgopoulos D.E., et al. Short- versus long-course antibacterial therapy for community-acquired pneumonia: a meta-analysis. Drugs. 2008;68(13):1841-54.
114. El Moussaoui R., de Borgie C.A., van den Broek P., et al. Effectiveness of discontinuing antibiotic treatment after three days versus eight days in mild to moderate-severe community acquired pneumonia: randomised, double blind study. BMJ. 2006;332:1355.
115. Dunbar L.M., Wunderink R.G., Habib M.P., et al. High-dose, short-course levofloxacin for community-acquired pneumonia: a new treatment paradigm. Clin Infect Dis. 2003; 37:752–760.
116. Daniel P., Rodrigo C., Mckeever T.M., et al. Time to first antibiotic and mortality in adults hospitalised with community-acquired pneumonia: a matched-propensity analysis. Thorax 2016;71(6):568-70.
117. Marras T.K., Nopmaneejumruslers C., MD, Chan C.K.N. Efficacy of Exclusively Oral Antibiotic Therapy in Patients Hospitalized with Nonsevere Community-Acquired Pneumonia:
A Retrospective Study and Meta-analysis. Am J Med. 2004;116:385–393.
118. Postma D.F., van Werkhoven C.H., van Elden L.J., et al. Antibiotic treatment strategies for community- acquired pneumonia in adults. N Engl J Med. 2015; 372:1312–1323.
119. Garin N., Genne D., Carballo S., et al. B-Lactam monotherapy vs b-lactam-macrolide combination treatment in moderately severe community-acquired pneumonia: a randomized noninferiority trial. JAMA Intern Med 2014; 174:1894–1901.
120. Grau S., Lozano V., Valladares A., et al. Antibiotic expected effectiveness and cost under real life microbiology: evaluation of ertapenem and ceftriaxone in the treatment of community-acquired pneumonia for elderly patients in Spain. Clinicoecon Outcomes Res 2014;6:83-92.
121. Torres A., Garau J., Arvis P., et al. Moxifloxacin monotherapy is effective in hospitalized patients with community-acquired pneumonia: the MOTIV study--a randomized clinical trial. Clin Infect Dis 2008;46(10):1499-509.
122. Leroy O., Saux P., Bédos J.P., et al. Comparison of levofloxacin and cefotaxime combined with ofloxacin for ICU patients with community-acquired pneumonia who do not require vasopressors. Chest 2005;128(1):172-83.
123. Rhew D.C., Tu G.S., Ofman J., et al. Early switch and early discharge strategies in patients with community-acquired pneumonia: a meta-analysis. Arch Intern Med 2001; 161: 722-727.
124. Halm E.A., Fine M.J., Marrie T.J., et al. Time to clinical stability in patients hospitalized with community-acquired pneumonia: implications for practice guidelines. JAMA 1998; 279: 1452-1457.
125. Ramirez J.A., Bordon J. Early switch from intravenous to oral antibiotics in hospitalized patients with bacteremic community-acquired Streptococcus pneumoniae pneumonia. Arch Intern Med 2001; 161: 848-850.
126. Tejerina E., Frutos V., Restrepo M.I., et al. Prognosis factors and outcome of community-acquired pneumonia needing mechanical ventilation. J Crit Care 2005; 20: 56–65.
127. Mortensen E.M., Coley C.M., Singer D.E., et al. Causes of death for patients with community-acquired pneumonia: results from the Pneumonia Patient Outcomes Research Team cohort study. Arch Intern Med 2002;162:1059–64.
128. Pascual F.E., Matthay M.A., Bacchetti P., et al. Assessment of prognosis in patients with community-acquired pneumonia who require mechanical ventilation. Chest 2000; 117(2): 503–12.
129. Barcroft J., Camis M. The dissociation curve of blood. J Physiol. Wiley-Blackwell; 1909; №39(2): 118–142.
130. Protti A., Andreis D.T., Iapichino G.E., et al. Ventilation with Lower Tidal Volumes as Compared with Traditional Tidal Volumes for Acute Lung Injury and the Acute Respiratory Distress Syndrome. N Engl J Med 2000; 42 (18):1301–1308.
131. Barrot L, Asfar P, Mauny F, et al. Liberal or Conservative Oxygen Therapy for Acute Respiratory Distress Syndrome. N Engl J Med 2020;382(11):999-1008.
132. Авдеев С.Н. Ургентная кислородотерапия. Вестник анестезиологии и реаниматологии 2011; №3: 42-51.
133. Ярошецкий А.И., Власенко А.В., Грицан А.И., и соавт. Применение неинвазивной вентиляции легких (второй пересмотр). Анестезиология и реаниматология 2019;6:5-19.
134. Mauri T, Turrini C, Eronia N, et al. Physiologic effects of high-flow nasal cannula in acute hypoxemic respiratory failure. Am J Respir Crit Care Med 2017;195:1207–1215.
135. Frat JP, Thille A.W, Mercat A, et al. High-flow oxygen through nasal cannula in ARF. N Engl J Med 2015; 372: 2185-2196.
136. Tobin MJ. Basing Respiratory Management of Coronavirus on Physiological Principles. Am J Respir Crit Care Med 2020; 201(11):1319-1320.
137. Jiang S, Liu T, Hu Y, et al. Efficacy and safety of glucocorticoids in the treatment of severe community-acquired pneumonia: A meta-analysis. Medicine (Baltimore). 2019;98(26):e16239.
138. Annane D., Bellissant E., Bollaert P-E., et al. Corticosteroids in treatment severe sepsis and septic shock in adults. A systematic review. JAMA 2009; 301(22): 2362-2375.
139. Annane D., Sebille V., Bellisant E., et al. Effect of low doses of corticosteroids in septic schock patients with or without early acute respiratory distress syndrome. Crit Care Med 2006; 34: 22-30.
140. Annane D., Sebille V., Charpentier C., et al. Effect of treatment with low doses of hydrocortisone and fludrocortisone on mortality in patients with septic shock. JAMA 2002;288:862-871.
141. Wan YD, Sun TW, Liu ZQ, et al. Efficacy and Safety of Corticosteroids for Community-Acquired Pneumonia: A Systematic Review and Meta-Analysis. Chest 2016;149:209-19.
142. Feldman C., Anderson R. Corticosteroids in the adjunctive therapy of community-acquired pneumonia: an appraisal of recent meta-analyses of clinical trials. J Thorac Dis 2016;8:E162-71.
143. Cronin L., Cook D., Carlet J., et al. Corticosteroid treatment for sepsis: a critical appraisal and meta-analysis of the literature. Crit Care Med 1995; 23:1430-1439.
144. Torres A., Sibila O., Ferrer M., et al. Effect of corticosteroids on treatment failure among hospitalized patients with severe community-acquired pneumonia and high in ammatory response: a randomized clinical trial. JAMA 2015;313:677-86.
145. Chen L.P., Chen J.H., Chen Y., et al. Efficacy and safety of glucocorticoids in the treatment of community-acquired pneumonia: A meta-analysis of randomized controlled trials. World J Emerg Med 2015;6:172-8.
146. Siemieniuk R.A., Meade M.O., Alonso-Coello P., et al. Corticosteroid Therapy for Patients Hospitalized With Community-Acquired Pneumonia: A Systematic Review and Meta-analysis. Ann Intern Med 2015;163:519-28. Wan YD, Sun TW, Liu ZQ, et al. Efficacy and Safety of Corticosteroids for Community-Acquired Pneumonia: A Systematic Review and Meta-Analysis. Chest 2016;149:209-19.
147. Alejandria M.,Lansang MA., Dans L.,et al. Intravenous immunoglobulin for treting sepsis and septic shock. Cochrane Database Syst Rev 2002 (1):CD001090.
148. Haque K.N., Remo C., Bahakim H. Comparison of two types of intravenous immunoglobulins in the treatment of neonatal sepsis. Clin Exp Immunol 1995; 101: 328–33.
149. Kreymann K.G., de Heer G., Nierhaus A., at al. Use polyclonal immunoglobulin as adjunctive therapy for severe sepsis and septic shock. Crit Care Med 2007; 35: 2677-2685.
150. Turgeon F., Hutton B., Fergusson D.A., et al. Meta-analysis: Intravenous immunoglobulin in crically ill audult patients with sepsis. Ann Int Med 2007; 146: 193 - 203.
151. Laupland K., Rirpatrick A., Delaney A. Polyclonal immunoglobulin for treatment severe sepsis and septic shock in crically ill audults. A systematic review and meta-analysis. Crit Care Med 2007; 35: 2686-2692.
152.Ceccato A, Ferrer M, Barbeta E., et al. Adjunctive Therapies for Community-Acquired Pneumonia Clin Chest Med 2018; 39(4): 753-764.
153. Bo L., Wang F., Zhu J., et al. Granulocyte-colony stimulating factor(G-CSF) and Granulocyte-macrophage colony stimulating factor (GM-CSF) for sepsis: meta-analysis. Crit Care 2011; 15: R58.
154. Cheng A.C., Stephens D.P., Currie B.J. Granulocyte-Colony Stimulating Factor (G-CSF) as an adjunct to antibiotics in the treatment of pneumonia in adults. Cochrane Database Syst Rev 2007, (2): CD004400.
155. Meisel C., Schefold J.C., Pschowski R., et al. Granulocyte-macrophage colony-stimulating factor to reverse sepsis-associated immunosuppression: a double-blind, randomized, placebo-controlled multicenter trial. Am J Respir Crit Care Med 2009; 180:640-648.
156. Mismetti P., Laporte-Simitsidis S., Tardy B., et al. Prevention of venous thromboembolism in internal medicine with unfractionated or low-molecular-weight heparins: a meta-analysis of randomised clinical trials. Thromb Haemost 2000;83:14–9.
157. Diao WQ, Shen N, Yu PX, et al. Efficacy of 23-valent pneumococcal polysaccharide vaccine in preventing community-acquired pneumonia among immunocompetent adults: A systematic review and meta-analysis of randomized trials. Vaccine 2016; 34(13):1496-1503.
158. McLaughlin J, Jiang Q, Isturiz RE, et al. Effectiveness of 13-Valent Pneumococcal Conjugate Vaccine Against Hospitalization for Community-Acquired Pneumonia in Older US Adults: A Test-Negative Design. Clinical Infectious Diseases 2018; 67(10): 1498-1506.
159. Bonten ,MJM, Huijts SM,, Bolkenbaas M., et al. Polysaccharide Conjugate Vaccine against Pneumococcal Pneumonia in Adults. The New England Journal of Medicine 2015; 372:1114-25.
160. Frenck RW Jr, Gurtman A, Rubino J, et al. Randomized, controlled trial of a 13-valent pneumococcal conjugate vaccine administered concomitantly with an influenza vaccine in healthy adults. Clin Vaccine Immunol 2012;19(8):1296-303.
161. Schwarz TF, Flamaing J, Rumke HC, et al. A randomized, double-blind trial to evaluate immunogenicity and safety of 13-valent pneumococcal conjugate vaccine given concomitantly with trivalent influenza vaccine in adults aged ≥65 years. Vaccine 2011;29(32):5195-202.
162. Ofori-Anyinam O., Leroux-Roels G, Drame M, et al. Immunogenicity and safety of an inactivated quadrivalent influenza vaccine co-administered with a 23-valent pneumococcal polysaccharide vaccine versus separate administration, in adults ≥50years of age: Results from a phase III, randomized, non-inferiority trial. Vaccine 2017;35(46):6321-6328.
163. Matanock A., Lee G., Gierke R., et al. Use of 13-Valent Pneumococcal Conjugate Vaccine and 23-Valent Pneumococcal Polysaccharide Vaccine Among Adults Aged ≥65 Years: Updated Recommendations of the Advisory Committee on Immunization Practices. MMWR Morb Mortal Wkly Rep 2019;68(46):1069-1075.
164. Авдеев С.Н., Алыева М.Х., Баранов А.А. и др. Вакцинопрофилактика пневмококковой инфекции у детей и взрослых. Методические рекомендации. Профилактическая медицина 2023; 26 (№9) (Приложение): 3-23.
165. Иммунизация взрослых. Методические рекомендации Драпкина О.М., Брико Н.И., Костинов М.П., и др. М., ФГБУ «НМИЦ ТПМ» Минздрава России: 2020, 248 с.
166. Приказ Минздрава Российской Федерации “Об утверждении национального календаря профилактических прививок, календаря профилактических прививок по эпидемическим показаниям и порядка проведения профилактических прививок" №1122-Н от 6 декабря 2021 г.
167. Falkenhorst G, Remschmidt C., Harder T., et al. Effectiveness of the 23-Valent Pneumococcal Polysaccharide Vaccine (PPV23) against Pneumococcal Disease in the Elderly: Systematic Review and Meta-Analysis. PLoS One 2017; 12(1):e0169368.
168. Намазова-Баранова Л.С., Федосеенко М.В., Селимзянова Л.Р., и соавт. Современные подходы к иммунопрофилактике инфекционных болезней в период беременности. Педиатрическая фармакология 2022;19(5):417–423.
169. Постановление Главного государственного санитарного врача Российской Федерации от 26 июля 2023 г. N 74470 г. Москва "О мероприятиях по профилактике гриппа и острых респираторных вирусных инфекций в эпидемическом сезоне 2023-2024 годов».
170. Cangemi R., Calvieri C., Falcone M., et al. Relation of Cardiac Complications in the Early Phase of Community-Acquired Pneumonia to Long-Term Mortality and Cardiovascular Events. Am J Cardiol 2015;116(4):647-51.
171. Kuhajda I., Zarogoulidis K., Tsirgogianni K., et al. Lung abscess-etiology, diagnostic and treatment options. Ann Transl Med 2015; 3(13):183.
172. Rome L., Murali G., Lippmann M. Nonresolving pneumonia and mimics of pneumonia. Med Clin North Am 2001; 85:1511–1530, xi.
173. de Jager C.P., Wever P.C., Gemen E.F., et al. The neutrophil-lymphocyte count ratio in patients with community-acquired pneumonia. PLoS One 2012;7(10):e46561.
174. Hedlund J., Hansson L.O. Procalcitonin and C-reactive protein levels in community-acquired pneumonia: correlation with etiology and prognosis. Infection 2000;28:68-73.
175. Johansson N., Kalin M., Backman-Johansson C., et al. Procalcitonin levels in community-acquired pneumonia - correlation with aetiology and severity. Scand J Infect Dis 2014;46:787-791.
176. Menendez R., Martinez R., Reyes S., et al. Biomarkers improve mortality prediction by prognostic scales in community-acquired pneumonia. Thorax 2009; 64: 587-591.
177. Evans L., Rhodes A., Alhazzani W., et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med 2021;47(11):1181-1247.
178. Howell M.D., Donnino M., Clardy P., et al. Occult hypoperfusion and mortality in patients with suspected infection. Intensive Care Med 2007;33:1892-1899.
179. Zhou H., Lan T., Guo S. Prognostic Prediction Value of qSOFA, SOFA, and Admission Lactate in Septic Patients with Community-Acquired Pneumonia in Emergency Department. Emerg Med Int 2020; 2020: 7979353.
180. Рачина С.А., Сухорукова М.В.. Микробиологическая диагностика инфекций нижних дыхательных путей. В кн.: Основы внутренней медицины. Под ред. В.С. Моисеева, Ж.Д. Кобалава, И.В. Маева и соавт. М.: МИА, 2020, 2-е изд. Т.1. С.97-106.
181. Walden A.P., Clarke G.M., McKechnie S., et al; ESICM/ECCRN GenOSept Investigators. Patients with community acquired pneumonia admitted to European intensive care units: an epidemiological survey of the GenOSept cohort. Crit Care 2014;18(2):R58. doi: 10.1186/cc13812.
182. Chow E.J., Doyle J.D., Uyeki T.M. Influenza Virus-Related Critical Illness: Prevention, Diagnosis, Treatment. Crit Care 2019;23(1):214. doi: 10.1186/s13054-019-2491-9.
183. Costantini E., Allara E., Patrucco F., et al. Adherence to Guidelines for Hospitalized Community-Acquired Pneumonia Over Time and Its Impact on Health Outcomes and Mortality. Intern Emerg Med 2016;11(7):929-40.
184. Piso R.J., Iven-Koller D., Koller M.T., et al. The Routine Use of Urinary Pneumococcal Antigen Test in Hospitalised Patients With Community Acquired Pneumonia Has Limited Impact for Adjustment of Antibiotic Treatment. Swiss Med Wkly 2012;142:w13679. doi: 10.4414/smw.2012.13679.
185. Claessens Y.E., Debray M.P., Tubach F., et al. Early Chest Computed Tomography Scan to Assist Diagnosis and Guide Treatment Decision for Suspected Community-acquired Pneumonia. Am J Respir Crit Care Med 2015;192(8):974-82.
186. Franquet T. Imaging of pneumonia: trends and algorithms. Eur Respir J 2001;18:196–208.
187. Фесенко О.В., Синопальников А.И. Заболевания плевры. В кн.: Основы внутренней медицины. В 2 т. Т. 1. 2 изд., перераб. и доп. Ред. Ж.Д. Кобалава, И.В. Маев, А.Д. Каприн и др. М.: ООО “МИА”. 2020. Т. 2, С. 265-272.
188. Lichtenstein D.A. BLUE-Protocol and FALLS-Protocol: Two applications of lung ultrasound in the critically ill. Chest 2015; 147(6): 1659-1670.
189. Llamas-Álvarez A.M., Tenza-Lozano E.M., Latour-Pérez J., et al. Accuracy of Lung Ultrasono-graphy in the Diagnosis of Pneumonia in Adults: Systematic Review and Meta-Analysis. Chest 2017; 151(2): 374-382.
190. Salih W., Schembri S., Chalmers J.D. Simplification of the IDSA/ATS criteria for severe CAP using meta-analysis and observational data. Eur Respir J 2014;43:842–851.
191. Calderon M., Gysin G., Gujjar A., et al. Bacterial co-infection and antibiotic stewardship in patients with COVID-19: a systematic review and meta-analysis. BMC Infect Dis 2023;23(1):14. doi: 10.1186/s12879-022-07942-x.
192. Metlay J.P., Watere G.W., Long A.C., et al. Diagnosis and Treatment of Adults With Community-acquired Pneumonia. An Official Clinical Practice Guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med 2019;200(7):e45-e67.
193. Козлов Р.С., Рачина С.А., Захаренко С.М. Общие принципы антимкробной химиотерапии инфекционных больных. В кн.: Руководство по инфекционным болезням. В 2 кн. Под ред. Ю. В. Лобзина, К. В. Жданова. 4-е изд., доп. и перераб. Санкт-Петербург: ООО «Издательство Фолиант», 2011. С. 58-106.
194. Liu V.X., Fielding-Singh V., Greene J.D., et al. The Timing of Early Antibiotics and Hospital Mortality in Sepsis. Am J Respir Crit Care Med 2017; 196(7): 856–863.
195. Rodríguez A., Mendia A., Sirvent J.M., et al. CAPUCI Study Group. Combination antibiotic therapy improves survival in patients with community-acquired pneumonia and shock. Crit Care Med 2007;35:1493–1498.
196. Waterer G.W., Somes G.W., Wunderink R.G. Monotherapy may be suboptimal for severe bacteremic pneumococcal pneumonia. Arch Intern Med 2001;161:1837–1842.
197. Martínez J.A., Horcajada J.P., Almela M., et al. Addition of a macrolide to a beta-lactam-based empirical antibiotic regimen is associated with lower in-hospital mortality for patients with bacteremic pneumococcal pneumonia. Clin Infect Dis 2003;36:389–395.
198. Baddour L.M., Yu V.L., Klugman K.P., et al. Combination antibiotic therapy lowers mortality among severely ill patients with Pneumococcal bacteraemia. Am J Respir Crit Care Med 2004;170:440–444.
199. Gattarello S., Borgatta B., Solé-Violán J., et al. Decrease in mortality in severe community-acquired pneumococcal pneumonia: impact of improving antibiotic strategies (2000–2013). Chest 2014;146:22–31.
200. De la Calle C., Hg T-DLV., Morata L., et al. Effectiveness of combination therapy versus monotherapy with a third-generation cephalosporin in bacteraemic pneumococcal pneumonia: a propensity score analysis. J Infection 2018;76:342–347.
201. Gattarello S., Lagunes L., Vidaur L., et al. Improvement of antibiotic therapy and ICU survival in severe non-pneumococcal community-acquired pneumonia: a matched case-control study. Crit Care 2015;10(19):335.
202. Garnacho-Montero J., Barrero-García I., Gómez-Prieto M.G., et al. Severe community-acquired pneumonia: current management and future therapeutic alternatives. Expert Rev Anti Infect Ther 2018;16(9):667-677.
203. Martin-Loeches I., Lisboa T., Rodriguez A., et al. Combination antibiotic therapy with macrolides improves survival in intubated patients with community-acquired pneumonia. Intensive Care Med 2010;36(4):612-20.
204. Restrepo M.I., Mortensen E.M., Waterer G.W., et al. Impact of macrolide therapy on mortality for patients with severe sepsis due to pneumonia. Eur Respir J 2009;33(1):153-9.
205. Lee J.H., Kim H.J., Kim Y.H. Is β-Lactam Plus Macrolide More Effective than β-Lactam Plus Fluoroquinolone among Patients with Severe Community-Acquired Pneumonia?: a Systemic Review and Meta-Analysis. J Korean Med Sci 2017; 32(1): 77–84.
206. Shorr A.F., Kollef M., Eckburg P.B., et al. Assessment of Ceftaroline Fosamil in the Treatment of Community-Acquired Bacterial Pneumonia Due to Streptococcus Pneumoniae: Insights From Two Randomized Trials. Diagn Microbiol Infect Dis 2013;75(3):298-303.
207. Restrepo M.I., Babu B.L., Reyes L.F., et al. Burden and risk factors for Pseudomonas aeruginosa community-acquired pneumonia: a multinational point prevalence study of hospitalised patients. Eur Respir J 2018 9;52(2). pii: 1701190.
208. Shindo Y, Sato S, Maruyama E, et al. Health-care-associated pneumonia among hospitalized patients in a Japanese community hospital. Chest 2009; 135: 633–40.
209. Prina E, Ranzani OT, Polverino E, et al. Risk factors associated with potentially antibiotic- resistant pathogens in community-acquired pneumonia. Ann Am Thorac Soc 2015; 12: 153–60.
210. González-Castillo J., Martín-Sánchez F.J., Llinares P., et al. Guidelines for the management of community-acquired pneumonia in the elderly patient. Rev Esp Quimioter 2014;27(1):69-86.
211. von Baum H., Welte T., Marre R., et al. Community-acquired pneumonia through Enterobacteriaceae and Pseudomonas aeruginosa: Diagnosis, incidence and predictors. Eur Respir J 2010; 35:598-605.
212. Calbo E., Romaní V., Xercavins M., et al. Risk factors for community-onset urinary tract infec- tions due to Escherichia coli harbouring extended-spectrum be- ta-lactamases. J Antimicrob Chemother 2006; 57:780-3.
213. Rodríguez-Baño J., Navarro M.D., Romero L., et al. Epidemiology and clinical fea- tures of infections caused by extended-spectrum beta-lactama- se-producing Escherichia coli in non hospitalized patients. J Clin Microbiol 2004; 42:1089-94.
214. Marik P.E. Aspiration pneumonitis and aspiration pneumonia. N Engl J Med 2001;344:665–671.
215. Marrie T.J., Durant H., Kwan C. Nursing home-acquired pneumonia: a case-control study. J Am Geriatr Soc 1986;34:697–702.
216. Cesar L., Gonzalez C., Calia F.M. Bacteriologic flora of aspiration- induced pulmonary infections. Arch Intern Med 1975;135: 711–714.
217. El-Solh A.A., Pietrantoni C., Bhat A, et al. Microbiology of severe aspiration pneumonia in institutionalized elderly. Am J Respir Crit Care Med 2003;167:1650–1654.
218. Marik P.E., Careau P. The role of anaerobes in patients with ventilator-associated pneumonia and aspiration pneumonia: a prospective study. Chest 1999;115:178–183.
219. Mier L., Dreyfuss D., Darchy B., et al. Is penicillin G an adequate initial treatment for aspiration pneumonia? A prospective evaluation using a protected specimen brush and quantitative cultures. Intensive Care Med 1993;19:279–284.
220. Lee N., Choi K.W., Chan P.K., et al. Outcomes of adults hospitalised with severe influenza. Thorax 2010;65:510–515.
221. McGeer A., Green K.A., Plevneshi A., et al.Antiviral therapy and outcomes of influenza requiring hospitalization in Ontario, Canada. Clin Infect Dis 2007;45:1568–1575.
222. Morel J., Casoetto J., Jospe ́ R., et al. De-escalation as part of a global strategy of empiric antibiotherapy management: a retrospective study in a medico-surgical intensive care unit. Crit Care 2010;14:R225.
223. Leone M., Bechis C., Baumstarck K., et al.; AZUREA Network Investigators. De-escalation versus continuation of empirical antimicrobial treatment in severe sepsis: a multicenter non-blinded randomized noninferiority trial. Intensive Care Med 2014;40:1399–1408.
224. Gutierrez-Pizarraya A., Leone M., Garnacho-Montero J., et al. Collaborative approach of individual participant data of prospective studies of de-escalation in non-immunosuppressed critically ill patients with sepsis. Expert Rev Clin Pharmacol 2017;10: 457–465.
225. Tansarli G.S., Mylonakis E. Systematic review and meta-analysis of the efficacy of short-course antibiotic treatments for community- acquired pneumonia in adults. Antimicrob Agents Chemother 2018; 62:e00635-18.
226. Grieco DL, Menga LS, Raggi V, et al. Physiological Comparison of High-Flow Nasal Cannula and Helmet Noninvasive Ventilation in Acute Hypoxemic Respiratory Failure. Am J Respir Crit Care Med 2020;201(3):303-312.
227. Ferreyro BL, Angriman F, Munshi L, et al. Association of Noninvasive Oxygenation Strategies With All-Cause Mortality in Adults With Acute Hypoxemic Respiratory Failure: A Systematic Review and Meta-analysis. JAMA 2020;324(1):57-67.
228. Carteaux G, Millán-Guilarte T, De Prost N, et al. Failure of Noninvasive Ventilation for De Novo Acute Hypoxemic Respiratory Failure: Role of Tidal Volume. Crit Care Med 2016;44(2):282-90.
229. Frat JP, Ragot S, Coudroy R, et al. Predictors of Intubation in Patients With Acute Hypoxemic Respiratory Failure Treated With a Noninvasive Oxygenation Strategy. Crit Care Med 2018;46(2):208-215.
230. Hraiech S, Alingrin J, Dizier S,, et al. Time to intubation is associated with outcome in patients with community-acquired pneumonia. PLoS One 2013;8:e74937.
231. Kangelaris K.N., Ware L.B., Wang C.Y., et al. Timing of intubation and clinical outcomes in adults with acute respiratory distress syndrome. Crit Care Med 2016; 44(1):120–129.
232. Kang BJ, Koh Y, Lim CM, et al. Failure of high-flow nasal cannula therapy may delay intubation and increase mortality. Intensive Care Med 2015;41:623–632.
233. Brochard L, Lefebvre JC, Cordioli RL, et al. Noninvasive ventilation for patients with hypoxemic acute respiratory failure. Semin Respir Crit Care Med 2014;35(4):492-500.
234. Pieralli F, Vannucchi V, Nozzoli C, et al. Acute cardiovascular events in patients with community acquired pneumonia: results from the observational prospective FADOI-ICECAP study. BMC Infect Dis 2021;21(1):116.
235. Confalonieri M, Potena A, Carbone G, et al. Acute respiratory failure in patients with severe community-acquired pneumonia. A prospective randomized evaluation of noninvasive ventilation. Am J Respir Crit Care Med 1999; 160:1585–1591.
236. Jolliet P, Abajo B, Pasquina P, et al. Non-invasive pressure support ventilation in severe community-acquired pneumonia. Intensive Care Med 2001; 27: 812–821.
237. Domenighetti G, Gayer R, Gentilini R. Noninvasive pressure support ventilation in non-COPD patients with acute cardiogenic pulmonary edema and severe community-acquired pneumonia: acute effects and outcome. Intensive Care Med 2001; 28:1226–1232;
238. Ferrer M, Esquinas A, Leon M, et al. Noninvasive ventilation in severe hypoxemic respiratory failure: a randomized clinical trial. Am J Respir Crit Care Med 2001; 168:1438–1444.
239. Kohno S, Seki M, Takehara K, et al. Prediction of requirement for mechanical ventilation in community-acquired pneumonia with acute respiratory failure: a multicenter prospective study. Respiration 2013;85(1):27-35.
240. Brochard L, Slutsky A, Pesenti A. Mechanical ventilation to minimize progression of lung injury in acute respiratory failure. Am J Respir Crit Care Med 2017;195(4):438–42.
241. Tonelli R, Fantini R, Tabbì L, et al. Inspiratory effort assessment by esophageal manometry early predicts noninvasive ventilation outcome in de novo respiratory failure: a pilot study. Am J Respir Crit Care Med 2020; 202 (4):558-567.
242. Demoule A, Jung B, Prodanovic H, et al. Diaphragm dysfunction on admission to the intensive care unit. Prevalence, risk factors, and prognostic impact-a prospective study. Am J Respir Crit Care Med 2013;188(2):213-219.
243. Behazin N, Jones SB, Cohen RI, et al. Respiratory restriction and elevated pleural and esophageal pressures in morbid obesity. J Appl Physiol 2010; 108: 212-218.
244. Guerin C, Reignier J, Richard JC, et al. Prone positioning in severe acute respiratory distress syndrome. N Engl J Med 2013; 368(23): 2159–2168.
245. Munshi L, Del Sorbo L, Adhikari NKJ, et al. Prone Position for Acute Respiratory Distress Syndrome. A Systematic Review and Meta-Analysis. Ann Am Thorac Soc 2017;14(Supplement_4):S280-S288.
246. Dreyfuss D, Djedaini K, Lanore JJ, et al. A comparative study of the effects of almitrine bismesylate and lateral position during unilateral bacterial pneumonia with severe hypoxemia. Am Rev Respir Dis 1992;146(2):295-9.
247. Rouby JJ, Lu Q., Goldstein I. Selecting the right level of positive end-expiratory pressure in patients with acute respiratory distress syndrome. Am J Respir Crit Care Med 2002; 165: 1182–1186.
248. Albaiceta G., Taboada F, Parra D, et al. Differences in the deflation limb of the pressure-volume curves in acute respiratory distress syndrome from pulmonary and extrapulmonary origin. Intensive Care Med 2003; 29: 1943–1949.
249. Ярошецкий А.И., Проценко Д.Н., Бойцов П.В. и соавт. Оптимальное положительное конечно-экспираторное давление при ОРДС у больных с гриппом А(H1N1)pdm09: баланс между максимумом конечно-экспираторного объема и минимумом перераздувания альвеол. Анестезиология и реаниматология 2016; 61(6): 425-432.
250. Amato MBP, Meade MO, Slutsky AS, et al. Driving pressure and survival in the acute respiratory distress syndrome. N Engl J Med 2015; 372: 747–755.
251. ARDS Network. Ventilation with Lower Tidal Volumes as Compared with Traditional Tidal Volumes for Acute Lung Injury and the Acute Respiratory Distress Syndrome. New Engl J Med 2000; 342(18):1301–1308.
252. Dessap AM, Viellard-Baron A, Charron C, et al. Acute cor pulmonale during protective ventilation: prevalence, predictors and clinical impact. Intensive Care Med 2016; 42(5):862-870.
253. Combes A, Hajage D, Capellier G, et al Extracorporeal Membrane Oxygenation for Severe Acute Respiratory Distress Syndrome. N Engl J Med 2018; 378:1965-1975.
254. Patroniti N, Bonatti G, Senussi T, et al. Mechanical ventilation and respiratory monitoring during extracorporeal membrane oxygenation for respiratory support. Ann Transl Med 2018; 6 (19): 386.
255. Yaroshetskiy AI, Avdeev SN, Konanykhin VD. Acute Respiratory Distress Syndrome in COVID-19: Do All These Patients Definitely Require Intubation and Mechanical Ventilation? Am J Respir Crit Care Med 2020; doi: 10.1164/rccm.202007-2713LE.
256. Metlay J P, Atlas S J, Borowsky L H, et al. Time course of symptom resolution in patients with community-acquired pneumonia. Respir Med 1998;92(9):1137-42.
257. Moussaoui R E, Opmeer BC, de Borgie C A J M , et al. Long-term symptom recovery and health-related quality of life in patients with mild-to-moderate-severe community-acquired pneumonia. Chest 2006;130(4):1165-72.
258. Wyrwich KW, Yu H, Sato R, et al. Observational longitudinal study of symptom burden and time for recovery from community-acquired pneumonia reported by older adults surveyed nationwide using the CAP Burden of Illness Questionnaire. Patient Relat Outcome Meas 2015;6:215-23.
259. Ebell MH, Bentivegna M, Cai X, et al. Accuracy of Biomarkers for the Diagnosis of Adult Community‐acquired Pneumonia: A Meta‐analysis. Academic Emergency Medicine 2020; 27 (3): 195-206.
260. Liu D, Su L_X, Guan W, et al. Prognostic value of procalcitonin in pneumonia: A systematic review and meta‐analysis. Respirology 2016; 21(2): 280-288.
261. Hökenek NM, Seyhan AU, Erdogan MO, et al. Evaluation of Blood Gas Analysis as a Mortality Predictor. South Clin Ist Euras 2019; 30 (3): 228-231.
262. O’Horo J. C., Thompson D., Safdar N. Is the Gram Stain Useful in the Microbiologic Diagnosis of VAP? A Meta-analysis. Clinical Infectious Diseases 2012; 55(4): 551–561.
263. Ebell, M. H., Chupp, H., Cai, X., et al. Accuracy of Signs and Symptoms for the Diagnosis of Community‐acquired Pneumonia: A Meta‐analysis. Academic Emergency Medicine 2020; 27 (7): 541-553.
264. Paul M., Dickstein Y., Raz-Pasteur A. Antibiotic de-escalation for bloodstream infections and pneumonia: systematic review and meta-analysis. Clinical Microbiology and Infection 2016; 22(12): 960-967.
265. Horita N., Otsuka T, Haranaga S, et al. Beta‐lactam plus macrolides or beta‐lactam alone for community‐acquired pneumonia: A systematic review and meta‐analysis. Respirology 2016; 21: 1193-1200.
266. Lee J. H., Kim H. J., Kim Y. H. Is β-Lactam Plus Macrolide More Effective than β-Lactam Plus Fluoroquinolone among Patients with Severe Community-Acquired Pneumonia?: a Systemic Review and Meta-Analysis. Journal of Korean medical science 2017; 32 (1): 77-84.
267. Paul M., Dickstein Y., Raz-Pasteur A. Antibiotic de-escalation for bloodstream infections and pneumonia: systematic review and meta-analysis. Clinical Microbiology and Infection 2016; 2 (12): 960-967.
268. Heneghan C, Onakpoya I, Jones MA, et al. Neuraminidase inhibitors for influenza: a systematic review and meta-analysis of regulatory and mortality data. Health Technology Assessment 2016; 20 (42): 1-242.
269. Mendes PV, Melro LMG, Li H Y, et al. Extracorporeal membrane oxygenation for severe acute respiratory distress syndrome in adult patients: a systematic review and meta-analysis. Revista Brasileira de terapia intensive 2019; 31(№4): 548-554.
270. Restivo V, Costantino C, Bono S, et al. Influenza vaccine effectiveness among high-risk groups: a systematic literature review and meta-analysis of case-control and cohort studies . Human vaccines & immunotherapeutics 2018;14 (3): 724-735.
271. Fang F., Zhang Yu., Tang J., et al. Association of Corticosteroid Treatment With Outcomes in Adult Patients With Sepsis. A Systematic Review and Meta-analysis. JAMA Intern Med 2019; 179(2): 213–223.
272. Cristinacce A., Wright J.G., Stone G.G., et al. A Retrospective Analysis of Probability of Target Attainment in Community-Acquired Pneumonia: Ceftaroline Fosamil Versus Comparators. Infect Dis Ther 2019;8(2):185-198.
273. Ollivier J., Carrie C., d’Houdain N., et al. Are Standard Dosing Regimens of Ceftriaxone Adapted for Critically Ill Patients with Augmented Creatinine Clearance? Antimicrob Agents Chemother 2019;63(3):e02134-18.
274. Valera A.I.A., Perez A.A., Ortega A.N., et al. Macrolide-resistant Mycoplasma pneumoniae: Do we know the situation in Europe? Rev Esp Quimioter 2023; 36(3): 259-266.
275. May M., Chang M, Dietz D., et al. Limited Utility of Procalcitonin in Identifying Community-Associated Bacterial Infections in Patients Presenting with Coronavirus Disease 2019. Antimicrob Agents Chemother 2021;65(4):e02167-20.
276. Martin-Loeches I., Torres A., Nagavci B., et al. ERS/ESICM/ESCMID/ ALAT guidelines for the management of severe community-acquired pneumonia. Eur Respir J. 2023; 61(4): 2200735.
277. Авдеев С.Н., Белобородов В.Б., Белоцерковский Б.З., и соавт. Тяжелая внебольничная пневмония у взрослых. Клинические рекомендации Федерации анестезиологов и реаниматологов России. Анестезиология и реаниматология
2022; 1: 6–35.
278. Restrepo M.I., Babu B.L., Reyes L.F., et al. Burden and risk factors for Pseudomonas aeruginosa community-acquired pneumonia: a multinational point prevalence study of hospitalised patients. Eur Respir J. 2018;9:52(2).
279. Torres A., Chalmers J.D., Dela Cruz C.S., et al. Challenges in severe com- munity-acquired pneumonia: a point-of-view review. Intensive Care Med. 2019;45:159-171.
280. Webb B.J., Dascomb K., Stenehjem E., et al. Predicting risk of drug-resistant organisms in pneumonia: moving beyond the HCAP model. Respir Med. 2015;109:1-10.
281. Козлов Р.С., Дехнич А.В. Цефдиторен пивоксил: клинико-фармакологическая и микробиологическая характеристика. Клин микробиол антимикроб химиотер 2014; 16(2):111-129.
282. Minov J., Stoleski S., Petrova T., et al. Cefpodoxime in the outpatient treatment of lower respiratory tract infections. Acad Med J. 2021;1(1):37-48.
283. Dequin P-F, Meziani F, Quenot J-P, et al. Hydrocortisone in severe community-acquired pneumonia. N Engl J Med 2023;388: 1931-41.
284. Meduri GU, Shih M-C, Bridges L, et al. Low-dose methyl- prednisolone treatment in critically ill patients with severe community-acquired pneumonia. Intensive Care Med 2022;48:1009- 23.
285. Grohskopf L.A., Blanton L.H., Ferdinands J.M., et al. Prevention and Control of Seasonal Influenza with Vaccines: Recommendations of the Advisory Committee on Immunization Practices - United States, 2023–24 Influenza Season. MMWR Morb Mortal Wkly Rep. 2023; 72(2): 1-25.
286. Giacobbe D.R., De Rosa F.G., Del Bono V., et al. Ceftobiprole: drug evaluation and place in therapy. Expert Rev Anti Infect Ther 2019; 17(9): 689-698.
287. Hawser S., Kothari N., Jemmely N., et al. Susceptibility of ceftobiprole against Gram-positive and Gram-negative clinical isolates from 2019 from different European territories. J Glob Antimicrob Resist 2022; 29: 393-397.
288. Bavaro D.F., Belati A., Bussini L., et al. Safety and effectiveness of fifth generation cephalosporins for the treatment of methicillin-resistant staphylococcus aureus bloodstream infections: a narrative review exploring past, present, and future. Expert Opin Drug Saf 2024; 23(1): 9-36.
289. Torres A., Kuraieva A., Stone G.G., et al. Systematic review of ceftaroline fosamil in the management of patients with methicillin-resistant Staphylococcus aureus pneumonia. Eur Respir Rev 2023; 32(170): 230117.
290. Nicholson S.C., Welte T., File T.M. Jr, et al. A randomised, double-blind trial comparing ceftobiprole medocaril with ceftriaxone with or without linezolid for the treatment of patients with community-acquired pneumonia requiring hospitalisation. Int J Antimicrob Agents 2012; 39(3): 240-6.
291. Bader J.C., Lakota E.A., Dale G.E., et.al. Pharmacokinetic-pharmacodynamic evaluation of ertapenem for patients with hospital-acquired or ventilator-associated bacterial pneumonia. Antimicrob Agents Chemother. 2019; 63(6): e00318-19.
292. Белообородов ВБ, Голощапов ОВ, Гусаров ВГ., и др. Методические рекомендации Российской некоммерческой общественной организации «Ассоциация анестезиологов-реаниматологов», Межрегиональной общественной организации «Альянс клинических химиотерапевтов и микробиологов», Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), общественной организации «Российский Сепсис Форум» «Диагностика и антимикробная терапия инфекций, вызванных полирезистентными штаммами микроорганизмов» (обновление 2022 г.). Вестник анестезиологии и реаниматологии. 2022;19(2):84–114.
293. Cosimi RA, Beik N, Kubiak DW, et al. Ceftaroline for Severe Methicillin-Resistant Staphylococcus aureus Infections: A Systematic Review. Open Forum Infect Dis. 2017 May 2;4(2):ofx084.
294.Комплекс программный для автоматической обработки радиологических изображений "Платформа RADLogics" по ТУ 58.29.32-320-17493389-2020, РЗН 2021/14627. Доступно на сайте: https://doi.org/10.1101/2023.08.31.23294896
295.Программное обеспечение для анализа исследований компьютерной томографии с помощью технологий искусственного интеллекта «Intelligent Radiology Assistants» по ТУ 58.29.32-001-44270315-2021, РЗН 2024/22895. Доступно на сайте: https://doi.org/10.1101/2023.08.31.23294896.
296. Программное обеспечение "Sciberia Lungs" автоматизированного анализа медицинских изображений компьютерной томографии лёгких по ТУ 58.29.32-001-354284672022, РЗН 2023/20608.
297. Программное обеспечение "JEMYS:ТЕЛЕМЕДИЦИНА с системой поддержки принятия решений при анализе рентгеновских изображений стандарта DICOM" по ТУ 58.29.32010-45327610-2020, РЗН 2021/16120.
298. Программное обеспечение ЦЕЛЬС® (ПО ЦЕЛЬС®) для автоматического анализа цифровых медицинских КТизображений органов грудной клетки по ТУ 58.29.32-00228139219-2021, РЗН 2024/21982.
299. Комплекс программ для регистрации, визуализации, обработки, архивирования, и передачи медицинских изображений и данных «Гамма Мультивокс» по ТУ 62.01.29-001-164283262018, РЗН 2021/13277.
300.Sergey Morozov, Anton Vladzymyrskyy, et al. Diagnostic accuracy of artificial intelligence for analysis of 1.3 million medical imaging studies: the Moscow experiment on computer vision technologies https://doi.org/10.1101/2023.08.31.23294896
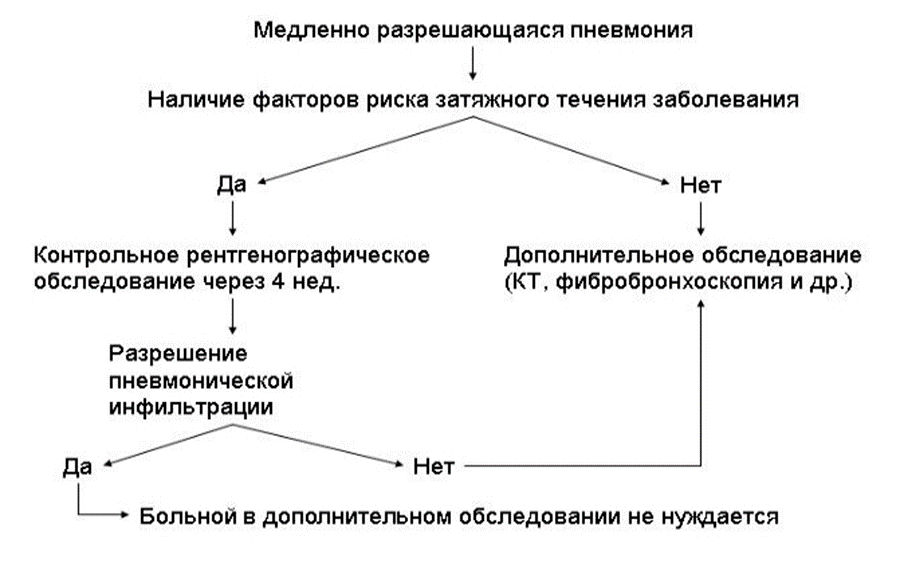
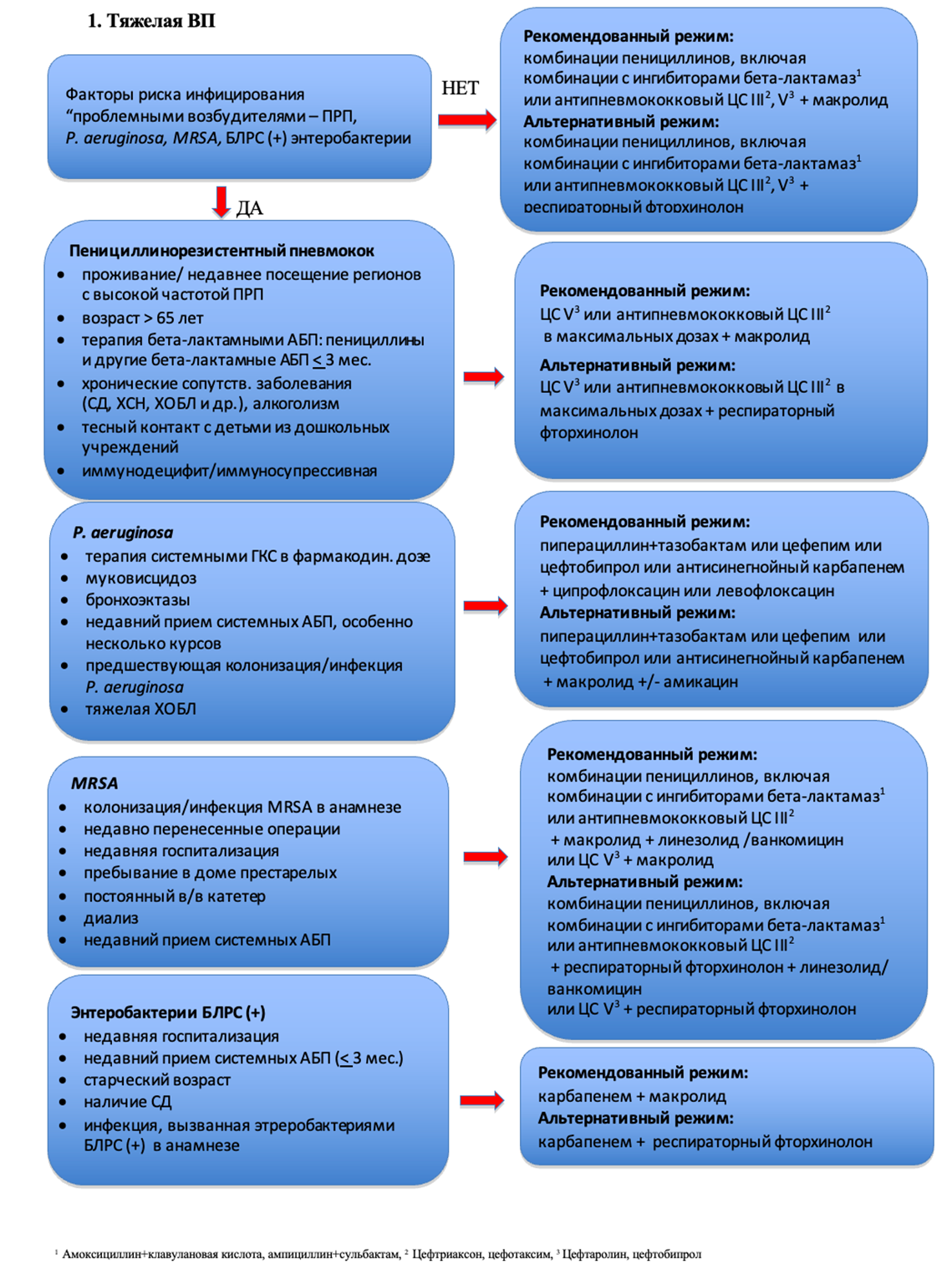
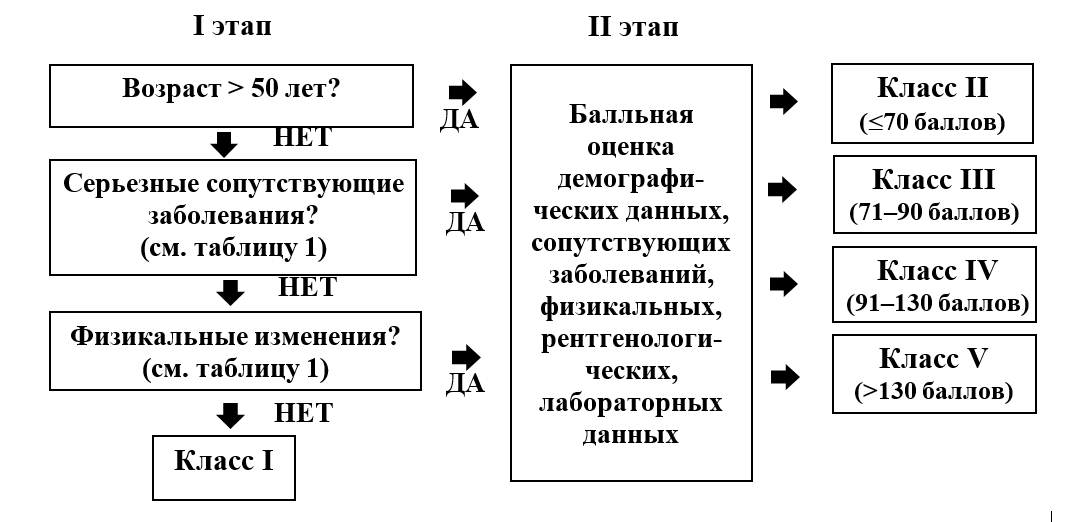 Таблица 1. Балльная оценка факторов риска неблагоприятного прогноза
Таблица 1. Балльная оценка факторов риска неблагоприятного прогноза